人教版初中化学2023-2024学年九年级下学期 金属材料和金属的化学性质练习卷
试卷更新日期:2024-01-27 类型:同步测试
一、选择题
-
1. “辽宁号”是我国第一艘航空舰.建造航母需要大量的特种钢材.钢材属于( )A、合成材料 B、天然材料 C、复合材料 D、金属材料2. 下列说法正确的是( )A、铁是地壳中含量最多的金属元素 B、纯铜硬度高于黄铜(铜锌合金) C、多数合金的抗腐蚀性能比组成它们的纯金属好 D、生铁和钢都是铁、碳形成的化合物3. 哈尔滨迎来入冬的第一场雪。冰雪路面严重影响交通,但使用先进的清雪车能够提高清雪效率。下列有关叙述错误的是( )
 A、清雪车以柴油作为燃料,柴油是石油分解得到的产品 B、清雪车的车体用到的铁合金属于混合物 C、清雪车的车体大量使用钢铁,车体喷漆起到防锈,美观,延长使用寿命的作用 D、清雪车行驶过程中实现了由化学能到机械能的转化4. 在氯化铜和氯化镁的混合溶液中,加入过量的锌粉,充分反应后过滤,留在滤纸上的物质是( )A、Zn B、Cu C、Cu和Mg D、Zn和Cu5. 金属活动性顺序表在化学学习中有重要作用,下列说法正确的是( )A、在Al、Mg、Fe中金属活动性最强的是Al B、“真金不怕火炼”说明金在高温时也不与氧气反应 C、Zn不能置换稀硫酸中的氢 D、Ag能将硝酸铜溶液中的铜置换出来6. 下列化学反应属于置换反应的是()A、2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ B、CaCO3+CO2+H2O=Ca(HCO3)2 C、2NaNO3 2NaNO2+O2↑ D、CuO+H2 Cu+H2O7. 现有X、Y、Z三种金属,如果把X和Y分别放入稀盐酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会,在Y表面有银析出,而Z没有变化,根据以上实验事实,相关分析错误的是( )A、三种金属可能分别是铁、铜、银 B、Y一定能从硫酸铜溶液中置换出铜 C、X与稀盐酸反应后溶液的质量一定增大 D、三种金属活动性由强到弱的顺序是X>Y>Z8. 可用于验证铜,铁,锌三种金属的金属活动性强弱的一组药品是( )A、Cu、Zn、FeSO4溶液 B、Cu、FeSO4溶液、ZnSO4溶液 C、Cu、Fe、ZnSO4溶液 D、Zn、FeSO4溶液、CuSO4溶液9. 现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X、Y在生成物中化合价均为+2价)。则下列说法中不正确的是( )
A、清雪车以柴油作为燃料,柴油是石油分解得到的产品 B、清雪车的车体用到的铁合金属于混合物 C、清雪车的车体大量使用钢铁,车体喷漆起到防锈,美观,延长使用寿命的作用 D、清雪车行驶过程中实现了由化学能到机械能的转化4. 在氯化铜和氯化镁的混合溶液中,加入过量的锌粉,充分反应后过滤,留在滤纸上的物质是( )A、Zn B、Cu C、Cu和Mg D、Zn和Cu5. 金属活动性顺序表在化学学习中有重要作用,下列说法正确的是( )A、在Al、Mg、Fe中金属活动性最强的是Al B、“真金不怕火炼”说明金在高温时也不与氧气反应 C、Zn不能置换稀硫酸中的氢 D、Ag能将硝酸铜溶液中的铜置换出来6. 下列化学反应属于置换反应的是()A、2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ B、CaCO3+CO2+H2O=Ca(HCO3)2 C、2NaNO3 2NaNO2+O2↑ D、CuO+H2 Cu+H2O7. 现有X、Y、Z三种金属,如果把X和Y分别放入稀盐酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会,在Y表面有银析出,而Z没有变化,根据以上实验事实,相关分析错误的是( )A、三种金属可能分别是铁、铜、银 B、Y一定能从硫酸铜溶液中置换出铜 C、X与稀盐酸反应后溶液的质量一定增大 D、三种金属活动性由强到弱的顺序是X>Y>Z8. 可用于验证铜,铁,锌三种金属的金属活动性强弱的一组药品是( )A、Cu、Zn、FeSO4溶液 B、Cu、FeSO4溶液、ZnSO4溶液 C、Cu、Fe、ZnSO4溶液 D、Zn、FeSO4溶液、CuSO4溶液9. 现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X、Y在生成物中化合价均为+2价)。则下列说法中不正确的是( ) A、生成氢气的质量:X>Y B、相对原子质量:X>Y C、金属活动性:Y>X D、消耗硫酸的质量:X>Y10. 为验证锌、铁、铜三种金属的活动性顺序,小西设计了如图所示的四个实验,下列说法中不正确的是( )
A、生成氢气的质量:X>Y B、相对原子质量:X>Y C、金属活动性:Y>X D、消耗硫酸的质量:X>Y10. 为验证锌、铁、铜三种金属的活动性顺序,小西设计了如图所示的四个实验,下列说法中不正确的是( ) A、通过实验①②能验证锌的金属活动性比铜的强 B、实验③中反应后溶液的质量变大 C、X可能为锌,Y可能为硫酸亚铁 D、只做实验③和④,可以验证锌、铁、铜的金属活动性顺序
A、通过实验①②能验证锌的金属活动性比铜的强 B、实验③中反应后溶液的质量变大 C、X可能为锌,Y可能为硫酸亚铁 D、只做实验③和④,可以验证锌、铁、铜的金属活动性顺序二、填空题
-
11. 大国重器“深海一号”是我国首个自主勘探开发的超深水大气田,它的二期工程已全面开工建设,为我国深化油气勘探开发又迈出可喜一步。海面上部桁架式组块及海底管道运用了大量的钢构件,钢属于材料,它的主要成分是 , 为防止其生锈,可采取的措施是。12. 金属的应用非常广泛。(1)、生活中常用铁锅炒菜,主要是利用了铁的____。A、导电性 B、导热性 C、延展性 D、有金属光泽(2)、目前世界上已有50%以上的废钢铁得到回收利用,其目的是____。A、节约金属资源 B、合理开采矿物 C、防止钢铁生锈(3)、常温下,铁生锈的条件是铁接触空气中的和。(4)、防止钢铁制品生锈常用的方法是(举一个实例)。13. 用铜制电线主要是利用铜具有良好的;铝制品耐腐蚀是因其表面生成了致密的薄膜,反应的化学方程式为;如图(U型管中装有红墨水)的密封性能完好,一段时间后,观察到的现象是。
 14. 将一根锃亮的铁丝放入蓝色的硫酸铜溶液中,过一会儿,发现铁丝表面出现了红色物质。(1)、写出发生反应的化学方程式:。(2)、由此判断,金属的活动性:FeCu(用“>”、“=”、“<”填空)。(3)、在化学反应中,元素化合价升高的反应物是还原剂,元素化合价降低的反应物是氧化剂。试判断上述反应中,氧化剂是。15. 金属材料的使用作为一个时代的标志,见证了人类文明发展的进程。(1)、《天工开物》是我国乃至世界科技史上一部极具价值的著作。书中记载“凡金箔每金七分造方寸金一千片”,体现金的哪种物理性质:。(2)、第24届冬奥会发行的冬奥币使用的材料是黄铜(铜锌合金)。黄铜和纯铜相互刻画,表面没有划痕的是。(3)、我国早在春秋战国时就开始炼铁。生铁生产过程中,一氧化碳与氧化铁在高温下反应的化学方程式为。(4)、金属锰(Mn)及其化合物用途广泛。经查阅,锰的化合物在水中溶解性如下:
14. 将一根锃亮的铁丝放入蓝色的硫酸铜溶液中,过一会儿,发现铁丝表面出现了红色物质。(1)、写出发生反应的化学方程式:。(2)、由此判断,金属的活动性:FeCu(用“>”、“=”、“<”填空)。(3)、在化学反应中,元素化合价升高的反应物是还原剂,元素化合价降低的反应物是氧化剂。试判断上述反应中,氧化剂是。15. 金属材料的使用作为一个时代的标志,见证了人类文明发展的进程。(1)、《天工开物》是我国乃至世界科技史上一部极具价值的著作。书中记载“凡金箔每金七分造方寸金一千片”,体现金的哪种物理性质:。(2)、第24届冬奥会发行的冬奥币使用的材料是黄铜(铜锌合金)。黄铜和纯铜相互刻画,表面没有划痕的是。(3)、我国早在春秋战国时就开始炼铁。生铁生产过程中,一氧化碳与氧化铁在高温下反应的化学方程式为。(4)、金属锰(Mn)及其化合物用途广泛。经查阅,锰的化合物在水中溶解性如下:MnCl2
MnSO4
MnCO3
Mn (NO3) 2
Mn (OH) 2
易溶
易溶
难溶
易溶
难溶
锰的金属活动性介于镁和铜之间。结合以上信息和已有知识,判断下列说法正确的是____。
A、锰不能与稀硫酸反应 B、锰能与硫酸铜溶液反应 C、碳酸锰不能与稀盐酸反应 D、硫酸锰溶液能与氢氧化钠溶液反应16. 金属在生产、生活和社会发展中有着广泛的应用。(1)、铝制品耐腐蚀的原因是。(2)、铁与空气中的O2和H2O发生反应锈蚀,请列举一种家庭中菜刀防锈的方法。(3)、某废液含有Fe(NO3)2、Cu(NO3)2、AgNO3 , 小组同学设计如下方案回收Ag:滤液A的溶质是 , 步骤Ⅲ中发生反应的化学方程式是。 17. 金属资源在生产生活中应用十分广泛。请回答下列问题。(1)、“共享单车”方便市民出行,颇受人们的喜爱。
17. 金属资源在生产生活中应用十分广泛。请回答下列问题。(1)、“共享单车”方便市民出行,颇受人们的喜爱。
①如图所示,单车上标示出的部件中由金属材料制成的是(填字母序号)。
②为防止钢链条生锈可采取的措施是。
③废旧单车中金属部件回收再利用的意义是(写一点即可)。
(2)、向硝酸银、硝酸镁的混合溶液中加入一定量铁粉和锌粉的混合物,充分反应后过滤,得到滤渣和滤液。若向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有(填化学式,下同);若滤液呈浅绿色,则滤液中一定含有的溶质有。18. 某工厂从废旧电子产品在回收部分金属的流程图如下。
已知:硫酸镍的化学式为NiSO4;。滤液1中的溶质为 , Cu、Fe、Ni的活动性由弱到强的顺序为 , 固体A的成分是(写化学式)。
三、科普阅读题
-
19. 仔细阅读下列材料
19世纪初,铝是比黄金还贵的金属,主要是由于铝的化学性质很活泼,在自然界中以化合物的形式存在。当时采用的与氯化铝在一定条件下发生反应得到铝,反应方程式为3Na+AlCl33NaCl+Al,因为生产成本高,所以铝十分珍贵。
19世纪末,霍尔应用电解熔融金属化合物的方法制备金属。他在用氧化铝制备金属鋁的过程中,发现氧化铝的熔点很高,很难达到熔融状态,必须物色一种能够溶解氧化铝且又能降低其熔点的材料,实验过程中他发现冰晶石(Na3AlF6)能起到这种作用。他把氧化鋁溶解在10%~15%的熔融的冰晶石里进行电解,发现有银白色小球状的铝生成,冰晶石在电解过程中不被分解,并有足够的流动性,有利于电解的进行。这种廉价炼铝方法的发现,使铝成为广泛应用的金属材料。
阅读文本,回答问题:
(1)、自然界中,以单质形式存在的金属有(举一例)。铝制品耐腐蚀的原因是。(2)、冰晶石中氟元素的化合价为。(3)、19世纪初,采用钠与氯化铝在一定条件下发生反应得到铝,该反应的基本反应类型是。(4)、写出通电分解氧化铝的化学方程式。(5)、由文中可知,金属广泛应用于生活生产与该金属有关。四、推断题
-
20. 根据下列化合物与单质相互转化的关系,回答:
 (1)、若乙的溶液为浅绿色,Y是红色固体,则X是;任写一个方程式:;(2)、若在常温下乙是气体,则X是;任写一个方式:。
(1)、若乙的溶液为浅绿色,Y是红色固体,则X是;任写一个方程式:;(2)、若在常温下乙是气体,则X是;任写一个方式:。五、实验探究题
-
21. M是生产、生活中常见的金属。张老师化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动。
【查阅资料】MSO4溶液是无色液体。
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】
(1)、小玉的猜想是M>Al>Cu;小静的猜想是Al>M>Cu;你的猜想是。(2)、【设计与实验一】小影取长短、粗细相同的M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有相同体积、相同浓度的稀盐酸):
实验操作
M丝插入试管①中
铜丝插入试管②中
铝丝插入试管③中
实验结论
刚开始的现象
有少量气泡产生
无气泡
无气泡
M>Cu;M>Al
几分钟后的现象
有少量气泡产生
无气泡
有大量气泡产生
【交流与表达】同学们对同一实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中无气泡产生的原因是铝丝表面的氧化膜与稀盐酸反应,因而无气泡产生。
(3)、【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取长短、粗细相同、打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
试管乙中观察到的现象是。
(4)、试管丙中反应的化学方程式为。(5)、【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管(填试管编号)中的实验,也可以得出正确的结论。【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序。
(6)、【评价与反思】实验结束后,同学们对实验过程进行了如下反思:影响金属与酸反应速率快慢的因素,除了相互反应的金属和酸的性质外,还与温度以及等因素有关(任写一种即可)。
六、计算题
-
22. 欲测定Cu-Zn合金及Cu-Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器,并进行了如图所示的实验。
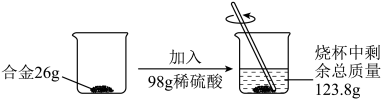 (1)、你认为能测出质量分数的是合金。(2)、计算该合金中铜的质量分数。
(1)、你认为能测出质量分数的是合金。(2)、计算该合金中铜的质量分数。
-
-
-