江苏省苏州市工业园区2023-2024学年九年级上学期12月月考化学试题
试卷更新日期:2024-01-25 类型:月考试卷
一、选择题
-
1. 中华文明源远流长,文物承载着文明的记忆。下列苏州博物馆馆藏文物中主要由金属材料制成的是( )A、清代瓷盘
 B、明代书轴
B、明代书轴 C、西周铜鼎
C、西周铜鼎 D、宋代石函
D、宋代石函 2. 空气由多种气体组成,其中体积分数约为21%的物质是( )A、 B、He C、 D、3. 人体中化学元素的多少直接影响健康。缺乏下列哪种元素易导致侏儒症( )A、锌 B、钙 C、碘 D、铁4. 苏州平江路河道水清见底,道尽江南之美。下列关于河水处理和保护的说法正确的是( )A、水中大颗粒的泥沙可通过静置沉降的方法除去 B、通过生态膜物理过滤可将河水中的离子全部滤去 C、为使河水变清澈可将河水蒸馏冷凝 D、厨房废水滤去固体后可直接排向河道5. 某些含氟化合物有利于保护牙齿。氟在元素周期表中的信息如图所示,下列有关说法正确的是( )
2. 空气由多种气体组成,其中体积分数约为21%的物质是( )A、 B、He C、 D、3. 人体中化学元素的多少直接影响健康。缺乏下列哪种元素易导致侏儒症( )A、锌 B、钙 C、碘 D、铁4. 苏州平江路河道水清见底,道尽江南之美。下列关于河水处理和保护的说法正确的是( )A、水中大颗粒的泥沙可通过静置沉降的方法除去 B、通过生态膜物理过滤可将河水中的离子全部滤去 C、为使河水变清澈可将河水蒸馏冷凝 D、厨房废水滤去固体后可直接排向河道5. 某些含氟化合物有利于保护牙齿。氟在元素周期表中的信息如图所示,下列有关说法正确的是( )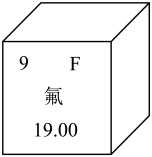 A、氟属于金属元素 B、氟的相对原子质量为9 C、氟单质在常温常压下为气体 D、氟原子失去1个电子形成6. 阅读下列材料,完成下面小题:
A、氟属于金属元素 B、氟的相对原子质量为9 C、氟单质在常温常压下为气体 D、氟原子失去1个电子形成6. 阅读下列材料,完成下面小题:火药是我国的四大发明之一。黑火药的主要成分有硫黄、硝酸钾、木炭,爆炸时发生的主要反应为:。
下列相关物质中属于氧化物的是( )
A、 B、 C、 D、C7. 下列相关化学用语表述正确的是( )A、——硫酸钾 B、——硝酸根离子 C、——碳元素的化合价 D、——氮分子8. 下列关于黑火药的说法不正确的是( )A、黑火药爆炸时产生大量气体 B、黑火药爆炸前后固体质量不变 C、黑火药爆炸时可能有生成 D、黑火药保存时应该远离火源9. 下列等量关系一定成立的是( )A、氢气与氧气充分反应,生成水 B、通常情况下,氢气和氧气反应,生成水 C、酒精与水混合,形成酒精溶液 D、氢氧化钠稀溶液与硫酸铜溶液混合,形成混合物10. 人类从来就没有停止过对物质世界构成规律的探索。下列说法正确的是( )A、汤姆生提出了原子学说 B、道尔顿确认原子内部有电子 C、拉瓦锡研究出原子结构 D、门捷列夫发表了元素周期表11. 下列物质由离子构成的是( )A、铜 B、二氧化碳 C、氯化钠 D、金刚石12. 下列有关金属的说法正确的是( )A、所有金属都呈银白色 B、青铜和黄铜都属于纯净物 C、金属在空气中都易被氧化 D、生铁和钢都属于铁的合金13. 下列物质性质和用途对应关系正确的是( )A、活性炭有吸附性,可用作除味剂 B、铝有导热性,可用于制电线 C、石墨有导电性,可用作润滑剂 D、镁是银白色金属,可用于制作烟花14. 重氢可应用于光导纤维制备。重氢和氢都属于氢元素,是因为它们的原子具有相同的( )A、质子数 B、中子数 C、体积 D、相对原子质量15. 用如图所示装置进行电解水实验(水中加入少量氢氧化钠溶液以增强导电性),反应一段时间。下列说法正确的是( )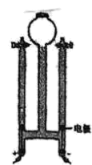 A、球形容器内液面上升 B、该实验说明水是由氢气和氧气组成的 C、与电源正极相连的玻璃管内产生的气体体积约为负极的两倍 D、与电源负极相连的玻璃管内产生的气体能使带火星的木条复燃16. 如图是“光催化固氮合成氨”反应前后分子种类变化的示意图。下列叙述正确的是( )
A、球形容器内液面上升 B、该实验说明水是由氢气和氧气组成的 C、与电源正极相连的玻璃管内产生的气体体积约为负极的两倍 D、与电源负极相连的玻璃管内产生的气体能使带火星的木条复燃16. 如图是“光催化固氮合成氨”反应前后分子种类变化的示意图。下列叙述正确的是( )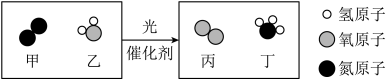 A、乙和丙都是氧化物 B、参加反应的甲和乙的分子个数比为 C、反应后原子数目增加 D、反应生成的丙和丁的质量比为17. “化学链燃烧”是指燃料不直接与空气接触,而是以载氧体在两个反应器之间的循环来实现燃料较低温度下燃烧的过程。某“化学链燃烧”的过程如下:
A、乙和丙都是氧化物 B、参加反应的甲和乙的分子个数比为 C、反应后原子数目增加 D、反应生成的丙和丁的质量比为17. “化学链燃烧”是指燃料不直接与空气接触,而是以载氧体在两个反应器之间的循环来实现燃料较低温度下燃烧的过程。某“化学链燃烧”的过程如下:
下列叙述错误的是( )
A、空气反应器中发生的反应为: B、X中氮气的含量比空气中高 C、与直接燃烧相比,“化学链燃烧”有利于二氧化碳的捕集 D、等质量的甲烷直接燃烧比“化学链燃烧”消耗氧气多18. 下列除杂方法能达到实验目的的是(括号中的物质为杂质)( )选项
物质
除杂方法
A
在空气中点燃
B
加入过量稀盐酸
C
加足量水溶解、过滤、洗涤、烘干
D
加入 , 并加热至不再产生气体为止
A、A B、B C、C D、D19. “价类二维图”是从元素化合价和物质所属类别两个维度认识元素及其化合物性质的坐标图。下图是铁元素的“价类二维图”,下列说法正确的是( )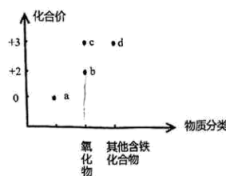 A、是单质 B、是铁丝在氧气中燃烧的产物 C、在通常情况下是黑色的固体 D、可能是铁与稀硫酸反应的产物20. 一种阻燃剂的化学式可表示为Mga(OH)b(CO3)c。其受热分解反应可表示如下:
A、是单质 B、是铁丝在氧气中燃烧的产物 C、在通常情况下是黑色的固体 D、可能是铁与稀硫酸反应的产物20. 一种阻燃剂的化学式可表示为Mga(OH)b(CO3)c。其受热分解反应可表示如下:(未配平)
取3.94g样品(杂质忽略不计)在空气中灼烧至固体质量不再减少,得到MgO2.00g和CO21.76g。下列说法正确的是( )
A、阻燃剂化学式中a=b+c B、样品分解时产生水0.18g C、样品中含镁元素的质量分数为 D、加热时该阻燃剂比MgO稳定二、非选择题
-
21. 苏州是国家首批历史文化名城之一,有着深写的文化积淀。(1)、姑苏美食,传承苏州味道。
①苏帮菜香味四溢,说明分子在。
②在人体内葡萄糖转化为二氧化碳,属于(填“物理变化”或“化学变化”)。
(2)、文化遗产,传承苏州底蕴。“姜思序堂”是苏州制作国画颜料的老字号,故宫博物院文物修复所需的颜料大多出自姜思序堂。石青就是青绿山水画所需要的重要颜料。石青的主要成分是碱式碳酸铜。
①中碳原子和氧原子的个数比为。
②受热分解会生成三种氧化物,写出反应的化学方程式。
(3)、轨交高铁,展现苏州速度。①高铁的运营离不开高性能的芯片。生产芯片的可用与在高温下反应获得,同时产生。该反应的化学方程式为。
②制造交通工具的铝合金表面容易形成一层 , 可有效保护金属材料。
22. 燃烧是生活中常见的化学反应。(1)、水无法被点燃,纸张能燃烧,说明发生燃烧的物质须有 性。(2)、酒精(化学式C2H6O)与O2反应生成8.8gCO2、5.6gCO和一定质量的H2O,则生成H2O的质量为。(3)、将一块棉布浸泡在某浓度的酒精溶液中,取出后点燃,一段时间后火焰熄灭,棉布完好无损,棉布未烧坏的原因是 。(4)、根据不同的起火原因选择不同的灭火方式。①活泼金属(如K、Na、Mg等)能在二氧化碳中燃烧,高温下能与水反应产生氢气,金属镁着火最好选用 灭火(填字母)。
A干冰 B水 C湿抹布 D沙土
②用电器着火不能用水扑灭,可选用四氯化碳,灭火时液态四氯化碳迅速转化为气态并覆盖在火焰上,由此推断四氯化碳可能具有的性质有。
23. 请回答下列实验问题: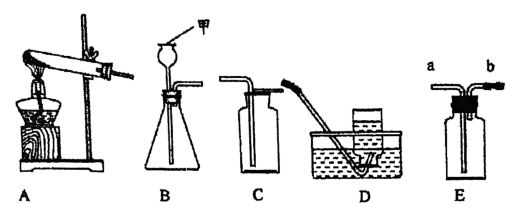 (1)、甲仪器的名称是。(2)、实验室用双氧水和二氧化锰制氧气的化学方程式为 , 可用C装置收集O2的原因是。(3)、实验室制备的化学方程式为;通常用澄清石灰水检验气体,其化学方程式为。(4)、用装置能完成的实验是____(填字母序号)。A、瓶内不放任何物质,从a端通入,用排空气法收集 B、瓶内装满水,a端连接导管伸入量筒,从b端通入,测量的体积 C、瓶内盛有可以吸水的液体,气体由导管端进入,除去中的少量水蒸气(5)、实验室可选用序号为的气体发生装置来制取。(6)、稀硫酸与两种金属混合物混合时的微观变化情况如下图所示:
(1)、甲仪器的名称是。(2)、实验室用双氧水和二氧化锰制氧气的化学方程式为 , 可用C装置收集O2的原因是。(3)、实验室制备的化学方程式为;通常用澄清石灰水检验气体,其化学方程式为。(4)、用装置能完成的实验是____(填字母序号)。A、瓶内不放任何物质,从a端通入,用排空气法收集 B、瓶内装满水,a端连接导管伸入量筒,从b端通入,测量的体积 C、瓶内盛有可以吸水的液体,气体由导管端进入,除去中的少量水蒸气(5)、实验室可选用序号为的气体发生装置来制取。(6)、稀硫酸与两种金属混合物混合时的微观变化情况如下图所示:
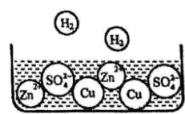
①未参加反应的金属名称是。
②发生反应的化学方程式为。
③根据图示,下列有关说法正确的是。
A.反应中每个锌原子得到2个电子,生成锌离子
B.从微观角度分析,该反应生成的新微粒是锌离子和氢分子
C.从反应的类型来看,该反应属于置换反应
D.从化合价角度看,该反应有3种元素化合价发生变化
(7)、科学家认为“氢能将成为未来的主要能源”,但制氢和储氢问题仍然是氢能开发和利用要面临的困难,化学储氢材料的研发是当下科技研究的热点之一。I.下列化学储氢材料中含烃量(即氢元素的质量分数)最高的是(填字母)。
A. B. C.
II.我国科学家发明了一种将甲烷中的氢转化为氢气的工艺(原理如图所示)。
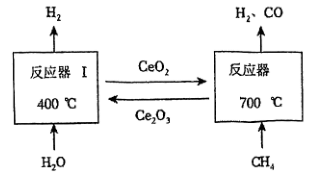
总反应的化学反应方程式为
①反应器I中的化学反应方程式为。
②当甲烷的转化率()为时,理论上1.0t甲烷与足量水反应前甲烷的质量蒸气反应生成氢气的总质量是多少t?(写出计算过程)
24. 阅读下列短文,回答相关问题。科技助力人工碳循环
中国的经济发展离不开大量的能源,目前我国的能源结构中以煤(高碳)、石油(中碳)、天然气(低碳)为代表的化石燃料仍占主导地位,化石燃料的燃烧在释放热量的同时产生 , 是最主要的温室气体。低碳、零碳、负碳技术的开发是我国科学家正致力研发的项目。
也是巨大的碳资源。目前,的低能耗捕集、转化和利用正受到世界各国的广泛关注。根据与其他能源的耦合方式不同,的转化利用技术可分为以下三条途径。
途径1:耦合化石能源的转化利用技术。如与催化重整为与CO。
途径2:耦合零碳能源的转化利用技术。如图所示是我国科研团队利用催化剂实现低温、高效、长寿命催化加氢制甲醇()的工艺。
途径3:直接转化利用技术。如以太阳能或其他可再生能源发电为驱动力,在温和条件下将直接转化为化学原料或燃料。
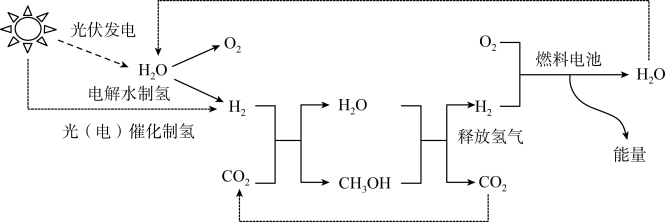
科学技术的研发和应用将促进自然界碳循环回归平衡。如何摆脱对含碳化石能源的依赖,转化利用丰富的资源,跨越低碳及创新新能源,拥抱新式零碳能源,期待同学们学好和利用化学开创未来。
(1)、写出自然界中吸收的一条途径:。(2)、氢氧燃料电池的能量转化形式是将化学能转化为。(3)、我国科学家将直接转化成葡萄糖的过程中,第一阶段的反应可表示为: , R的化学式是。(4)、写出和在催化剂和加热条件下转化为甲醇()的化学方程式:。(5)、下列叙述正确的是(填序号)。a.、与在一定条件下可相互转化
b.途径2解决了氢气低成本制取和有效储存的难题
c.能源的开发与利用向“减碳趋氢”的方向发展
25. 废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。现设计如下实验,以回收其中的铜。已知:①金、银的金属活动性比较弱,不与稀硫酸反应。
②;不考虑金、银发生类似反应。
③每一步反应假设完全。
 (1)、将电路板粉碎成粉末的目的是。(2)、步骤①所得滤液中的阳离子有。(3)、步骤②所得滤渣的成分是。(4)、步骤③中一定发生反应的化学方程式是。(5)、步骤④中反应的实验现象:。26. 实验室以软锰矿(主要含的矿石)为原料制备的流程如下:
(1)、将电路板粉碎成粉末的目的是。(2)、步骤①所得滤液中的阳离子有。(3)、步骤②所得滤渣的成分是。(4)、步骤③中一定发生反应的化学方程式是。(5)、步骤④中反应的实验现象:。26. 实验室以软锰矿(主要含的矿石)为原料制备的流程如下: (1)、催化分解的化学反应方程式为。(2)、“酸浸”时,为使软锰矿充分反应,可采取的措施有(写一条)。(3)、“沉锰”反应为。加热温度不能过高的原因是。(4)、在空气中“煅烧”会生成不同的锰氧化物,各锰氧化物质量分数随煅烧温度的变化关系如图所示。
(1)、催化分解的化学反应方程式为。(2)、“酸浸”时,为使软锰矿充分反应,可采取的措施有(写一条)。(3)、“沉锰”反应为。加热温度不能过高的原因是。(4)、在空气中“煅烧”会生成不同的锰氧化物,各锰氧化物质量分数随煅烧温度的变化关系如图所示。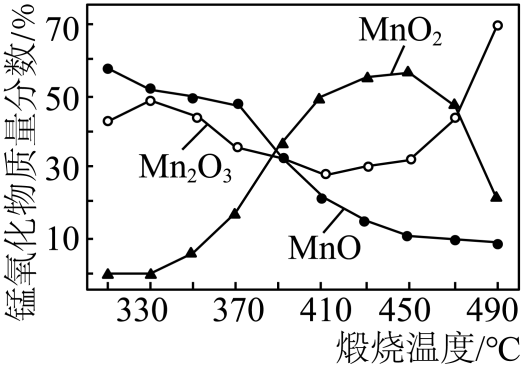
①370~410℃发生主要反应为。该反应属于基本反应类型中的反应。
②已知酒精灯外焰的最高温度可达600℃以上。称取一定质量的 , 与混合均匀,充分加热后冷却,溶解、过滤、洗涤、烘干后称量,发现固体质量减少。质量减少的主要原因是。