河北省秦皇岛市北戴河区2023-2024学年九年级上学期期末复习化学试题
试卷更新日期:2024-01-25 类型:期末考试
一、选择题(本题共20个小题,每小题2分,共 40分。下列各题,每小题只有一个选项符合题意。)
-
1. 下列过程中发生了物理变化的是( )A、葡萄酿酒 B、玻璃破碎 C、纸张燃烧 D、金属锈蚀2. 中学生应有一定的安全常识. 发现火险或遇火灾时,下列做法不正确的是( )A、液化气泄漏起火时,首先关闭阀门 B、炒菜油锅内着火,立即盖上锅盖灭火 C、室内起火时,立即打开所有门窗通风 D、被困时,用湿毛巾捂住口鼻低下身子逃生3. 下列各图所表示的化学实验操作正确的是( )A、
 闻气体气味
B、
闻气体气味
B、 倾倒液体
C、
倾倒液体
C、 添加药品
D、
添加药品
D、 检查气密性
4. 分子、原子、离子等都是构成物质的微粒.下列物质由离子构成的是( )A、氯化钠 B、黄金 C、金刚石 D、干冰5. 青少年正处于成长期,需要摄入足量钙,这里的“钙”是指( )A、原子 B、元素 C、分子 D、单质6. 北斗系统的全面建成彰显了中国航天的力量。在航天科技中运用了大量金属材料,下列有关金属材料的说法正确的是( )A、合金中一定只含金属元素 B、金属单质在常温下都是固体 C、生铁和钢都是铁的合金,且生铁的含碳量更高 D、纯金属的硬度一般比它们组成合金的硬度更高7. 不同温度下KNO3的溶解度如下表所示。下列说法正确的是( )
检查气密性
4. 分子、原子、离子等都是构成物质的微粒.下列物质由离子构成的是( )A、氯化钠 B、黄金 C、金刚石 D、干冰5. 青少年正处于成长期,需要摄入足量钙,这里的“钙”是指( )A、原子 B、元素 C、分子 D、单质6. 北斗系统的全面建成彰显了中国航天的力量。在航天科技中运用了大量金属材料,下列有关金属材料的说法正确的是( )A、合金中一定只含金属元素 B、金属单质在常温下都是固体 C、生铁和钢都是铁的合金,且生铁的含碳量更高 D、纯金属的硬度一般比它们组成合金的硬度更高7. 不同温度下KNO3的溶解度如下表所示。下列说法正确的是( )温度/℃
20
30
40
溶解度/g
31.6
45.8
63.9
A、20℃时,100gKNO3饱和溶液中溶质质量为31.6g B、30℃时,KNO3的饱和溶液加入NaCl不能继续溶解 C、30℃时,将50gKNO3放入100g水中得到150g溶液 D、40℃时,100g水最多溶解63.9gKNO38. 下列实验设计中不能达到目的的是( )A、探究同种物质在不同溶剂中的溶解性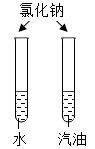 B、探究可燃物燃烧的条件
B、探究可燃物燃烧的条件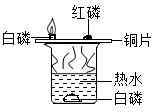 C、探究铁生锈的条件
C、探究铁生锈的条件 D、探究二氧化碳和水的反应
D、探究二氧化碳和水的反应 9. 下列化学方程式中,书写正确的是( )A、 B、 C、 D、10. 实验课上,同学们设计了如下四个实验,其中能达到目的是( )A、实验室制取氢气
9. 下列化学方程式中,书写正确的是( )A、 B、 C、 D、10. 实验课上,同学们设计了如下四个实验,其中能达到目的是( )A、实验室制取氢气 B、白磷在水中燃烧
B、白磷在水中燃烧  C、防止铁丝生锈
C、防止铁丝生锈  D、测定空气里氧气含量
D、测定空气里氧气含量  11. 某同学不小心将Fe掉入浓硫酸中,发现溶液颜色变黄,并生成一种有刺激性气味的气体,该气体可能是( )A、H2 B、SO2 C、HCl D、NH312. 我国古代炼丹家魏伯阳著有《周易参同契》是世界上现存最早的一部炼丹专著。书中描写到:“金入于猛火,色不夺精光”,这句话是指黄金的性质在强热的条件下( )A、易还原 B、较活泼 C、易氧化 D、较稳定13. 金银花是在预防新冠肺炎时用到的一味传统中药,其中起抗菌杀毒作用的有效成分是绿原酸和异绿原酸(化学式为C25H24O12)。下列对异绿原酸描述正确的是( )A、异绿原酸属于氧化物 B、异绿原酸中氢、氧元素的质量比是2:1 C、异绿原酸中氢元素的质量分数最小 D、异绿原酸由25个碳原子、24个氢原子、12个氧原子构成14. 推理是一种重要的化学思维方式,以下推理不正确的是( )A、干冰升华可以吸收大量的热,则干冰可用于人工降雨 B、单质是由同种元素组成的,则由同种元素组成的纯净物一定是单质 C、煤粉比煤块在空气燃烧更剧烈,则可燃物与氧气的接触面积越大燃烧越剧烈 D、化学反应通常伴随着能量变化,则人类利用的能量都是由化学反应提供的15. 如图是电解水的实验装置。下列说法中,正确的是( )
11. 某同学不小心将Fe掉入浓硫酸中,发现溶液颜色变黄,并生成一种有刺激性气味的气体,该气体可能是( )A、H2 B、SO2 C、HCl D、NH312. 我国古代炼丹家魏伯阳著有《周易参同契》是世界上现存最早的一部炼丹专著。书中描写到:“金入于猛火,色不夺精光”,这句话是指黄金的性质在强热的条件下( )A、易还原 B、较活泼 C、易氧化 D、较稳定13. 金银花是在预防新冠肺炎时用到的一味传统中药,其中起抗菌杀毒作用的有效成分是绿原酸和异绿原酸(化学式为C25H24O12)。下列对异绿原酸描述正确的是( )A、异绿原酸属于氧化物 B、异绿原酸中氢、氧元素的质量比是2:1 C、异绿原酸中氢元素的质量分数最小 D、异绿原酸由25个碳原子、24个氢原子、12个氧原子构成14. 推理是一种重要的化学思维方式,以下推理不正确的是( )A、干冰升华可以吸收大量的热,则干冰可用于人工降雨 B、单质是由同种元素组成的,则由同种元素组成的纯净物一定是单质 C、煤粉比煤块在空气燃烧更剧烈,则可燃物与氧气的接触面积越大燃烧越剧烈 D、化学反应通常伴随着能量变化,则人类利用的能量都是由化学反应提供的15. 如图是电解水的实验装置。下列说法中,正确的是( ) A、电解水的方程式为 B、实验说明水是由氢气和氧气组成的 C、试管2管内产生的气体能使带火星木条复燃 D、试管1、2中产生气体的质量比为2:116. 将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下:在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法错误的是( )
A、电解水的方程式为 B、实验说明水是由氢气和氧气组成的 C、试管2管内产生的气体能使带火星木条复燃 D、试管1、2中产生气体的质量比为2:116. 将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下:在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法错误的是( )物质
a
b
c
d
反应前质量(g)
10
10
10
2
反应后质量(g)
待测
2
21
2
A、该反应是化合反应,d可能是催化剂 B、a、b两种物质中元素种类一定与c物质中元素种类相同 C、b物质可能是单质 D、反应后a物质的质量为3g17. 某地质科考人员野外考察时,发现了一种能在氧气中燃烧的带螺纹的矿石,发生的主要反应是 , 下列说法正确的是( )A、SO2的排放能引起酸雨 B、Fe2O3中铁、氧元素的质量比是2:3 C、氧气由两个氧原子构成 D、物质X的化学式是Fe4S818. 化学用语是学习化学的重要工具。下列化学用语所表达的意义正确的是( )A、Ba2+表示钡元素化合价为+2价 B、Mg既可表示镁元素,又可表示镁单质 C、2H表示两个氢分子 D、H2O2表示一个过氧化氢分子中含有一个氢分子和一个氧分子19. 下列4个图像中,能正确反映变化关系的是( )A、 将水通电电解一段时间
B、
将水通电电解一段时间
B、 用红磷燃烧的方法测量空气中氧气的含量
C、
用红磷燃烧的方法测量空气中氧气的含量
C、 加热分解高锰酸钾
D、
加热分解高锰酸钾
D、 用两份完全相同的过氧化氢溶液分别制取氧气
20. 举例是掌握化学规律的重要方法。针对下列化学规律所举示例中错误的是( )
用两份完全相同的过氧化氢溶液分别制取氧气
20. 举例是掌握化学规律的重要方法。针对下列化学规律所举示例中错误的是( )选项
化学规律
示例
A
结构决定性质
原子的最外层电子数决定元素的化学性质
B
性质决定用途
氧气具有助燃性,常用做燃料
C
性质决定鉴别方法
一氧化碳与二氧化碳——用燃着的木条
D
现象决定本质
久置的澄清石灰水变浑浊,是由于石灰水与空气中的二氧化碳反应生成了难溶的碳酸钙
A、A B、B C、C D、D二、填空题(共6题,总计 35分)
-
21. 空气和水是自然界赠与人类最珍贵的资源。(1)、空气中含量较多且常用作保护气的气体为。(2)、生活需要干净的水,净化水时利用活性炭的性来除去色素和异味。22. 在高温条件下,碳单质不仅能与金属氧化物反应,还能与非金属氧化物反应,碳与二氧化碳反应的化学方程式为;潜水员戴的呼吸面具中装有过氧化钠(Na2O2),它能吸收人体呼出的二氧化碳,其反应原理是 , 则X的化学式为。23. 化学在日常生活、能源和科学技术等领域有广泛应用。(1)、科学家用Xe(氙气)首次合成了XePtF6 , 在XePtF6中Xe、F分别显+1、―1价,则XePtF6中Pt(铂)的化合价是。(2)、氢氧燃料电池是一种新型电池,氢气可通过以下反应获取:2NaCl+2H2O2X+Cl2↑+H2↑。其中X的化学式为。(3)、我国在南海神狐海域连续试采可燃冰刷新记录,可燃冰可释放出甲烷气体,写出甲烷完全燃烧的化学方程式。24. 红磷燃烧除需要氧气外,还需满足的条件是;该反应的化学方程式;用红磷做“测定空气里氧气含量”的实验时,若红磷的量不足,所测得氧气的体积分数(填“偏大"、“偏小"或“不变”)。25. 风电制氢是一种绿色低碳的制氢方式,其过程如图所示。
 (1)、电解槽中与电源极相连的一端生成的是氢气。(2)、通过该实验能得出水是由组成的结论。(3)、加压过程的变化与电解槽中变化的本质区别是。26. 某化学探究小组为了验证镁、铜、锌、银的金属活动性顺序,设计了如下实验方案:①把镁加入到稀硫酸中;②将锌片加入到氯化镁溶液中;③将铜片加入到硝酸银溶液中;④将金属片X加入到Y中、(该方案中所有金属均已打磨,所使用的稀硫酸的浓度均相同)(1)、写出①中反应的化学方程式:。(2)、通过上述实验,可以判断铜的金属活动性比银强,依据的现象是 , 化学方程式为。(3)、要得出这四种金属的活动性顺序,如果④中Y表示硫酸铜溶液,则X表示的一种金属是 , 如果X表示铜,则Y表示的一种溶液是或。(写出溶质所属物质种类不同的两种溶液)
(1)、电解槽中与电源极相连的一端生成的是氢气。(2)、通过该实验能得出水是由组成的结论。(3)、加压过程的变化与电解槽中变化的本质区别是。26. 某化学探究小组为了验证镁、铜、锌、银的金属活动性顺序,设计了如下实验方案:①把镁加入到稀硫酸中;②将锌片加入到氯化镁溶液中;③将铜片加入到硝酸银溶液中;④将金属片X加入到Y中、(该方案中所有金属均已打磨,所使用的稀硫酸的浓度均相同)(1)、写出①中反应的化学方程式:。(2)、通过上述实验,可以判断铜的金属活动性比银强,依据的现象是 , 化学方程式为。(3)、要得出这四种金属的活动性顺序,如果④中Y表示硫酸铜溶液,则X表示的一种金属是 , 如果X表示铜,则Y表示的一种溶液是或。(写出溶质所属物质种类不同的两种溶液)三、实验探究题(共3题,总计20分)
-
27. 某研究性学习小组欲利用下列装置进行相关气体制取的实验。请你分析回答下列问题。
 (1)、仪器a、b的名称分别为a。b。(2)、利用上述B、C装置的组合可以制取的一种气体是 , 利用此种方法制取该气体的化学方程式为。(3)、实验室选用高锰酸钾来制取氧气,反应的化学方程式为 , 则应选用的发生装置是 , 若选用E装置收集氧气时发现水槽中的水变成了紫红色,可能的原因是;若选用C装置收集氧气,则验满的方法为。(4)、若要制取氢气,可以使用D或E装置收集,能用E装置收集的原因是;若选用F装置代替C装置收集氢气,气体应从(填"c"或"d")导管口通入。28. 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物。实验时在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验。
(1)、仪器a、b的名称分别为a。b。(2)、利用上述B、C装置的组合可以制取的一种气体是 , 利用此种方法制取该气体的化学方程式为。(3)、实验室选用高锰酸钾来制取氧气,反应的化学方程式为 , 则应选用的发生装置是 , 若选用E装置收集氧气时发现水槽中的水变成了紫红色,可能的原因是;若选用C装置收集氧气,则验满的方法为。(4)、若要制取氢气,可以使用D或E装置收集,能用E装置收集的原因是;若选用F装置代替C装置收集氢气,气体应从(填"c"或"d")导管口通入。28. 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物。实验时在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验。 (1)、B中反应的化学方程式是;此处出现的现象是。(2)、实验过程中,D处点燃的目的是。(3)、对该实验的分析正确的是(选填编号)。
(1)、B中反应的化学方程式是;此处出现的现象是。(2)、实验过程中,D处点燃的目的是。(3)、对该实验的分析正确的是(选填编号)。a.实验结束时应先熄灭B处酒精灯
b.C中增加的质量与B中固体减少的质量相等
c.反应结束后继续通入一氧化碳的目的是防止铜被氧化
(4)、甲同学认为A装置用于证明一氧化碳不能和石灰水反应,乙同学认为省略A可达到同样的目的,因为。29. 学校化学探究小组为研究影响石灰石与稀盐酸反应速率的因素,于是进行了以下探究:【提出问题】石灰石与稀盐酸反应的快慢受哪些因素的影响呢?
【猜想与假设】猜想:可能与温度有关;
猜想2:可能与石灰石形状有关。
(1)、【设计实验】小明设计的实验方案:实验时,小明同时将注射器内足量稀盐酸全部推出后,观察到下图1所示现象,于是他得出粉末状石灰石和稀盐酸反应产生二氧化碳较快的结论,写出石灰石与稀盐酸反应的化学方程式 , 班级同学通过讨论对小明设计的实验方案提出质疑,请你指出小明设计方案的不科学之处是。 (2)、小明按照图2所示实验装置进行实验,并比较收集60mL二氧化碳的时间。
(2)、小明按照图2所示实验装置进行实验,并比较收集60mL二氧化碳的时间。
实验编号
温度/℃
石灰石颗粒
大小、3g
稀盐酸浓度
/%
收集60mL二氧化碳的
时间/s
①
20
块状
10
84
②
20
粉状
10
43
③
40
块状
10
68
④
40
粉状
10
32
①C装置应该选择(填“Cl”或“C2”)。
②通过对比实验①②,得出的结论是;若比较温度对该反应的影响,可以通过实验(写实验编号)对比。
(3)、【拓展延伸】除了上述比较的方法外,还有比较快慢的方法是。
(4)、为探究二氧化碳的性质,小英同学设计了如图所示的装里(a、d为浸有紫色石蕊试液的湿润棉花,b、c为用紫色石蕊试液浸过的干燥棉花,垂直固定玻璃管的装置未画出)
①棉球b和c均不变红,这是因为:。
②棉球d比a先变红,说明:。
四、计算题(共5分)
-
30. 为测定某含杂质的镁带中镁的质量分数,某同学取3g该镁带样品于烧杯中,逐滴加入稀硫酸,当加入50g稀硫酸时,恰好完全反应,反应后得到的混合物总质量是52.8g(杂质不与稀硫酸反应)。求:(1)、生成氢气的质量是g。(2)、该镁带中镁的质量分数。