2023-2024学年沪教版初中化学九年级下册 6.3 物质的溶解性 同步分层训练培优题(第1课时)
试卷更新日期:2024-01-25 类型:同步测试
一、选择题
-
1. 下列关于溶液的说法正确的是( )A、均一、稳定的液体都是溶液 B、溶液组成中一定含有水 C、饱和溶液就是不能再溶解任何物质的溶液 D、汽油可以溶解在煤油中形成溶液2. 一杯10℃的硝酸钾溶液,能证明它是饱和溶液的方法是( )A、蒸发5g水有固体溶质析出 B、加入少许硝酸钾晶体不溶 C、把溶液降温至0℃有固体溶质析出 D、上述三种方法都行3. 在相同温度下,在盛有等质量饱和食盐水和不饱和食盐水的两只烧杯中,各放一个完全相同的乒乓球,则下列说法不正确的是( )A、两只烧杯中溶液的溶质质量分数不相同 B、两个乒乓球受到的浮力相同 C、两个乒乓球高出液面的部分不相同 D、两只烧杯中溶液的导电能力相同4. 某“天气瓶”通过樟脑在酒精溶液中的结晶情况反映气温变化。如图为该“天气瓶”在三种不同气温下的状况,则瓶内溶液一定为相应气温下樟脑饱和溶液的是( )
 A、甲、乙 B、甲、丙 C、乙、丙 D、甲、乙、丙5. 一定温度下,把1克熟石灰加入到100克水中,充分搅拌后仍有少许的熟石灰未溶解,静置后取上层清液,关于此清液的叙述正确的是( )
A、甲、乙 B、甲、丙 C、乙、丙 D、甲、乙、丙5. 一定温度下,把1克熟石灰加入到100克水中,充分搅拌后仍有少许的熟石灰未溶解,静置后取上层清液,关于此清液的叙述正确的是( )
A、它是不饱和溶液 B、它是浓溶液 C、它是该温度下的饱和溶液 D、它的溶质质量分数为1%6. 关于饱和溶液的有关叙述,一定正确的是( )A、有晶体析出的溶液 B、是浓溶液 C、混合物 D、不能再溶解该物质的溶液7. 能证明硝酸钾溶液在20℃时已经达到饱和状态的叙述是( )A、温度不变时,向该溶液中加入少量水,溶质的质量分数变小 B、温度不变时,向该溶液中加入少量KNO3晶体,晶体不在溶解 C、取少量该溶液,升温后无KNO3析出 D、取少量该溶液,降温到10℃时,有KNO3晶体析出8. 一定能使饱和溶液变为不饱和溶液的方法是( )A、升高溶液的温度 B、保持溶液温度不变,加入溶剂 C、降低溶液的温度 D、保持溶液温度不变,加入溶质9. 在一定的温度下,向不饱和的 NaNO3溶液中,逐渐加入 NaNO3晶体,下列图像中符合加入 NaNO3晶体的质量和溶液中的溶质质量变化规律的是( )A、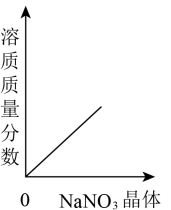 B、
B、 C、
C、 D、
D、 10. 下列图像能正确反映对应变化关系的是( )
10. 下列图像能正确反映对应变化关系的是( ) A、如图1所示,高温煅烧石灰石 B、如图2所示,向一定质量二氧化锰固体中加入一定质量过氧化氢溶液 C、如图3所示,一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 D、如图4所示,将足量的镁、铁两种金属分别与等质量、等溶质质量分数的稀硫酸充分反应11. 室温下,烧杯中装有溶液编号;向烧杯中加入固体,充分搅拌后,尚有固体未溶解,此时的溶液为编号;再向烧杯中加入水,固体全部溶解,此时的溶液为编号。下列说法正确的是( )A、溶液是的饱和溶液 B、溶液可能是的饱和溶液 C、溶液是的饱和溶液 D、溶液的溶质质量分数最大12. 在20℃时,向质量均为50g的5份水中分别加入一定质量的氯化钾固体,然后搅拌至完全溶解得到溶液(如有不溶解的氯化钾,则过滤除去)。加入氯化钾的质量与所得溶液的质量见下表。下列选项正确的是 ( )
A、如图1所示,高温煅烧石灰石 B、如图2所示,向一定质量二氧化锰固体中加入一定质量过氧化氢溶液 C、如图3所示,一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 D、如图4所示,将足量的镁、铁两种金属分别与等质量、等溶质质量分数的稀硫酸充分反应11. 室温下,烧杯中装有溶液编号;向烧杯中加入固体,充分搅拌后,尚有固体未溶解,此时的溶液为编号;再向烧杯中加入水,固体全部溶解,此时的溶液为编号。下列说法正确的是( )A、溶液是的饱和溶液 B、溶液可能是的饱和溶液 C、溶液是的饱和溶液 D、溶液的溶质质量分数最大12. 在20℃时,向质量均为50g的5份水中分别加入一定质量的氯化钾固体,然后搅拌至完全溶解得到溶液(如有不溶解的氯化钾,则过滤除去)。加入氯化钾的质量与所得溶液的质量见下表。下列选项正确的是 ( )实验编号
1
2
3
4
5
加入氯化钾的质量/g
5
10
15
20
25
溶液的质量/g
55
60
65
67
67
A、在20℃时,实验3所得的溶液为饱和溶液 B、在20℃时,所得溶液的溶质的质量分数:实验1<实验2<实验3<实验4<实验5 C、在20℃时,实验1所得的溶液为不饱和溶液,可以通过蒸发溶剂的方法使它变为饱和溶液 D、在20℃时,实验5所得的溶液中溶质的质量为25g13. 室温时,取一定质量的氯化钠固体放入烧杯中,如图所示,加水搅拌充分溶解,下列分析不正确的是( ) A、乙和丙烧杯中的氯化钠溶液一定是饱和溶液 B、丁烧杯中的氯化钠溶液一定是不饱和溶液 C、乙→丙的过程中,烧杯中溶质质量分数不变 D、丁→戊的过程中,烧杯中溶液质量增加14. 某温度下有一杯饱和的硝酸钾溶液,欲使其溶质的质量分数发生改变,下列操作可行的是( )A、加入一定质量的硝酸钾晶体 B、加入少量的水 C、降低温度 D、恒温蒸发溶剂15. 已知在20℃时,100g水中最多溶解31.6gKNO3、30℃时100g水中最多溶解45.8gKNO3 , 某同学按如图所示步骤进行实验,下列说法正确的是( )
A、乙和丙烧杯中的氯化钠溶液一定是饱和溶液 B、丁烧杯中的氯化钠溶液一定是不饱和溶液 C、乙→丙的过程中,烧杯中溶质质量分数不变 D、丁→戊的过程中,烧杯中溶液质量增加14. 某温度下有一杯饱和的硝酸钾溶液,欲使其溶质的质量分数发生改变,下列操作可行的是( )A、加入一定质量的硝酸钾晶体 B、加入少量的水 C、降低温度 D、恒温蒸发溶剂15. 已知在20℃时,100g水中最多溶解31.6gKNO3、30℃时100g水中最多溶解45.8gKNO3 , 某同学按如图所示步骤进行实验,下列说法正确的是( ) A、溶液中KNO3的质量分数:I<II<III B、II中溶液是30℃时KNO3的不饱和溶液 C、II中KNO3的质量分数是I中的2倍 D、III中KNO3溶液的质量是131.6g
A、溶液中KNO3的质量分数:I<II<III B、II中溶液是30℃时KNO3的不饱和溶液 C、II中KNO3的质量分数是I中的2倍 D、III中KNO3溶液的质量是131.6g二、综合题
-
16. 农业配制无士栽培营养液,一般先配制成浓缩贮备液后,再用大量水稀释后使用。项目学习小组欲在实验室配制100g溶质质量分数为16%的硝酸钾营养液。请回答下列问题。
 (1)、需要硝酸钾固体的质量为g,水的体积为mL(水的密度为1g/mL)。(2)、如图中还缺少的一种玻璃仪器是。(填名称)(3)、下列操作会导致所配的溶液溶质质量分数偏大的是____(填字母序号)。A、硝酸钾固体中含有不溶于水的杂质 B、烧杯内有水 C、量取水的体积时采用俯视的方法读数 D、把配制好的溶液倒入试剂瓶时有部分溅出(4)、在炎热的夏天从冰箱拿出一瓶硝酸钾浓缩贮备液,溶液状态如图甲,一段时间后溶液状态变成如图乙(不考虑水的蒸发)。下列说法正确的是____(填字母序号)。
(1)、需要硝酸钾固体的质量为g,水的体积为mL(水的密度为1g/mL)。(2)、如图中还缺少的一种玻璃仪器是。(填名称)(3)、下列操作会导致所配的溶液溶质质量分数偏大的是____(填字母序号)。A、硝酸钾固体中含有不溶于水的杂质 B、烧杯内有水 C、量取水的体积时采用俯视的方法读数 D、把配制好的溶液倒入试剂瓶时有部分溅出(4)、在炎热的夏天从冰箱拿出一瓶硝酸钾浓缩贮备液,溶液状态如图甲,一段时间后溶液状态变成如图乙(不考虑水的蒸发)。下列说法正确的是____(填字母序号)。 A、图甲溶液一定是硝酸钾的饱和溶液 B、图乙溶液一定是硝酸钾的不饱和溶液 C、溶液从甲状态变成乙状态,溶液质量不变 D、溶液从甲状态变成乙状态,溶质质量分数变大(5)、若要把配制好的100g溶质质量分数为16%的硝酸钾溶液稀释成4%的硝酸钾溶液,需要加入水的质量为多少克?(请写出计算过程)17. 20℃时,向 50g 水中加入 31.6g 硝酸钾(KNO3)固体并进行如下系列操作,请回答相关问题:
A、图甲溶液一定是硝酸钾的饱和溶液 B、图乙溶液一定是硝酸钾的不饱和溶液 C、溶液从甲状态变成乙状态,溶液质量不变 D、溶液从甲状态变成乙状态,溶质质量分数变大(5)、若要把配制好的100g溶质质量分数为16%的硝酸钾溶液稀释成4%的硝酸钾溶液,需要加入水的质量为多少克?(请写出计算过程)17. 20℃时,向 50g 水中加入 31.6g 硝酸钾(KNO3)固体并进行如下系列操作,请回答相关问题: (1)、图中烧杯A、C 中的溶液一定是饱和溶液,理由是。(2)、若烧杯 B 中的溶液恰好饱和,则烧杯 C 中剩余固体的质量20g(>,<,=)。(3)、操作 a 可采用的方法是。(答一条即可)(4)、向 B 中恰好饱和的硝酸钾溶液中加入少量高锰酸钾固体,充分搅拌后发现溶液变为紫红色,由此可以得出的结论有____。A、一定温度下硝酸钾的饱和溶液还能继续溶解其它物质 B、溶液不一定都是无色的 C、相同条件下,高锰酸钾的溶解能力比硝酸钾的溶解能力强 D、一种溶液中可以有多种溶质(5)、实验需要 30g10%的硝酸钾溶液,若用 15%的硝酸钾溶液加水稀释,则需要多少克蒸馏水?(写出具体计算过程)(6)、下列因素会造成上述所配溶液溶质质量分数偏小的是____(填字母序号)。A、量取蒸馏水时仰视读数 B、量取蒸馏水时俯视读数 C、将称量好的 NaCl 固体转移至烧杯时,NaCl 洒落 D、配好的溶液转移到试剂瓶时,部分溶液溅出
(1)、图中烧杯A、C 中的溶液一定是饱和溶液,理由是。(2)、若烧杯 B 中的溶液恰好饱和,则烧杯 C 中剩余固体的质量20g(>,<,=)。(3)、操作 a 可采用的方法是。(答一条即可)(4)、向 B 中恰好饱和的硝酸钾溶液中加入少量高锰酸钾固体,充分搅拌后发现溶液变为紫红色,由此可以得出的结论有____。A、一定温度下硝酸钾的饱和溶液还能继续溶解其它物质 B、溶液不一定都是无色的 C、相同条件下,高锰酸钾的溶解能力比硝酸钾的溶解能力强 D、一种溶液中可以有多种溶质(5)、实验需要 30g10%的硝酸钾溶液,若用 15%的硝酸钾溶液加水稀释,则需要多少克蒸馏水?(写出具体计算过程)(6)、下列因素会造成上述所配溶液溶质质量分数偏小的是____(填字母序号)。A、量取蒸馏水时仰视读数 B、量取蒸馏水时俯视读数 C、将称量好的 NaCl 固体转移至烧杯时,NaCl 洒落 D、配好的溶液转移到试剂瓶时,部分溶液溅出