2023-2024学年沪教版初中化学九年级下册 6.2 溶液组成的表示 同步分层训练培优题
试卷更新日期:2024-01-25 类型:同步测试
一、选择题
-
1. 规律总结是学习的重要手段,下列分析归纳中,不合理的是( )A、空气是重要的资源宝库,可利用分离液态空气法制得“工业氧气” B、为准确配置一定质量分数的硫酸铜溶液,可将硫酸铜晶体放入量筒,再精确加入一定量程的蒸馏水,振荡即可得到溶液 C、氧气常规收集方法中,收集纯度较高的氧气,一般采用排水集气法 D、一般情况下,氮气不能燃烧,也不支持燃烧,不易溶于水2. 下列有关“一定溶质质量分数的氯化钠溶液的配制”的实验操作中不规范的是( ).A、
 取氯化钠
B、
取氯化钠
B、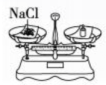 称量一定质量的氯化钠
C、
称量一定质量的氯化钠
C、 向烧杯中加入氯化钠粉末
D、
向烧杯中加入氯化钠粉末
D、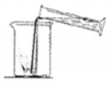 向烧杯中加水
3. 关于30 g溶质质量分数为10%的氯化钠溶液,说法错误的是( )A、从物质分类角度:氯化钠溶液属于混合物 B、从性质特点角度:取出15 g该溶液,溶质的质量分数为5% C、从微观角度:溶液中含有大量的钠离子、氯离子、水分子 D、从质量关系角度:氯化钠和水按1∶9的质量比配制成的溶液4. 医生常用生理盐水(溶质质量分数为0.9%)给患者输液。下列对生理盐水的理解不正确的是( )A、生理盐水中氯化钠是溶质,水是溶剂 B、生理盐水中氯化钠与水的质量比为9:1000 C、每输入100g生理盐水,进入患者体内的氯化钠质量为0.9g D、输液时,输液管中和输液瓶中生理盐水的溶质质量分数相同5. 下列溶液中溶剂不是水的是( )A、碘酒溶液 B、生理盐水 C、过氧化氢溶液 D、葡萄糖注射液6. 将100g 溶质质量分数为 10%NaNO3 溶液,将其溶质质量分数扩大一倍,下列做法正确的是( )A、加入10g NaNO3 固体 B、蒸发掉40g溶剂 C、加入20g NaNO3 固体 D、加入100g质量分数30%的NaNO3溶液7. 某醋酸(化学式为CH3COOH)溶液中,醋酸分子中所含的氢原子总数与水分子中所含的氢原子总数相等,则此醋酸溶液中溶质的质量分数是( )A、62.5% B、46% C、65% D、71.8%8. 硝酸钾可作为无土栽培的一种营养液。欲将质量分数为20%的硝酸钾溶液稀释成200 g质量分数为10%的硝酸钾溶液,需要加水( )A、10 g B、100 g C、200 g D、20 g9. 某同学要配制50g质量分数为14%的氯化钠溶液,下列关于配制该溶液的说法不正确的是( )
向烧杯中加水
3. 关于30 g溶质质量分数为10%的氯化钠溶液,说法错误的是( )A、从物质分类角度:氯化钠溶液属于混合物 B、从性质特点角度:取出15 g该溶液,溶质的质量分数为5% C、从微观角度:溶液中含有大量的钠离子、氯离子、水分子 D、从质量关系角度:氯化钠和水按1∶9的质量比配制成的溶液4. 医生常用生理盐水(溶质质量分数为0.9%)给患者输液。下列对生理盐水的理解不正确的是( )A、生理盐水中氯化钠是溶质,水是溶剂 B、生理盐水中氯化钠与水的质量比为9:1000 C、每输入100g生理盐水,进入患者体内的氯化钠质量为0.9g D、输液时,输液管中和输液瓶中生理盐水的溶质质量分数相同5. 下列溶液中溶剂不是水的是( )A、碘酒溶液 B、生理盐水 C、过氧化氢溶液 D、葡萄糖注射液6. 将100g 溶质质量分数为 10%NaNO3 溶液,将其溶质质量分数扩大一倍,下列做法正确的是( )A、加入10g NaNO3 固体 B、蒸发掉40g溶剂 C、加入20g NaNO3 固体 D、加入100g质量分数30%的NaNO3溶液7. 某醋酸(化学式为CH3COOH)溶液中,醋酸分子中所含的氢原子总数与水分子中所含的氢原子总数相等,则此醋酸溶液中溶质的质量分数是( )A、62.5% B、46% C、65% D、71.8%8. 硝酸钾可作为无土栽培的一种营养液。欲将质量分数为20%的硝酸钾溶液稀释成200 g质量分数为10%的硝酸钾溶液,需要加水( )A、10 g B、100 g C、200 g D、20 g9. 某同学要配制50g质量分数为14%的氯化钠溶液,下列关于配制该溶液的说法不正确的是( )①若用氯化钠固体配制,需称取氯化钠固体7.0g
②选用200mL量筒量取所需水的体积
③实验中用到的玻璃仪器有托盘天平、烧杯、量筒、玻璃棒和试剂瓶
④用量筒量取水时,俯视读数,配得溶液的溶质质量分数偏大(假设:其余步骤无误)
A、①③ B、②④ C、①② D、②③10. 实验室用氯化钠固体配制100g质量分数为8%的氯化钠溶液,下列说法中错误的是( )A、实验的步骤为计算、称量、量取、溶解 B、量取水时,用规格100mL的量筒 C、若用量筒量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8% D、溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解11. 向一定质量的硝酸钾溶液中,逐渐加水稀释,下列图象符合有关量变化规律的是( )A、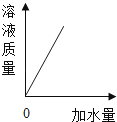 B、
B、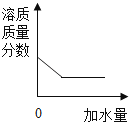 C、
C、 D、
D、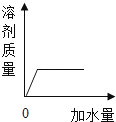 12. 如图,海水淡化可采用膜分离技术,对淡化膜右侧的海水加压,而海水中的各离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析( )
12. 如图,海水淡化可采用膜分离技术,对淡化膜右侧的海水加压,而海水中的各离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析( )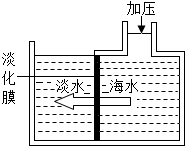 A、溶质质量增加 B、溶剂质量减少 C、溶液质量不变 D、溶质质量分数减少13. 在配制10%的氯化钠溶液的过程中,导致溶液中氯化钠质量分数小于10%的可能原因是()
A、溶质质量增加 B、溶剂质量减少 C、溶液质量不变 D、溶质质量分数减少13. 在配制10%的氯化钠溶液的过程中,导致溶液中氯化钠质量分数小于10%的可能原因是()①用量筒量取水时俯视读数
②配制溶液的烧杯用少量蒸馏水润洗
③在托盘天平的左盘称取氯化钠时,游码不在零位置就调节天平平衡,后将游码移动得到读数
④盛装溶液的试剂瓶用蒸馏水润洗
⑤氯化钠晶体不纯.
A、①②③④⑤ B、只有①②④⑤ C、只有①②③ D、只有②③④⑤14. 取的石灰石与稀盐酸恰好完全反应,反应后所得溶液的质量为 , 则该稀盐酸的溶质质量分数为( ).A、14.6% B、3.65% C、7.3% D、10%二、综合题
-
15. 分别填写下列溶液中溶质和溶剂的名称。(1)、蔗糖溶液:溶质;溶剂。(2)、碘酒(即碘的酒精溶液):溶质;溶剂。(3)、酒精:溶质;溶剂。(4)、0.9%的生理盐水:溶质;溶剂。16. 可乐是我们经常饮用的一种饮料,下图是一种瓶装可乐外观上的部分文字。请回答:
 (1)、该饮料里的溶剂是。(2)、常温下一瓶合格的可乐密封放置一段时间后,是否会出现浑浊现象?(填“是”或“否”),原因是。(3)、该饮料(填“是”或“不是”)混合物。17. 如图为医用葡萄糖氯化钠注射液,溶液中氯化钠的质量分数为。用量筒取用该溶液时仰视量筒刻度,取用的葡萄糖的量比所需的用量(填“偏小”,“偏大”或“无影响”)。
(1)、该饮料里的溶剂是。(2)、常温下一瓶合格的可乐密封放置一段时间后,是否会出现浑浊现象?(填“是”或“否”),原因是。(3)、该饮料(填“是”或“不是”)混合物。17. 如图为医用葡萄糖氯化钠注射液,溶液中氯化钠的质量分数为。用量筒取用该溶液时仰视量筒刻度,取用的葡萄糖的量比所需的用量(填“偏小”,“偏大”或“无影响”)。
三、实验探究题
-
18. 实验室欲配制1 000 g溶质质量分数为4%的氢氧化钠溶液。(1)、配制步骤:
①计算:列式计算所需氢氧化钠固体质量,水的体积(水的密度是
1 g/cm3)。
②称量:氢氧化钠固体盛放在中,放在托盘天平的左盘上;用量筒量取所需的水。
③溶解:将氢氧化钠固体溶于水,用搅拌,使氢氧化钠全部溶解,冷却至室温。
④装瓶:把配好的溶液装入试剂瓶,盖好瓶盖并贴上标签,放入试剂柜中。请在装有所配制溶液的试剂瓶(如图)标签上标明相应的信息:。
 (2)、在配制过程中,导致溶液中氢氧化钠质量分数小于4%的可能原因是____。
(2)、在配制过程中,导致溶液中氢氧化钠质量分数小于4%的可能原因是____。①用量筒量取水时俯视读数 ②配制溶液的烧杯用少量蒸馏水润洗 ③盛装溶液的试剂瓶用蒸馏水润洗 ④氢氧化钠固体不纯
A、①②③④ B、只有①②④ C、只有①②③ D、只有②③④(3)、若老师提供的药品有500 g 8%的氢氧化钠溶液,500 g 1%的氢氧化钠溶液,足量的氢氧化钠固体和水,你可以设计出哪些配制方案。方案
具体物质用量(无需书写实验步骤)
方案一
方案二
方案三
四、计算题
-
19. 将6克硝酸钾完全溶于54克水中,并将形成的溶液平均分成三份,计算:(1)、根据溶液的均一性,任取其中一份,其溶质的质量分数是。(2)、另取一份,使其溶质质量分数增大一倍,需加入硝酸钾克;再取一份,欲使其溶质质量分数减小一半,需加入溶质质量分数为1%的硝酸钾溶液克。(3)、现有溶质质量分数为10%的硝酸钾溶液200 g,若配制成溶质质量分数为2%的硝酸钾溶液,需要加水的质量是多少?(写出计算过程)20. 化学兴趣小组为测定某大理石样品中CaCO3的含量,进行如下实验:取18.0g样品置于烧杯中,向其中加入质量分数为5%的稀盐酸(样品中杂质不与盐酸反应),测得生成气体的质量与加入盐酸的质量关系如图所示,请回答下列问题。
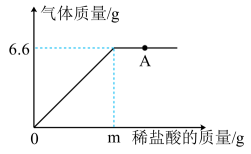 (1)、实验室现有质量分数为30%的盐酸50.0g,最多可配制质量分数为5%的盐酸g。(2)、图中“A”点的溶质是(填化学式)。(3)、计算该样品中CaCO3的质量分数。(写出计算过程,结果精确到0.1%)
(1)、实验室现有质量分数为30%的盐酸50.0g,最多可配制质量分数为5%的盐酸g。(2)、图中“A”点的溶质是(填化学式)。(3)、计算该样品中CaCO3的质量分数。(写出计算过程,结果精确到0.1%)
-