吉林省白山市浑江区2023-2024学年九年级上学期化学期末试题
试卷更新日期:2024-01-22 类型:期末考试
一、单项选择题(共10分)
-
1. 空气是一种宝贵的资源,下列生产生活中用到的气体不是来自空气的是()A、作为燃料电池燃料的H2 B、用于生产氮肥的N2 C、用于医疗急救的O2 D、用于飞艇的He2. 下列有关化学史的叙述,错误的是( )A、法国化学家拉瓦锡,第一次根据实验提出:空气是由氧气和氮气组成的 B、中国化学家张青莲,在1991年精确测定了铟(In)的相对原子质量 C、俄国科学家门捷列夫,将当时已发现的63种元素排序,制得了第一张元素周期 D、中国化学家侯德榜,在工业制烧碱的研究中,取得了巨大成就3. 下列能用于加热的仪器是( )A、
 B、
B、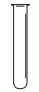 C、
C、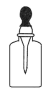 D、
D、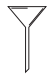 4. 生活中处处有化学,下列说法正确的是( )A、煤、石油是可再生能源 B、合理使用农药,减少农药对农产品和环境的污染 C、大气污染物主要包括悬浮颗粒物、和等 D、油罐起火,消防队员用高压水枪向油罐喷水,是为了降低石油的着火点5. 在中国传统文化中“笔、墨、纸、砚”被称为“文房四宝”,其中蕴含了丰富的化学知识。下列说法中错误的是( )A、鉴别毛笔笔头是羊毫(含蛋白质)还是合成纤维可用灼烧法 B、用墨写字、作画,常温下可保持长时间不褪色 C、造纸工艺中常使用草木灰水,这会使得纸张酸化 D、砚石有不同的颜色,当含有较多赤铁矿时,可显红棕色6. 蛋白质是构成细胞的基本物质,它是由多种氨基酸(如甘氨酸、丙氨酸等)构成的极为复杂的化合物,其中丙氨酸的化学式为 , 下列说法不正确的是( )A、丙氨酸中含有13个原子 B、丙氨酸属于有机物 C、丙氨酸中碳元素的质量分数最大 D、丙氨酸中氮元素和氧元素的质量比为7:167. 某同学在水电解器中加入含酚酞的稀溶液(溶液呈中性且不参与反应),至充满管A和管B。通直流电一段时间后现象如下图所示,电解结束后将容器内所有液体倒入烧杯中,溶液呈无色。下列说法不正确的是( )
4. 生活中处处有化学,下列说法正确的是( )A、煤、石油是可再生能源 B、合理使用农药,减少农药对农产品和环境的污染 C、大气污染物主要包括悬浮颗粒物、和等 D、油罐起火,消防队员用高压水枪向油罐喷水,是为了降低石油的着火点5. 在中国传统文化中“笔、墨、纸、砚”被称为“文房四宝”,其中蕴含了丰富的化学知识。下列说法中错误的是( )A、鉴别毛笔笔头是羊毫(含蛋白质)还是合成纤维可用灼烧法 B、用墨写字、作画,常温下可保持长时间不褪色 C、造纸工艺中常使用草木灰水,这会使得纸张酸化 D、砚石有不同的颜色,当含有较多赤铁矿时,可显红棕色6. 蛋白质是构成细胞的基本物质,它是由多种氨基酸(如甘氨酸、丙氨酸等)构成的极为复杂的化合物,其中丙氨酸的化学式为 , 下列说法不正确的是( )A、丙氨酸中含有13个原子 B、丙氨酸属于有机物 C、丙氨酸中碳元素的质量分数最大 D、丙氨酸中氮元素和氧元素的质量比为7:167. 某同学在水电解器中加入含酚酞的稀溶液(溶液呈中性且不参与反应),至充满管A和管B。通直流电一段时间后现象如下图所示,电解结束后将容器内所有液体倒入烧杯中,溶液呈无色。下列说法不正确的是( )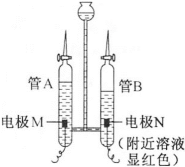 A、硫酸钠在水中解离出和 , 可增强导电性 B、电解过程中化学能转化为电能 C、电解过程中,电极M附近产生的微粒有和 D、管A中的气体与管B中的气体体积比1:28. 下列事实都能从微观角度进行解释,主要体现“分子间隔与物质状态有关”的是( )A、八月桂花飘香 B、变瘪的乒乓球放在热水中可恢复原形 C、物质热胀冷缩 D、相同质量的水和冰所占体积不同9. 下列说法正确的是( )A、现有NaOH、稀、NaCl、四种溶液,不用其他试剂就可以鉴別出来 B、区分NaOH溶液和溶液:取样,分别加入水中观察温度变化 C、制备氢氧化钠溶液:将碳酸钠溶液与过量的饱和石灰水混合,过滤 D、除去NaOH溶液中的:加入适量的稀盐酸至不再产生气泡10. 如图表示五种不同类别物质间的关系。图中“—”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质,A是铁锈主要成分,C俗称苛性钠。下列说法正确的是( )
A、硫酸钠在水中解离出和 , 可增强导电性 B、电解过程中化学能转化为电能 C、电解过程中,电极M附近产生的微粒有和 D、管A中的气体与管B中的气体体积比1:28. 下列事实都能从微观角度进行解释,主要体现“分子间隔与物质状态有关”的是( )A、八月桂花飘香 B、变瘪的乒乓球放在热水中可恢复原形 C、物质热胀冷缩 D、相同质量的水和冰所占体积不同9. 下列说法正确的是( )A、现有NaOH、稀、NaCl、四种溶液,不用其他试剂就可以鉴別出来 B、区分NaOH溶液和溶液:取样,分别加入水中观察温度变化 C、制备氢氧化钠溶液:将碳酸钠溶液与过量的饱和石灰水混合,过滤 D、除去NaOH溶液中的:加入适量的稀盐酸至不再产生气泡10. 如图表示五种不同类别物质间的关系。图中“—”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质,A是铁锈主要成分,C俗称苛性钠。下列说法正确的是( )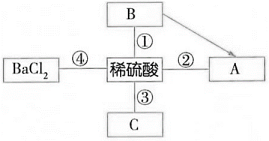 A、物质B可通过在纯氧中燃烧生成物质 B、除去二氧化碳中混有的水蒸气,可用固体C作干燥剂 C、反应②的化学方程式为: D、反应④可观察到有白色沉淀生成
A、物质B可通过在纯氧中燃烧生成物质 B、除去二氧化碳中混有的水蒸气,可用固体C作干燥剂 C、反应②的化学方程式为: D、反应④可观察到有白色沉淀生成二、填空题(每空1分,共10分)
-
11. 请用化学用语回答下列问题。(1)、磷原子;(2)、三个氧原子构成的分子;(3)、+5价氮的氧化物。12. 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任。
甲
 乙
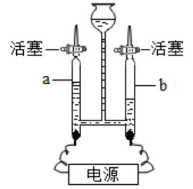
乙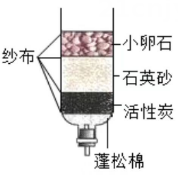 (1)、用如图甲装置进行电解水的实验,b中收集到的气体是;(2)、我国水资源丰富,但分布不均,有些村民地下水作为生活用水,人们常用检验地下水是硬水还是软水;某同学自制如图乙所示简易净水器,图中小卵石和石英砂所起的作用是。13. 华为公司作为我国高新科技的代表,其自主研制的“麒麟”芯片已达到世界领先水平,该芯片的主要材料为高纯度的单质硅。请回答以下与硅有关的问题。
(1)、用如图甲装置进行电解水的实验,b中收集到的气体是;(2)、我国水资源丰富,但分布不均,有些村民地下水作为生活用水,人们常用检验地下水是硬水还是软水;某同学自制如图乙所示简易净水器,图中小卵石和石英砂所起的作用是。13. 华为公司作为我国高新科技的代表,其自主研制的“麒麟”芯片已达到世界领先水平,该芯片的主要材料为高纯度的单质硅。请回答以下与硅有关的问题。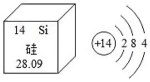 (1)、如图是硅元素在元素周期表中的相关信息及其原子结构示意图,硅元素在素元素周期表中第周期;(2)、工业制取高纯硅的部分反应原理的微观示意图如图,该反应的化学方程式为 , 反应后硅元素的化合价(选填“升高”“降低”或“不变”)。
(1)、如图是硅元素在元素周期表中的相关信息及其原子结构示意图,硅元素在素元素周期表中第周期;(2)、工业制取高纯硅的部分反应原理的微观示意图如图,该反应的化学方程式为 , 反应后硅元素的化合价(选填“升高”“降低”或“不变”)。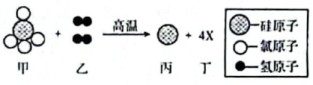
三、简答题(每空1分,化学方程式2分,共12分)
-
14. 铁是目前世界上使用最多的金属。(1)、生活中:把铁制成铁锅利用了铁的延展性和性;(2)、实验室:细铁丝在氧气中燃烧的主要现象是火星四射,产生黑色固体等,该反应的化学方程式是。(3)、工业上:用一氧化碳和赤铁矿反应炼铁,该反应利用了一氧化碳的性(填化学性质)。15. 如图是A、B、C三种固体物质在水中的溶解度曲线,回答下列问题。
 (1)、℃时,三种物质的溶解度由小到大的顺序是;(2)、在温度不变的条件下,将C的不饱和溶液变为饱和溶液的方法是(写一种即可)(3)、若A物质中含有少量的B物质,可通过的方法提纯A。16. 碳和部分碳的化合物问转化关系如图所示。
(1)、℃时,三种物质的溶解度由小到大的顺序是;(2)、在温度不变的条件下,将C的不饱和溶液变为饱和溶液的方法是(写一种即可)(3)、若A物质中含有少量的B物质,可通过的方法提纯A。16. 碳和部分碳的化合物问转化关系如图所示。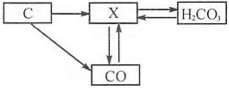 (1)、物质X的化学式为;(2)、从图中任选一种物质,写出它的一种用途。17. 海水中蕴藏着丰富的化学资源,工业上常利用海水提取粗盐(含 , 等杂质),然后进一步得到精制食盐,并广泛用于氯碱工业和侯氏制碱工业等。过程如图所示。
(1)、物质X的化学式为;(2)、从图中任选一种物质,写出它的一种用途。17. 海水中蕴藏着丰富的化学资源,工业上常利用海水提取粗盐(含 , 等杂质),然后进一步得到精制食盐,并广泛用于氯碱工业和侯氏制碱工业等。过程如图所示。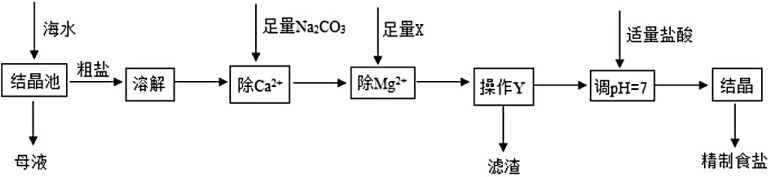 (1)、试剂X为____(填字母序号);A、NaOH B、KOH C、(2)、操作Y为;(3)、加适量盐酸的作用是为了除去。
(1)、试剂X为____(填字母序号);A、NaOH B、KOH C、(2)、操作Y为;(3)、加适量盐酸的作用是为了除去。四、实验与探究题(每空1分,化学方程式2分,共12分)
-
18. 如图是实验室制取和收集气体的常用装置。请回答下列问题。
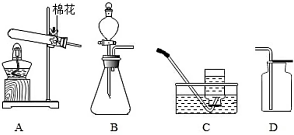 (1)、甲同学用石灰石和稀盐酸来制取和收集二氧化碳气体,他应选用的实验装置是;(2)、乙同学用加热高锰酸钾来制取氧气,试管口放一团棉花的原因是;实验过程中发现装置A的试管口有少量水滴。这些水不是生成物的理由是;(3)、丙同学在选用B装置探究“二氧化锰能加快过氧化氢分解制氧气”的实验时,老师要求他补充“在盛有少量二氧化锰的试管中加入适量水,并把带火星的木条伸入试管,观察现象。”的实验,增补该对照实验的目的是。19. 做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,意外看到有气泡产生。查验标签后确认药品没有拿错,在瓶口发现有白色粉末状物质。
(1)、甲同学用石灰石和稀盐酸来制取和收集二氧化碳气体,他应选用的实验装置是;(2)、乙同学用加热高锰酸钾来制取氧气,试管口放一团棉花的原因是;实验过程中发现装置A的试管口有少量水滴。这些水不是生成物的理由是;(3)、丙同学在选用B装置探究“二氧化锰能加快过氧化氢分解制氧气”的实验时,老师要求他补充“在盛有少量二氧化锰的试管中加入适量水,并把带火星的木条伸入试管,观察现象。”的实验,增补该对照实验的目的是。19. 做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,意外看到有气泡产生。查验标签后确认药品没有拿错,在瓶口发现有白色粉末状物质。【猜测】氢氧化钠溶液变质了。
(1)、分析原因:氢氧化钠溶液变质的原因(用化学方程式表示)。(2)、实验验证:分别滴入四种不同类别的试剂,设计实验再次确认该氢氧化钠溶液已变质。D中加入的是溶液(填化学式);四种方案中不合理的是(填试管编号“A~D”);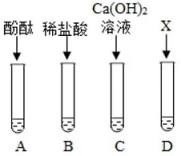
【结论】氢氧化钠溶液已经变质。
(3)、提出质疑:该氢氧化钠溶液是否完全变质?方案编号
实验步骤及现象
结论
方案一
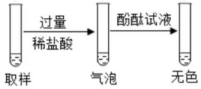
完全变质
方案二
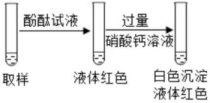
部分变质
方案三
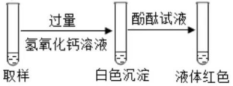
部分变质
经过讨论,一致认为只有方案二是正确的,方案一如果部分变质,过量的稀盐酸和氢氧化钠反应生成氯化钠和水,和碳酸钠反应生成氯化钠、水和二氧化碳,滴加酚酞试液时溶液都不变色,方案三中都能使酚酞变红;结论:氢氧化钠溶液部分变质。
(4)、如图,为得到纯净的氢氧化钠固体,加水溶解后加入(试剂),过滤蒸发;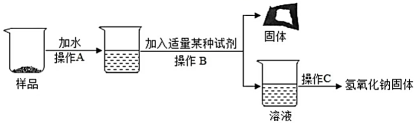 (5)、为了测定样品中氢氧化钠的纯度,小红同学设计如图装置(铁架台略去),已知饱和碳酸氢钠溶液不吸收二氧化碳。
(5)、为了测定样品中氢氧化钠的纯度,小红同学设计如图装置(铁架台略去),已知饱和碳酸氢钠溶液不吸收二氧化碳。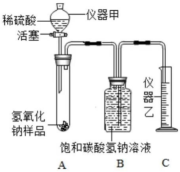
①取106g样品进行实验,根据实验数据,通过计算可知产生了4.4g,根据上述数据,请计算该样品中碳酸钠的质量分数是;
②利用该实验装置,若操作正确,装置气密性良好,立即读数,测定的氢氧化钠的纯度会偏小,理由是。
五、计算题(共6分)
-
20. 单晶硅是一种极为重要的半导体材料,实验室在高温高压下,用氢气置换四氯化硅()制取少量的硅。(1)、计算34g四氯化硅完全反应制得硅的质量。(2)、为防止污染空气,处理尾气的方法是。