2023-2024学年人教版初中化学九年级下册 9.2 溶解度 同步分层训练提升题
试卷更新日期:2024-01-21 类型:同步测试
一、选择题
-
1. 能证明某氯化钾溶液已经达到饱和状态的方法是( )。A、温度不变时,向该溶液中加入少量水 B、取出少量该溶液,降温,有氯化钾晶体析出. C、取出少量该溶液,升温,无氯化钾晶体析出 D、温度不变时,向该溶液中加入少量氯化钾晶体,晶体不再溶解2. 关于饱和溶液的有关叙述,一定正确的是( )A、有晶体析出的溶液 B、是浓溶液 C、混合物 D、不能再溶解该物质的溶液3. 制汽水时,为了使二氧化碳的溶解度增大,可采用的方法是( )A、降低压强 B、降低压强并升高温度 C、升高温度 D、增大压强并降低温度4. 下列措施不能使不饱和溶液转变为饱和溶液的是( )A、蒸发溶剂 B、增加溶质 C、改变温度 D、加速搅拌5. 下列有关溶液的说法,正确的是( )A、任何溶液的溶剂都是水 B、硝酸钾饱和溶液降温后析出晶体,说明硝酸钾的溶解度随温度的降低而减小 C、食用油加入水中能形成溶液 D、饱和溶液就是不能再溶解任何物质的溶液6. 已知20℃时CuSO4的溶解度为32g。20℃时,取一定质量某CuSO4溶液于烧杯中,按下图进行实验(整个过程中忽略溶剂损失),下列说法不正确的是( )
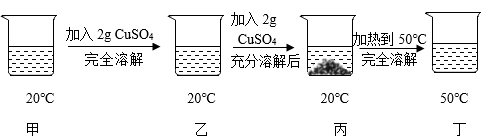 A、溶液中溶质质量分数的大小关系为丁>丙>甲 B、丙中溶液溶质与溶剂的质量比为8:25 C、丁溶液一定是饱和溶液 D、CuSO4 50℃时的溶解度比20℃时的大7. “20℃时氯化钠的溶解度是 36g”,根据这一条件及溶解度的含义,判断下列说法正确的是( )A、100g 水溶解 36g 氯化钠恰好能配成饱和溶液 B、20℃时,100g 氯化钠饱和溶液里含有 36g 氯化钠 C、20℃时,把 136g 氯化钠饱和溶液蒸干,可得到 36g 氯化钠 D、饱和氯化钠溶液中溶质、溶剂、溶液的质量比为 36:100:1368. 对图象的分析正确的是( )A、
A、溶液中溶质质量分数的大小关系为丁>丙>甲 B、丙中溶液溶质与溶剂的质量比为8:25 C、丁溶液一定是饱和溶液 D、CuSO4 50℃时的溶解度比20℃时的大7. “20℃时氯化钠的溶解度是 36g”,根据这一条件及溶解度的含义,判断下列说法正确的是( )A、100g 水溶解 36g 氯化钠恰好能配成饱和溶液 B、20℃时,100g 氯化钠饱和溶液里含有 36g 氯化钠 C、20℃时,把 136g 氯化钠饱和溶液蒸干,可得到 36g 氯化钠 D、饱和氯化钠溶液中溶质、溶剂、溶液的质量比为 36:100:1368. 对图象的分析正确的是( )A、 气体溶解度随温度、压强的变化关系,可知P2>P1
B、
气体溶解度随温度、压强的变化关系,可知P2>P1
B、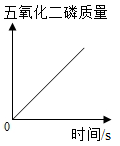 一定量的红磷在空气中燃烧
C、
一定量的红磷在空气中燃烧
C、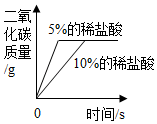 等质量的碳酸钠粉末分别与足量的不同浓度的稀盐酸反应
D、
等质量的碳酸钠粉末分别与足量的不同浓度的稀盐酸反应
D、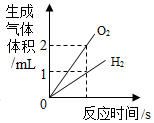 电解水生成的气体体积关系
9. 下列有关溶液的说法中正确的是( )A、蔗糖溶液的下层比上层甜 B、溶质都以分子形式溶解在溶剂里 C、温度不变,则某物质饱和溶液的浓度不变 D、溶质溶解时均无明显的温度变化10. 图1是甲、乙、丙三种固体物质的溶解度曲线,图2是30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后的溶解情况,下列说法正确的是( )
电解水生成的气体体积关系
9. 下列有关溶液的说法中正确的是( )A、蔗糖溶液的下层比上层甜 B、溶质都以分子形式溶解在溶剂里 C、温度不变,则某物质饱和溶液的浓度不变 D、溶质溶解时均无明显的温度变化10. 图1是甲、乙、丙三种固体物质的溶解度曲线,图2是30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后的溶解情况,下列说法正确的是( )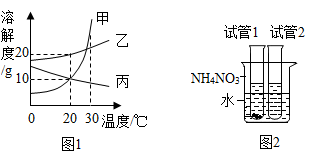 A、甲物质的溶解度比乙物质的溶解度大 B、加入试管1的固体是丙 C、向烧杯中加入NH4NO3固体后,试管2中一定有晶体析出 D、将30℃时甲、乙、丙三种物质的饱和溶液各100g降温至20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙11. 已知KNO3的落解度随温度的升高而增大,下列是某KNO3饱和溶液的浓度随温度升高而变化的图像(不考虑溶剂的质量变化),其中正确的是( )。A、
A、甲物质的溶解度比乙物质的溶解度大 B、加入试管1的固体是丙 C、向烧杯中加入NH4NO3固体后,试管2中一定有晶体析出 D、将30℃时甲、乙、丙三种物质的饱和溶液各100g降温至20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙11. 已知KNO3的落解度随温度的升高而增大,下列是某KNO3饱和溶液的浓度随温度升高而变化的图像(不考虑溶剂的质量变化),其中正确的是( )。A、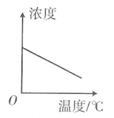 B、
B、 C、
C、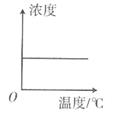 D、
D、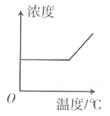 12. 20℃时,将18.6g硝酸钠放人50g水中,充分搅拌后全部溶解,则20℃时硝酸钠的溶解度为( )。A、37.2g B、18.6g C、9.3g D、无法计算
12. 20℃时,将18.6g硝酸钠放人50g水中,充分搅拌后全部溶解,则20℃时硝酸钠的溶解度为( )。A、37.2g B、18.6g C、9.3g D、无法计算二、填空题
-
13. 根据图中甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
 (1)、P点的含义:。(2)、t2℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是。(3)、在t2℃时、向盛有15g甲物质的烧杯中加入50g水,充分溶解后,所得溶液为(选填“饱和”或“不饱和”)溶液,所得溶液的质量为g。(4)、若甲物质中混有少量乙物质,最好采用(选填“降温结晶”或“蒸发结晶”)的方法提纯甲。(5)、t1℃时,将甲、乙、丙三种物质的饱和溶液同时升温至t2℃,所得溶液中溶质质量分数由大到小的顺序为。14. 烧开水时,加热不久在锅底会出现许多气泡,这说明气体的溶解度随 而减小,打开汽水瓶盖时,有大量气泡由瓶口逸出,这是因为。由此可以得出,增大CO2气体在水中的溶解度应采用的方法是 , 因此食品工业上在常温下制汽水、啤酒时常采取 的方法增大CO2的溶解度。
(1)、P点的含义:。(2)、t2℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是。(3)、在t2℃时、向盛有15g甲物质的烧杯中加入50g水,充分溶解后,所得溶液为(选填“饱和”或“不饱和”)溶液,所得溶液的质量为g。(4)、若甲物质中混有少量乙物质,最好采用(选填“降温结晶”或“蒸发结晶”)的方法提纯甲。(5)、t1℃时,将甲、乙、丙三种物质的饱和溶液同时升温至t2℃,所得溶液中溶质质量分数由大到小的顺序为。14. 烧开水时,加热不久在锅底会出现许多气泡,这说明气体的溶解度随 而减小,打开汽水瓶盖时,有大量气泡由瓶口逸出,这是因为。由此可以得出,增大CO2气体在水中的溶解度应采用的方法是 , 因此食品工业上在常温下制汽水、啤酒时常采取 的方法增大CO2的溶解度。三、综合题
-
15. 根据下列溶解度曲线图回答:
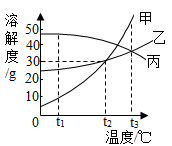 (1)、t2℃时,甲、乙的溶解度曲线交点的含义是 , 在t2℃时,将20g甲物质放入50g水中,形成的溶液的质量是g;(2)、甲中含有少量的乙,若提纯甲可采用法;(3)、要想把一瓶接近饱和的丙溶液变成饱和溶液,具体措施有:①加入丙物质、②升高温度、③降低温度、④加入水、⑤蒸发水后再恢复到原温度其中措施正确的是。(4)、将甲、乙、丙三种物质t1℃时的饱和溶液升温到t3℃,所得溶液中溶质的质量分数最大的是。16. 根据下表数据,回答问题。
(1)、t2℃时,甲、乙的溶解度曲线交点的含义是 , 在t2℃时,将20g甲物质放入50g水中,形成的溶液的质量是g;(2)、甲中含有少量的乙,若提纯甲可采用法;(3)、要想把一瓶接近饱和的丙溶液变成饱和溶液,具体措施有:①加入丙物质、②升高温度、③降低温度、④加入水、⑤蒸发水后再恢复到原温度其中措施正确的是。(4)、将甲、乙、丙三种物质t1℃时的饱和溶液升温到t3℃,所得溶液中溶质的质量分数最大的是。16. 根据下表数据,回答问题。温度/℃
0
20
40
60
80
100
溶解度/g
KNO3
13.3
31.6
63.9
110
169
246
NaCl
35.7
36.0
36.6
37.3
38.4
39.8
(1)、20℃时,KNO3的溶解度是g;(2)、60℃时,200g KNO3溶液中含溶质100g,将该溶液降温至20℃,可析出KNO3g;(3)、NaCl溶液中含有少量KNO3 , 提纯NaCl,采用的方法是 (选填“蒸发结晶”或“降温结晶”)。四、实验探究题
-
17. 小明对硝酸钾在水中的溶解情况进行实验探究,他在烧杯中倒入20mL蒸馏水(如图所示)。继续实验:
 (1)、请你完成他的实验报告
(1)、请你完成他的实验报告操作
现象
结论
①加入5g硝酸钾,搅拌
固体全部溶解
20℃时5g硝酸钾能溶解在20mL水中
②再加入5g硝酸钾,搅拌
固体部分溶解
③加热至80℃
固体全部溶解
80℃时10g硝酸钾能溶解在20mL水中
④冷却至20℃
(2)、①、②中都要搅拌,目的是。四个实验中一定得到饱和溶液的是(填序号),实验探究了影响硝酸钾的溶解性的因素是。(3)、已知鸡蛋的平均密度是1.1 , 20℃时水的密度是1.0 , 假设硝酸钾溶于水的过程中可以忽略溶液体积的变化,20℃时可以配置一种硝酸钾溶液,使鸡蛋在溶液中漂浮吗?用原始数据的计算式说明。五、计算题
-
18. 如图是甲、乙两种固体物质的溶解度曲线图,请回答下列问题:
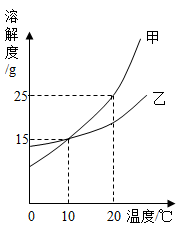 (1)、20℃时,将15g的甲物质充分溶解在50g水中,所形成溶液的溶质质量分数是。(2)、10℃时,欲将150g乙物质的饱和溶液的溶质质量分数减小一半,需要加水g。(3)、某同学欲将20℃时300g20%的甲溶液的溶质质量分数增大一倍。他采用恒温蒸发水的方法,并进行了如下计算:
(1)、20℃时,将15g的甲物质充分溶解在50g水中,所形成溶液的溶质质量分数是。(2)、10℃时,欲将150g乙物质的饱和溶液的溶质质量分数减小一半,需要加水g。(3)、某同学欲将20℃时300g20%的甲溶液的溶质质量分数增大一倍。他采用恒温蒸发水的方法,并进行了如下计算:解:设蒸发水的质量为x,
300g×20%=(300g-x)×40%
解得:x=150g
试分析:他能否达到目的,并说明理由。
-