2023-2024学年人教版初中化学九年级下册 10.2 酸和碱的中和反应 同步分层训练提升题
试卷更新日期:2024-01-20 类型:同步测试
一、选择题
-
1. 下列实验操作中,正确的是( )A、
 稀释浓硫酸
B、
稀释浓硫酸
B、 倾倒稀盐酸
C、
倾倒稀盐酸
C、 给液体加热
D、
给液体加热
D、 测定溶液的酸碱度
2. 用pH试纸测定下列水果汁的pH值如下,其中酸性最强的是( )A、橙汁:4 B、苹果汁:3 C、柠檬汁:2 D、西瓜汁:53. 空气是一种宝贵的自然资源。下列有关空气的说法正确的是( )A、空气污染指数越高,空气质量越好 B、酸雨的产生与空气中的二氧化碳有关 C、二氧化硫、二氧化氮和一氧化碳都是空气污染物 D、空气中氮气的质量分数约为4. 向水中加入下列物质,pH值不会发生变化的是( )A、生石灰 B、食醋 C、氯化钠 D、碳酸钠5. 推理是学习化学的重要方法之一。下列推理正确的是( )A、向某固体物质中加入稀盐酸,生成无色无味气体,证明该物质一定是碳酸盐 B、酸溶液的pH<7,所以pH<7的溶液一定是酸溶液 C、酸碱中和反应生成盐和水,所以有盐和水生成的反应均为中和反应 D、向碳酸钠溶液中滴加无色酚酞试剂,溶液变成红色,说明碳酸钠溶液呈碱性6. 向某稀盐酸中逐渐加入试剂X后溶液的pH变化如图。试剂x可能是下列物质中的( )
测定溶液的酸碱度
2. 用pH试纸测定下列水果汁的pH值如下,其中酸性最强的是( )A、橙汁:4 B、苹果汁:3 C、柠檬汁:2 D、西瓜汁:53. 空气是一种宝贵的自然资源。下列有关空气的说法正确的是( )A、空气污染指数越高,空气质量越好 B、酸雨的产生与空气中的二氧化碳有关 C、二氧化硫、二氧化氮和一氧化碳都是空气污染物 D、空气中氮气的质量分数约为4. 向水中加入下列物质,pH值不会发生变化的是( )A、生石灰 B、食醋 C、氯化钠 D、碳酸钠5. 推理是学习化学的重要方法之一。下列推理正确的是( )A、向某固体物质中加入稀盐酸,生成无色无味气体,证明该物质一定是碳酸盐 B、酸溶液的pH<7,所以pH<7的溶液一定是酸溶液 C、酸碱中和反应生成盐和水,所以有盐和水生成的反应均为中和反应 D、向碳酸钠溶液中滴加无色酚酞试剂,溶液变成红色,说明碳酸钠溶液呈碱性6. 向某稀盐酸中逐渐加入试剂X后溶液的pH变化如图。试剂x可能是下列物质中的( ) A、H2O B、H2SO4 C、NaOH D、CaCO37. 空气是一种宝贵的资源,下列说法错误的是( )A、氧气具有可燃性 B、氧气的化学性质比较活泼 C、稀有气体通电发出各种不同颜色的光是物理变化 D、酸雨的形成与空气中的污染物二氧化硫、二氧化氮有关8. pH能定量描述溶液酸碱性的强弱。下面对pH的认识中正确的是( )A、pH表示的是溶液中所含酸或碱的质量分数 B、pH大小与一定量溶液中所含H+或OH﹣的数量多少有关 C、不同种类的酸,它们的溶液pH大小一定不同 D、溶液的碱性越强,pH越小9. 下列实际应用中,利用中和反应原理的是( )
A、H2O B、H2SO4 C、NaOH D、CaCO37. 空气是一种宝贵的资源,下列说法错误的是( )A、氧气具有可燃性 B、氧气的化学性质比较活泼 C、稀有气体通电发出各种不同颜色的光是物理变化 D、酸雨的形成与空气中的污染物二氧化硫、二氧化氮有关8. pH能定量描述溶液酸碱性的强弱。下面对pH的认识中正确的是( )A、pH表示的是溶液中所含酸或碱的质量分数 B、pH大小与一定量溶液中所含H+或OH﹣的数量多少有关 C、不同种类的酸,它们的溶液pH大小一定不同 D、溶液的碱性越强,pH越小9. 下列实际应用中,利用中和反应原理的是( )①用氢氧化钠溶液洗涤石油中残余的硫酸②用含氢氧化铝的药物治疗胃酸过多
③用熟石灰改良酸性土壤
④将稀氨水(含有、OH-)涂抹在蚊虫叮咬处(分泌出蚁酸)能止痒
A、①②③④ B、仅①②③ C、仅②③④ D、仅①③④10. 类比推理在化学学习和科学研究中有重要意义,下列类比推理正确的是( )A、氢氧化钠可以中和盐酸,因此用氢氧化钠治疗胃酸过多 B、中和反应生成盐和水,因此有盐和水生成的反应一定是中和反应. C、酸能使紫色石蕊溶液变红,因此使石蕊溶液变红的就一定是酸性溶液 D、溶液具有均一性、稳定性,因此具有均一、稳定性的液体一定是溶液11. 将pH=2的盐酸不断加水稀释,下列图中能正确描述该过程中溶液pH变化的图象是( )A、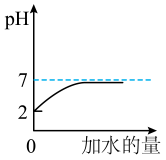 B、
B、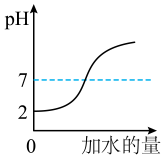 C、
C、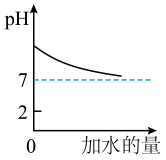 D、
D、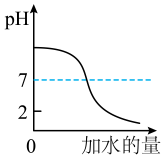 12. 某实验探究小组用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程,实验操作和测定结果如图所示。下列叙述中正确的是( )
12. 某实验探究小组用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程,实验操作和测定结果如图所示。下列叙述中正确的是( )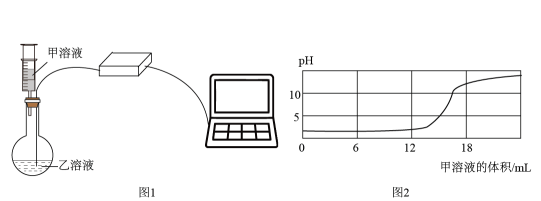
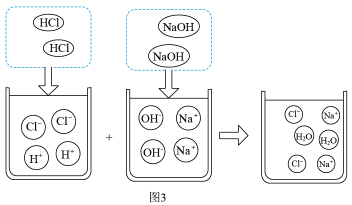 A、图1使用注射器加入甲溶液,主要是为了精确地计量液体体积 B、依据图2给定结果,圆底烧瓶内加入的乙溶液为NaOH溶液 C、结合图3分析,加入甲溶液6mL时,烧瓶中的溶液只有Na+、Cl- D、加入甲溶液12mL后,将所得溶液蒸干,得到固体只含NaCl
A、图1使用注射器加入甲溶液,主要是为了精确地计量液体体积 B、依据图2给定结果,圆底烧瓶内加入的乙溶液为NaOH溶液 C、结合图3分析,加入甲溶液6mL时,烧瓶中的溶液只有Na+、Cl- D、加入甲溶液12mL后,将所得溶液蒸干,得到固体只含NaCl二、填空题
-
13. 如图是某酸碱中和反应的微观示意图。
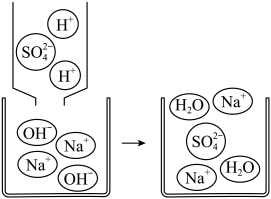 (1)、写出该反应的化学方程式。(2)、为了验证反应的发生,先向碱溶液中滴入几滴无色酚酞溶液,然后再逐渐加入酸溶液至过量,请描述该过程中可观察到的现象。14. 请从A~C中任选2个作答。
(1)、写出该反应的化学方程式。(2)、为了验证反应的发生,先向碱溶液中滴入几滴无色酚酞溶液,然后再逐渐加入酸溶液至过量,请描述该过程中可观察到的现象。14. 请从A~C中任选2个作答。装置及药品
现象
解释或结论

A、①
②铁丝
铁丝表面产生红色固体,溶液颜色变浅
Fe的金属活动性比Cu的强
B、①稀盐酸
②氧化铁
固体减少,得到黄色溶液
化学方程式:
C、①稀硫酸
②滴有酚酞的NaOH溶液
NaOH能与硫酸反应
三、综合题
-
15. 我省全面夯实新型综合能源大省地位,推进地方美食与文化旅游高质量融合发展,实现了转型跨越。请依据图文信息,解答21~24题的相关问题。
 (1)、传统的燃煤发电会排放二氧化硫等污染物导致的产生,目前山西全省用电负荷的四分之一来自风力发电和光伏发电,光伏发电是将转化为电能。(2)、山西沁水建成了全国最大的煤层气田。煤层气俗称“瓦斯”,主要成分是甲烷,属于(填“可再生”或“不可再生”)能源,其燃烧的化学方程式为。(3)、流行于山西曲沃一带的“冷香豆腐脑”以浓郁、适口著称,其制作工序繁杂,包含“磨浆”、“隔渣”等流程。“磨浆”是将泡过水的黄豆磨成豆浆,该过程发生了(填“物理”或“化学”)变化;“隔渣”是将豆渣和豆浆进行分离,这一操作相当于化学实验操作中的 , 实验室进行该操作时用到的主要玻璃仪器有烧杯、漏斗和。(4)、山西汾河源头位于宁武县东寨镇管涔山脚下,“汾源灵沼”终年山泉流淌不绝,成为来山西旅游的“打卡地”之一。欲检验该山泉水是硬水还是软水可用 , 保护汾河,人人都是行动者,请写出一条汾河流域生态保护措施。16. 如图所示,图1为稀盐酸和氢氧化钠溶液反应的实验操作,图2为反应过程中烧杯内溶液pH的变化曲线。请回答下列问题:
(1)、传统的燃煤发电会排放二氧化硫等污染物导致的产生,目前山西全省用电负荷的四分之一来自风力发电和光伏发电,光伏发电是将转化为电能。(2)、山西沁水建成了全国最大的煤层气田。煤层气俗称“瓦斯”,主要成分是甲烷,属于(填“可再生”或“不可再生”)能源,其燃烧的化学方程式为。(3)、流行于山西曲沃一带的“冷香豆腐脑”以浓郁、适口著称,其制作工序繁杂,包含“磨浆”、“隔渣”等流程。“磨浆”是将泡过水的黄豆磨成豆浆,该过程发生了(填“物理”或“化学”)变化;“隔渣”是将豆渣和豆浆进行分离,这一操作相当于化学实验操作中的 , 实验室进行该操作时用到的主要玻璃仪器有烧杯、漏斗和。(4)、山西汾河源头位于宁武县东寨镇管涔山脚下,“汾源灵沼”终年山泉流淌不绝,成为来山西旅游的“打卡地”之一。欲检验该山泉水是硬水还是软水可用 , 保护汾河,人人都是行动者,请写出一条汾河流域生态保护措施。16. 如图所示,图1为稀盐酸和氢氧化钠溶液反应的实验操作,图2为反应过程中烧杯内溶液pH的变化曲线。请回答下列问题: (1)、胶头滴管里面的试剂名称是。(2)、a点对应溶液中的溶质是。(3)、c点对应溶液中的NaCl的质量与(填“a”或“b”)点对应溶液中的NaCl的质量相等。
(1)、胶头滴管里面的试剂名称是。(2)、a点对应溶液中的溶质是。(3)、c点对应溶液中的NaCl的质量与(填“a”或“b”)点对应溶液中的NaCl的质量相等。四、实验探究题
-
17. 探究氢氧化钠与稀硫酸是否发生反应。(1)、甲同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,发现管壁发烫,得出酸碱中和反应是放热反应的结论,乙同学认为推理不合理,理由是。(2)、乙同学将实验加以改进:将稀硫酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出氢氧化钠溶液温度随加入稀硫酸质量的变化,如图所示:

①由图可知,稀硫酸与氢氧化钠溶液发生的反应是(填“放热”或“吸热”)反应,B点表示的含义是。
②从A到B的过程中,烧杯中溶液pH逐渐(填“变大”“变小”或“不变”)。
③从B到C的过程中,烧杯内溶液中的阳离子有(填离子符号)。
(3)、向滴有酚酞试液的氢氧化钠溶液中滴加稀硫酸至恰好完全反应,证明反应发生的实验现象为
至恰好完全反应时,烧杯中离子数目的变化情况是(不考虑酚酞),反应的微观实质是。(4)、氨水(NH3·H2O)也能使酚酞变色,原因是氨水和氢氧化钠溶液中均含有一种相同离子:(填离子符号)。(5)、丁同学认为氢氧化钠溶液与稀硫酸混合没有明显现象,于是他想借助下列物质来验证反应是否发生,你觉得可行的是____。A、pH试纸 B、BaCl2 C、FeCl3 D、KNO3五、计算题
-
18. 计算题:化学小组参与“铅蓄废电池中硫酸回收”的研学项目,回收时需要测定电池废液中硫酸的质量分数。向装有50g废液的锥形瓶中加入质量分数为10%的氢氧化钠溶液,并充分搅拌,利用pH计等电子设备采集信息并绘制成下图,请据图回答相关问题。(杂可溶但不参加反应)
 (1)、称量g NaOH固体,溶解,配制40g10%的NaOH溶液。(2)、如图乙,a点溶液中含有的溶质是。(3)、请计算废液中的质量分数。
(1)、称量g NaOH固体,溶解,配制40g10%的NaOH溶液。(2)、如图乙,a点溶液中含有的溶质是。(3)、请计算废液中的质量分数。
-