辽宁省实验顶级名校2023-2024学年高三上学期期中考试化学试卷
试卷更新日期:2024-01-19 类型:期中考试
一、选择题(包含15小题,每小题3分,共45分,每题只有一个选项符合题意)
-
1. 唐代著名诗人白居易曾写过著名诗句:“绿蚁新醅酒,红泥小火炉”、“酥暖薤白酒,乳和地黄粥”。下列关于诗句中所提及物质的说法正确的是( )A、酿酒原料高粱、谷物等主要成分为纤维素 B、红泥的颜色主要来自氧化铁 C、乳和粥的分散质是蛋白质 D、纯酒精比乙醇溶液杀菌效果更佳2. 下列有关物质的性质和用途说法不正确的是( )A、利用高纯单质硅的半导体性能,可以制成光电池 B、石灰石在高温下的分解产物可与SO2反应,可用于减少燃煤烟气中的SO2 C、Na2O2与CO2反应放出氧气,可用于制作呼吸面具 D、二氧化硅导电能力强,可用于制造光导纤维3. 下列实验中的颜色变化与氧化还原反应无关的是( )
选项
A
B
C
D
实验
溶液滴入溶液中
通入溶液中
溶液滴入浊液中
石蕊溶液滴入氯水中
现象
产生白色沉淀,最终变为红褐色
产生淡黄色沉淀
沉淀由白色逐渐变为黄色
溶液变红,随后迅速褪色
A、A B、B C、C D、D4. 在标准状况下,将NO2、NO、O2混合气体充满一圆底烧瓶,倒置水中,进行喷泉实验,最后无气体剩余,若所得产物不扩散,则所得溶液的物质的量浓度的数值大小范围为( )A、 B、 C、 D、5. SO2是引发酸雨的主要污染物,将工业废气中的吸收能有效减少对大气的污染、并实现资源化利用。下列离子方程式正确的是( )已知常温下亚硫酸的电离平衡常数碳酸的电离平衡常数
A、硫酸型酸雨露置于空气中一段时间后溶液酸性增强: B、用过量溶液吸收废气中的 C、用过量氨水吸收废气中的 D、用过量溶液吸收废气中的6. 某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液,下列物质组合不符合要求的是( )
气体
液体
固体粉末
A
CO2
饱和Na2CO3溶液
CaCO3
B
Cl2
FeCl2溶液
Fe
C
HCl
Cu(NO3)2溶液
Cu
D
NH3
H2O
Al(OH)3
A、A B、B C、C D、D7. NA为阿伏加德罗常数的值,下列说法正确的是( )A、12 g 金刚石中含有的C-C键数目为4NA B、标准状况下,11.2LNO与11.2LO2混合后的分子数目为0.75NA C、23gNa与78gNa2O2分别与足量水反应生成的气体体积相同 D、100g质量分数为46%的乙醇溶液中含有氢原子数为12NA8. 实验室进行含硫化合物性质探究的装置(夹持装置省略)如图所示,分液漏斗①中盛有浓硫酸,将其逐滴加入到试管②的固体中。下列说法正确的是( )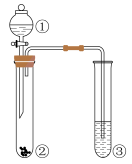 A、若②中为固体,③中盛石蕊溶液,则③中溶液先变红后褪色 B、若②中为蔗糖,③中盛有溴水,能说明浓硫酸具有脱水性和氧化性 C、若②中为固体,③中盛有氯化钡溶液,则③中生成白色沉淀 D、若②中为铜单质,③中盛有硫化氢水溶液,则③中生成黄色沉淀9. 由一种金属阳离子(包括NH)与两种酸根阴离子组成的盐称为混盐,如Ca(NO3)Cl可看成CaCl2和Ca(NO3)2。向混盐Na4S2O3中加入足量稀硫酸,发生如下反应:2Na4S2O3+4H2SO4=4Na2SO4+3S↓+SO2↑+4H2O。下列说法正确的是( )A、Na4S2O3溶液与AlCl3溶液混合可生成Al2S3沉淀 B、向混盐CaOCl2中加入足量稀硫酸会有Cl2产生 C、该反应每产生3molS,转移电子的物质的量为6mol D、1molNa4S2O3固体中含离子的物质的量为5mol10. 常温下取金属钠、铝、铁各1克,加入1mol/L的硫酸V升,要使铝、铁反应后放出等量的氢气,且比钠反应生成的氢气少,V的大小范围是( )A、V≥ B、V≤ C、V< D、V≤11. 某NaAlO2、Na2CO3的混合溶液中逐滴加入 1mol·L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。(已知:H2CO3的电离平衡常数K1=4.3×10-7 , K2=5.6×10-11;Al(OH)3的酸式电离平衡常数K=6.3×10-13)则下列说法正确的是( )
A、若②中为固体,③中盛石蕊溶液,则③中溶液先变红后褪色 B、若②中为蔗糖,③中盛有溴水,能说明浓硫酸具有脱水性和氧化性 C、若②中为固体,③中盛有氯化钡溶液,则③中生成白色沉淀 D、若②中为铜单质,③中盛有硫化氢水溶液,则③中生成黄色沉淀9. 由一种金属阳离子(包括NH)与两种酸根阴离子组成的盐称为混盐,如Ca(NO3)Cl可看成CaCl2和Ca(NO3)2。向混盐Na4S2O3中加入足量稀硫酸,发生如下反应:2Na4S2O3+4H2SO4=4Na2SO4+3S↓+SO2↑+4H2O。下列说法正确的是( )A、Na4S2O3溶液与AlCl3溶液混合可生成Al2S3沉淀 B、向混盐CaOCl2中加入足量稀硫酸会有Cl2产生 C、该反应每产生3molS,转移电子的物质的量为6mol D、1molNa4S2O3固体中含离子的物质的量为5mol10. 常温下取金属钠、铝、铁各1克,加入1mol/L的硫酸V升,要使铝、铁反应后放出等量的氢气,且比钠反应生成的氢气少,V的大小范围是( )A、V≥ B、V≤ C、V< D、V≤11. 某NaAlO2、Na2CO3的混合溶液中逐滴加入 1mol·L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。(已知:H2CO3的电离平衡常数K1=4.3×10-7 , K2=5.6×10-11;Al(OH)3的酸式电离平衡常数K=6.3×10-13)则下列说法正确的是( )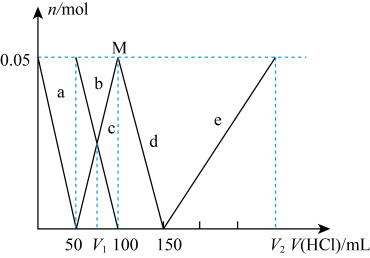 A、V1:V2=1:4 B、M点时生成的CO2为0.05mol C、原混合溶液中的CO32-与AlO2-的物质的量之比为1:3 D、a曲线表示的离子方程式为:AlO2-+4H+=Al3++2H2O12. 如图所示,实验室中利用洁净的铜片(0.3 mol)和浓硫酸进行反应,实验中无气体生成,Y型管左侧得到Cu2S和白色固体a,倾斜Y型管使左侧的物质全部转移到右侧稀硝酸中,反应生成固体单质b、a的溶液和NO。下列说法错误的是( )
A、V1:V2=1:4 B、M点时生成的CO2为0.05mol C、原混合溶液中的CO32-与AlO2-的物质的量之比为1:3 D、a曲线表示的离子方程式为:AlO2-+4H+=Al3++2H2O12. 如图所示,实验室中利用洁净的铜片(0.3 mol)和浓硫酸进行反应,实验中无气体生成,Y型管左侧得到Cu2S和白色固体a,倾斜Y型管使左侧的物质全部转移到右侧稀硝酸中,反应生成固体单质b、a的溶液和NO。下列说法错误的是( )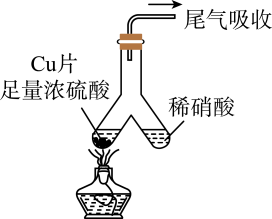 A、白色固体为CuSO4 B、NO为还原产物,b为氧化产物 C、NO与b的物质的量之和可能为0.2 mol D、参加反应的浓硫酸中,表现氧化性的占25%13. 2.48 g铁铜合金完全溶解于80 mL 4.0 mol·L-1稀硝酸中,得到标准状况下672 mL NO气体(假设此时无其他气体产生),下列说法正确的是( )A、取反应后溶液,滴入几滴KSCN溶液,无血红色出现 B、该合金中铁与铜的物质的量之比是1∶2 C、反应后溶液(忽略溶液体积变化)中c(H+)=2.5 mol·L-1 D、向反应后的溶液中加入2.0 mol·L-1NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120 mL14. 某溶液可能含有Al3+、NH、Fe2+、Na+、CO、SO、Cl-、NO中的若干种,若在该溶液中逐滴加入稀盐酸至过量,无明显现象,并得到X溶液,对溶液进行如图实验,下列结论正确的是(忽略水的电离,且原溶液中各离子浓度均为0.5mol/L)( )
A、白色固体为CuSO4 B、NO为还原产物,b为氧化产物 C、NO与b的物质的量之和可能为0.2 mol D、参加反应的浓硫酸中,表现氧化性的占25%13. 2.48 g铁铜合金完全溶解于80 mL 4.0 mol·L-1稀硝酸中,得到标准状况下672 mL NO气体(假设此时无其他气体产生),下列说法正确的是( )A、取反应后溶液,滴入几滴KSCN溶液,无血红色出现 B、该合金中铁与铜的物质的量之比是1∶2 C、反应后溶液(忽略溶液体积变化)中c(H+)=2.5 mol·L-1 D、向反应后的溶液中加入2.0 mol·L-1NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120 mL14. 某溶液可能含有Al3+、NH、Fe2+、Na+、CO、SO、Cl-、NO中的若干种,若在该溶液中逐滴加入稀盐酸至过量,无明显现象,并得到X溶液,对溶液进行如图实验,下列结论正确的是(忽略水的电离,且原溶液中各离子浓度均为0.5mol/L)( )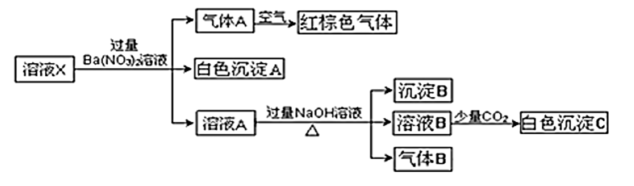 A、原溶液中一定存在NH、Fe2+、SO B、原溶液中可能含有NO和Al3+ C、白色沉淀C可能是Al(OH)3 D、沉淀B可能是Fe(OH)2和Fe(OH)3的混合物15. 将由三种固体组成的混合物溶于足量的水中,用玻璃棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是( )
A、原溶液中一定存在NH、Fe2+、SO B、原溶液中可能含有NO和Al3+ C、白色沉淀C可能是Al(OH)3 D、沉淀B可能是Fe(OH)2和Fe(OH)3的混合物15. 将由三种固体组成的混合物溶于足量的水中,用玻璃棒搅拌,充分溶解,一段时间后,向稳定的混合物溶液中滴加的稀硫酸,加入稀硫酸的体积与生成沉淀的物质的量关系如图所示。下列有关判断不正确的是( )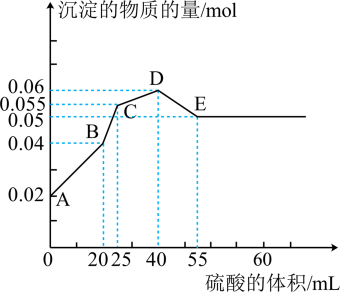 A、AB段发生反应的离子方程式为: B、D点表示的溶液呈酸性 C、混合物中FeSO4和AlCl3的物质的量相等 D、BC段发生反应的离子方程式为:
A、AB段发生反应的离子方程式为: B、D点表示的溶液呈酸性 C、混合物中FeSO4和AlCl3的物质的量相等 D、BC段发生反应的离子方程式为:二、II卷(非选择题,共55分)
-
16. 完成下列填空。(1)、已知A、B、C、D为气体,其中A、B为单质,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
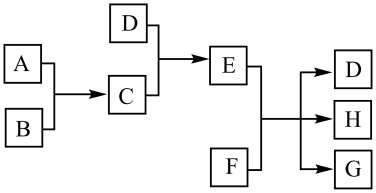
请回答下列问题:
①C的化学式是 , D的电子式为。
②如何检验E溶液中阳离子?。
(2)、在高压下,NO在下分解生成两种化合物,体系中各组分的物质的量随时间变化曲线如图甲所示。NO分解的化学方程式为。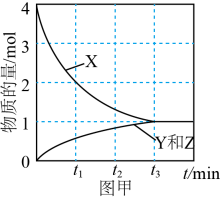 (3)、有色金属提取工艺中会产生大量含氰(CN·)废水,对环境造成了极大的负担。在碱性条件下可用ClO-将其氧化成和写出反应的离子方程式:。(4)、向酸性废水中加入NaClO,消除污染。写出相应的离子方程式为。(5)、将软锰矿与硫铁矿粉碎混合,用硫酸浸取。研究发现,酸浸时,和颗粒构成两个原电池反应,其原理如图所示(部分产物未标出)。
(3)、有色金属提取工艺中会产生大量含氰(CN·)废水,对环境造成了极大的负担。在碱性条件下可用ClO-将其氧化成和写出反应的离子方程式:。(4)、向酸性废水中加入NaClO,消除污染。写出相应的离子方程式为。(5)、将软锰矿与硫铁矿粉碎混合,用硫酸浸取。研究发现,酸浸时,和颗粒构成两个原电池反应,其原理如图所示(部分产物未标出)。
若原电池中生成单质S,其反应的离子方程式为。
17. 硫酸镍是一种重要的化工原料,无机工业常用其生产硫酸镍铵、氧化镍、碳酸镍等。粗硫酸镍晶体中含有Cu2+、Fe2+、Fe3+、Ca2+等杂质离子,现欲进一步提纯硫酸镍晶体,设计如下流程: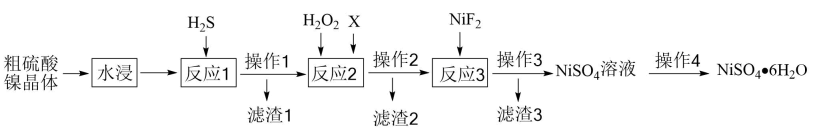
已知:室温下,
(1)、Ni在周期表中的位置为。(2)、通入气体发生反应的离子方程式为、。(3)、加入的主要目的是。(4)、试剂X可以是NiO或等,目的是。(5)、反应3加入的目的是。(6)、由溶液得到的操作为。18. 叠氮化钠(NaN₃)是一种防腐剂和分析试剂,在有机合成和汽车行业也有重要应用。学习小组对叠氮化钠的制备和产品纯度测定进行相关探究。查阅资料:
I.氨基钠熔点为易潮解和氧化;有强氧化性,不与酸、碱反应;易溶于水,叠氮酸(HN₃)不稳定,易分解爆炸;+2价锡具有较强的还原性。
II.
回答下列问题:
(1)、制备
①按气流方向,上述装置合理的连接顺序为(填仪器接口字母)。
②D的作用为。
③C处充分反应后,停止加热,为防止倒吸,需继续进行的操作为;E中溶液的作用是。
(2)、用如图所示装置测定产品纯度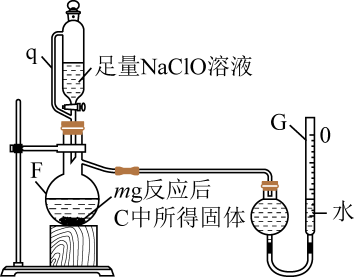
①仪器F中发生反应的离子方程式为。
②管q
 作用为。
作用为。③若G的初始读数为末读数为V₂mL,本实验条件下气体摩尔体积为Vmol·L-1 , 则产品中的质量分数为。
19.(1)、Ⅰ.次氯酸钠溶液和二氯异氰尿酸钠都是常用的杀菌消毒剂。NaClO可用于制备二氯异氰尿酸钠。
NaClO溶液可由低温下将Cl₂缓慢通入NaOH溶液中而制得。制备NaClO的离子反应方程式为;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是。(2)、有研究显示,南极臭氧空洞中的污染物硝酸氯与次氯酸钠在结构上有类似之处。下列推测有一项不合理 , 该选项是____。A、具有强氧化性 B、与NaOH溶液反应可生成两种钠盐 C、与盐酸作用能产生氯气 D、水解生成盐酸和硝酸(3)、Ⅱ.二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为:;
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗溶液20.00mL。
如何判断滴定达到了终点?。
(4)、通过计算判断该样品是否为优质品。(写出计算过程)该样品的有效氯=(5)、若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值(填“偏高”或“偏低”)。