江苏省连云港名校2023-2024学年高一上学期期中考试化学试卷
试卷更新日期:2024-01-17 类型:期中考试
一、单项选择题(本题包括20题,每题3分,共60分。每题只有一个选项符合题意。)
-
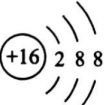
1. 我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。下列措施对实现“碳中和”不具有直接贡献的是( )A、推行生活垃圾分类 B、发展捕集技术 C、采取节能低碳生活方式 D、创新转化为碳燃料的技术2. 我国古代伟大发明黑火药的爆炸反应方程式为:。下列说法不正确的是( )A、属于强电解质 B、属于酸性氧化物 C、中子数为8的碳原子可表示为 D、的结构示意图是:
 3. 朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”月光穿过薄雾形成种种美景的本质原因是( )A、发生了丁达尔效应 B、空气中的小水滴颗粒的运动 C、雾是一种胶体,胶粒带有电荷 D、空气中的小水滴颗粒直径为1~100nm4. 下列化学用语表示正确的是( )A、次氯酸钙的化学式:CaCl2 B、H、D、T的关系:同位素 C、HCl的摩尔质量:36.5 D、质子数为6、中子数为7的碳原子5. 苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+ , 在空气中易转变为Fe3+。若榨汁时加入维生素C,可有效防止这种现象的发生。这说明维生素C具有( )A、还原性 B、氧化性 C、碱性 D、酸性6. 对于反应: , 下列说法不正确的是( )A、是氧化剂 B、发生氧化反应 C、每有反应将生成 D、每有电子转移将生成7. 下列有关物质的性质与用途具有对应关系的是( )A、Cl2能溶于水,可用于与H2反应制HCl B、NaHCO3受热易分解,可用制备抗酸药物 C、Al2O3能与酸反应,可用于制备耐高温材料 D、铁粉能与O2反应,可用作食品保存的脱氧剂8. 下列既能导电又属于电解质的物质是( )A、铜 B、石灰水 C、熔融NaCl D、CO29. 用NA表示阿伏加德罗常数的值,下列说法正确的是( )A、0.5mol·L-1的MgCl2溶液中离子总数为1.5NA B、标准状况下,22.4L水所含分子数为NA C、65gZn与足量H2SO4完全反应生成的H2所含原子数目为2NA D、足量的Na在11.2L氯气中完全燃烧,转移电子数为0.5NA10. 下列体系中氯离子浓度最大的是( )A、标准状况下22.4L 氯气 B、2mL 0.3mo/L HCl溶液 C、10mL 0.2mol/LCaCl2溶液 D、1mL 0.5mol/L KClO3溶液11. 以NaCl为原料,可制取纯碱。Na2CO3可用侯氏制碱法制取,主要涉及如下反应:; , 下列有关实验室模拟侯氏制碱法的实验原理和装置正确的是( )
3. 朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”月光穿过薄雾形成种种美景的本质原因是( )A、发生了丁达尔效应 B、空气中的小水滴颗粒的运动 C、雾是一种胶体,胶粒带有电荷 D、空气中的小水滴颗粒直径为1~100nm4. 下列化学用语表示正确的是( )A、次氯酸钙的化学式:CaCl2 B、H、D、T的关系:同位素 C、HCl的摩尔质量:36.5 D、质子数为6、中子数为7的碳原子5. 苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+ , 在空气中易转变为Fe3+。若榨汁时加入维生素C,可有效防止这种现象的发生。这说明维生素C具有( )A、还原性 B、氧化性 C、碱性 D、酸性6. 对于反应: , 下列说法不正确的是( )A、是氧化剂 B、发生氧化反应 C、每有反应将生成 D、每有电子转移将生成7. 下列有关物质的性质与用途具有对应关系的是( )A、Cl2能溶于水,可用于与H2反应制HCl B、NaHCO3受热易分解,可用制备抗酸药物 C、Al2O3能与酸反应,可用于制备耐高温材料 D、铁粉能与O2反应,可用作食品保存的脱氧剂8. 下列既能导电又属于电解质的物质是( )A、铜 B、石灰水 C、熔融NaCl D、CO29. 用NA表示阿伏加德罗常数的值,下列说法正确的是( )A、0.5mol·L-1的MgCl2溶液中离子总数为1.5NA B、标准状况下,22.4L水所含分子数为NA C、65gZn与足量H2SO4完全反应生成的H2所含原子数目为2NA D、足量的Na在11.2L氯气中完全燃烧,转移电子数为0.5NA10. 下列体系中氯离子浓度最大的是( )A、标准状况下22.4L 氯气 B、2mL 0.3mo/L HCl溶液 C、10mL 0.2mol/LCaCl2溶液 D、1mL 0.5mol/L KClO3溶液11. 以NaCl为原料,可制取纯碱。Na2CO3可用侯氏制碱法制取,主要涉及如下反应:; , 下列有关实验室模拟侯氏制碱法的实验原理和装置正确的是( )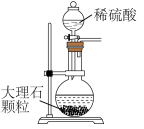
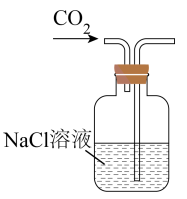


A.制取CO2
B.制取NaHCO3
C.分离NaHCO3
D.制取Na2CO3
A、A B、B C、C D、D12. 已知溶液中可与恰好完全反应,反应后全部转化为 , 则可能转化为( )A、 B、 C、 D、13. 下列有关实验操作的叙述合理的是( )A、用酒精灯加热烧瓶、蒸发皿时,都需要垫上石棉网 B、用酒精为萃取剂萃取碘水中的碘单质 C、蒸馏自来水实验中发现忘加沸石,冷却后再加入沸石 D、蒸发操作时,将溶液放入坩埚中加热到出现大量晶体后停止加热14. 配制一定物质的量浓度的Na2CO3溶液的操作过程如图,下列说法中错误的是( ) A、“操作1”中烧杯洗涤液也要转移到容量瓶中 B、“操作2”中玻璃棒起引流作用 C、所配制的Na2CO3溶液中c(Na+ )为2mol/L D、“操作4”定容时俯视刻度线会造成所配溶液浓度偏低15. 现有下列三种气体:a. 32 g CH4 , b.约含有6.02×1023个HCl分子的氯化氢气体,c.标准状况下33.6 L NH3。下列排列顺序一定正确的是( )A、质量:a>b>c B、氢原子数目:a>c>b C、分子数:b>a>c D、体积:c>a>b16. 下列说法不正确的是( )A、道尔顿认为物质是由原子构成,原子是不能被创造,在化学反应中不可再分 B、卢瑟福提出了带核的原子结构模型 C、汤姆生发现了原子中电子的存在 D、20世纪初,科学家揭示了微观世界波粒二象性的规律,认识到原子核外电子的运动遵循经典力学的原理。17. 下列有关氯及其化合物说法中不正确的是( )A、新制氯水可使蓝色石蕊试纸先变红后褪色 B、ClO2有强氧化性,可用于自来水消毒 C、实验室可用浓盐酸洗去试管壁上黏附的少量MnO2 D、氯水久置后,漂白性和酸性均减弱18. 根据下列实验操作及现象,得出的实验结论正确的是( )
A、“操作1”中烧杯洗涤液也要转移到容量瓶中 B、“操作2”中玻璃棒起引流作用 C、所配制的Na2CO3溶液中c(Na+ )为2mol/L D、“操作4”定容时俯视刻度线会造成所配溶液浓度偏低15. 现有下列三种气体:a. 32 g CH4 , b.约含有6.02×1023个HCl分子的氯化氢气体,c.标准状况下33.6 L NH3。下列排列顺序一定正确的是( )A、质量:a>b>c B、氢原子数目:a>c>b C、分子数:b>a>c D、体积:c>a>b16. 下列说法不正确的是( )A、道尔顿认为物质是由原子构成,原子是不能被创造,在化学反应中不可再分 B、卢瑟福提出了带核的原子结构模型 C、汤姆生发现了原子中电子的存在 D、20世纪初,科学家揭示了微观世界波粒二象性的规律,认识到原子核外电子的运动遵循经典力学的原理。17. 下列有关氯及其化合物说法中不正确的是( )A、新制氯水可使蓝色石蕊试纸先变红后褪色 B、ClO2有强氧化性,可用于自来水消毒 C、实验室可用浓盐酸洗去试管壁上黏附的少量MnO2 D、氯水久置后,漂白性和酸性均减弱18. 根据下列实验操作及现象,得出的实验结论正确的是( )选项
实验操作及现象
实验结论
A
取样品试剂,滴加溶液,生成白色沉淀,再加稀沉淀不溶解
一定有存在
B
取样品试剂,滴加溶液,生成白色沉淀,再加稀盐酸后沉淀不溶解
一定有存在
C
取样品试剂,滴加澄清石灰水,生成白色沉淀
一定有
D
取样品试剂,滴加稀盐酸,生成的气体能使澄清石灰水变浑浊
一定有存在
A、A B、B C、C D、D19. 实验室利用如图所示装置制备氯气,图中涉及气体发生、除杂、干燥、收集、尾气处理装置,其中共有几处错误( )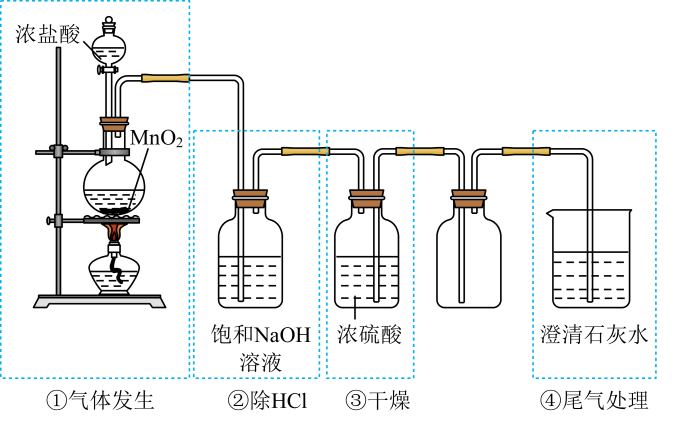 A、1处 B、2处 C、3处 D、4处20. 青蒿素是无色针状晶体,易溶于有机溶剂,几乎不溶于水,熔点为156~157℃,热稳定性差;乙醚的沸点为35℃.屠呦呦提取青蒿素的流程可简化如下:
A、1处 B、2处 C、3处 D、4处20. 青蒿素是无色针状晶体,易溶于有机溶剂,几乎不溶于水,熔点为156~157℃,热稳定性差;乙醚的沸点为35℃.屠呦呦提取青蒿素的流程可简化如下: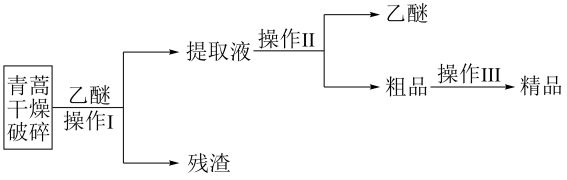
下列说法错误的是( )
A、破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素浸取率 B、操作Ⅰ需要用到的玻璃仪器有漏斗、玻璃棒、烧杯 C、操作II利用了乙醚与青蒿素的沸点相差较大 D、操作III的主要过程是加水溶解、蒸发浓缩、冷却结晶、过滤二、非选择题(共40分)
-
21. 填空。(1)、和的分子数之比为 , 原子数之比。(2)、某氯化物 , 含有 , M的摩尔质量为。(3)、同温同压下,同体积的气体和气体质量之比为。(4)、从溶液中取出 , 则溶液中物质的量为 , 的物质的量浓度是。22. 实验室欲配制的溶液500mL,有以下仪器:①烧杯②100mL量筒③1000mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)⑦药匙。(1)、配制时,必须使用的仪器有(填代号),还缺少的玻璃仪器是 , 该实验中两次用到玻璃棒,其作用分别是、。(2)、配制时,一般可分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却,其正确的操作顺序是。23. 消毒是疫情防控的重要措施。含氯消毒剂是高效、安全的杀菌消毒剂。(1)、84消毒液是一种家庭常用消毒剂,其主要成分具有性。(2)、新制氯水也可杀菌消毒,氯水中、、微粒摩尔分数随溶液pH变化关系如图所示。

①描述溶液中浓度随增大的变化情况:。
②氧化性强于 , 由图可知为6时消毒效果比7.5时。(填强、弱)
③亚氯酸钠是一种消毒能力更强的杀菌剂,消毒效果更持久。将气体通入、混合溶液,得同时放出 , 方程式为。
24. 某学习小组探究潮湿的与反应的产物,进行如下实验: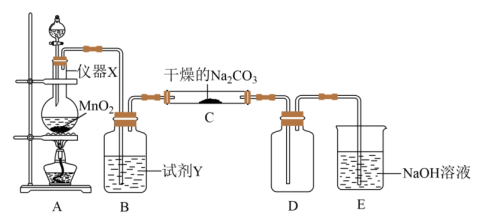
请回答:
(1)、试剂Y是。(2)、请写出装置A中的化学方程式。(3)、装置C中潮湿的与以等物质的量反应,生成、气体和另一种盐,试写出该反应化学方程式。(4)、若将上述装置中的C、D、E部分换成下图所述装置,其中Ⅰ与Ⅲ是干燥的有色布条,E中盛装溶液,请回答下列问题:
①装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅱ的作用是。
②E中化学方程式。