湖南省郴州市桂东县2023-2024学年九年级上学期12月联考化学试题
试卷更新日期:2024-01-15 类型:月考试卷
一、选择题(每小题有一个正确答案。每小题3分,本题共45分)
-
1. 下列变化属于化学变化的是( )A、高炉炼铁 B、胆矾的研碎 C、干冰升华 D、酒精的挥发2. 某磁性纳米材料X的一种制备方法为:FeCl2+2FeCl3+8NaOH=X+8NaCl+4H2O,该磁性纳米材料的化学式是( )A、Fe(OH)2 B、Fe(OH)3 C、Fe2O3 D、Fe3O43. 可用于验证铜,铁,锌三种金属的金属活动性强弱的一组药品是( )A、Cu、Zn、FeSO4溶液 B、Cu、FeSO4溶液、ZnSO4溶液 C、Cu、Fe、ZnSO4溶液 D、Zn、FeSO4溶液、CuSO4溶液4. 下列实验操作正确的是( )A、
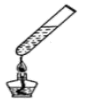 加热液体
B、
加热液体
B、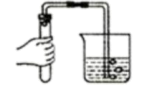 检查装置的气密性
C、
检查装置的气密性
C、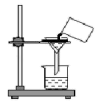 分离固液混合物
D、
分离固液混合物
D、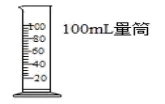 量取9.5mL液体
5. 下列化学反应属于置换反应的是()A、2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ B、CaCO3+CO2+H2O=Ca(HCO3)2 C、2NaNO3 2NaNO2+O2↑ D、CuO+H2 Cu+H2O6. 蔗糖(C12H22O11)是一种常用的食品甜味剂。下列关于蔗糖的说法正确的是()A、蔗糖是由碳、氢、氧三种元素组成 B、蔗糖中含有45个原子 C、蔗糖中氢元素的质量分数最高 D、蔗糖的相对分子质量为342g7. 生活中的下列现象,用分子的相关知识加以解释,其中不正确的是( )A、室内插花,满室飘香,说明分子不断地运动 B、热胀冷缩,说明分子大小随温度而改变 C、10mL酒精和10mL水混合后,体积小于20mL,说明分子之间有间隔 D、湿衣服放在火炉旁,干得较快,说明分子运动速率随温度升高而增大8. 按图所示装置,持续通入气态物质X,可以看到玻璃管中有红色物质生成,无水CuSO4变蓝,澄清石灰水变浑浊,则X不可能是( )
量取9.5mL液体
5. 下列化学反应属于置换反应的是()A、2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ B、CaCO3+CO2+H2O=Ca(HCO3)2 C、2NaNO3 2NaNO2+O2↑ D、CuO+H2 Cu+H2O6. 蔗糖(C12H22O11)是一种常用的食品甜味剂。下列关于蔗糖的说法正确的是()A、蔗糖是由碳、氢、氧三种元素组成 B、蔗糖中含有45个原子 C、蔗糖中氢元素的质量分数最高 D、蔗糖的相对分子质量为342g7. 生活中的下列现象,用分子的相关知识加以解释,其中不正确的是( )A、室内插花,满室飘香,说明分子不断地运动 B、热胀冷缩,说明分子大小随温度而改变 C、10mL酒精和10mL水混合后,体积小于20mL,说明分子之间有间隔 D、湿衣服放在火炉旁,干得较快,说明分子运动速率随温度升高而增大8. 按图所示装置,持续通入气态物质X,可以看到玻璃管中有红色物质生成,无水CuSO4变蓝,澄清石灰水变浑浊,则X不可能是( )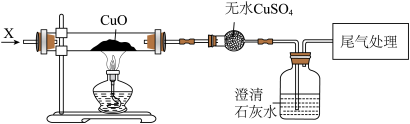 A、氢气和水蒸气 B、氢气和二氧化碳 C、一氧化碳和氢气 D、一氧化碳和水蒸气9. 下列各组物质,按混合物、化合物、单质顺序排列的是( )A、冰水混合物、干冰、氢气 B、石油、煤、天然气 C、氯化钠、甲烷、水银 D、洁净的空气、硫酸铜、液氧10. 下列有关化学实验与实验目的相符的是( )A、用带火星的木条伸入集气瓶中,可以证明氧气是否集满 B、电解H2O生成H2和O2 , 可以说明H2O是由H2和O2组成的 C、在煤炉上放一壶水,可以防止一氧化碳中毒 D、水墨画能长期保存是因为常温下碳的化学性质不活泼11. 在一个密闭容器中放入X、Y、Z、M四种物质,使之在一定条件下发生化学反应。一段时间后,测得有关数据如下表:
A、氢气和水蒸气 B、氢气和二氧化碳 C、一氧化碳和氢气 D、一氧化碳和水蒸气9. 下列各组物质,按混合物、化合物、单质顺序排列的是( )A、冰水混合物、干冰、氢气 B、石油、煤、天然气 C、氯化钠、甲烷、水银 D、洁净的空气、硫酸铜、液氧10. 下列有关化学实验与实验目的相符的是( )A、用带火星的木条伸入集气瓶中,可以证明氧气是否集满 B、电解H2O生成H2和O2 , 可以说明H2O是由H2和O2组成的 C、在煤炉上放一壶水,可以防止一氧化碳中毒 D、水墨画能长期保存是因为常温下碳的化学性质不活泼11. 在一个密闭容器中放入X、Y、Z、M四种物质,使之在一定条件下发生化学反应。一段时间后,测得有关数据如下表:物质
X
Y
Z
M
反应前的质量/g
20
5
3
28
反应后的质量/g
待测值
30
3
8
关于此反应的认识不正确的是( )
A、物质Z可能是该反应的催化剂 B、待测值为15 C、参加反应的Y、M的质量比为5:4 D、该反应一定不是化合反应12. 下面是对四个实验绘制的图形,其中实验结果与对应图形正确的是( )A、等质量的镁粉、锌粉与足量的同浓度的稀硫酸反应 B、过氧化氢分解生成氧气,一份加入二氧化锰,一份不加入二氧化锰
B、过氧化氢分解生成氧气,一份加入二氧化锰,一份不加入二氧化锰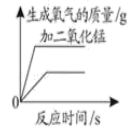 C、电解水生成的气体质量比
C、电解水生成的气体质量比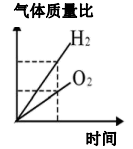 D、在密闭容器中加热高锰酸钾
D、在密闭容器中加热高锰酸钾 13. 逻辑推理是一种重要的化学思维方法。下列推理合理的是( )A、在同一化合物中,金属元素显正价,则非金属元素一定显负价 B、化学变化伴随着能量的变化,则有能量变化的一定是化学变化 C、蜡烛燃烧生成二氧化碳和水,则蜡烛组成中一定含有碳元素和氢元素 D、催化剂的质量在反应前后不变,则在反应前后质量不变的物质一定是该反应的催化剂14. 除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是( )A、N2气体(O2)一通过灼热的铜网 B、木炭粉(CuO)一在空气中灼烧 C、KCl固体(MnO2)一加入足量的水溶解,过滤,蒸发结晶 D、FeCl2溶液(CuCl2)一加入过量的铁粉,过滤15. 取一定质量的碳酸钙高温加热一段时间后,冷却,测得剩余固体的质量为 21.2g,其中钙元素和碳元素的质量比为 10:1,向剩余固体中加入足量稀盐酸,充分反应后生成二氧化碳气体的质量为( )A、4.4g B、2.2g C、1.1g D、0
13. 逻辑推理是一种重要的化学思维方法。下列推理合理的是( )A、在同一化合物中,金属元素显正价,则非金属元素一定显负价 B、化学变化伴随着能量的变化,则有能量变化的一定是化学变化 C、蜡烛燃烧生成二氧化碳和水,则蜡烛组成中一定含有碳元素和氢元素 D、催化剂的质量在反应前后不变,则在反应前后质量不变的物质一定是该反应的催化剂14. 除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是( )A、N2气体(O2)一通过灼热的铜网 B、木炭粉(CuO)一在空气中灼烧 C、KCl固体(MnO2)一加入足量的水溶解,过滤,蒸发结晶 D、FeCl2溶液(CuCl2)一加入过量的铁粉,过滤15. 取一定质量的碳酸钙高温加热一段时间后,冷却,测得剩余固体的质量为 21.2g,其中钙元素和碳元素的质量比为 10:1,向剩余固体中加入足量稀盐酸,充分反应后生成二氧化碳气体的质量为( )A、4.4g B、2.2g C、1.1g D、0二、填空题(20分)(每个化学方程式2分)
-
16. 用适当的化学用语填空:(1)、2个氮分子;(2)、2个铁离子;(3)、标出硫酸铝中铝元素的化合价;(4)、相对分子质量为720的碳单质的化学式:;(5)、一个水分子(H2O)中含有中子。17. 郴州东江湖,储水量大,水质优良,一直保持地表水一类水标准,被引入到多地作为居民饮用水。请回答下列问题:(1)、天然水中含有许多杂质,可以利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是。(2)、以下防治水污染的措施中,你认为可行的是_________________(填写字母编号)A、禁止使用农药和化肥 B、应用新技术、新工艺减少污染物的产生 C、抑制水中所有动植物的生长 D、工业废水经净化处理达标后再排放(3)、水是一种常见的溶剂,同时也参与很多化学反应,如反应 ,其中X的化学式为 , Mg3N2也能与水发生上述类似的反应,请写出反应的化学方程。18. 元素周期表是学习化学的重要工具。下图为元素周期表的一部分:
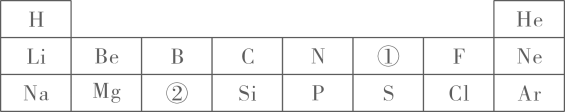 (1)、晶体硅是制造计算机芯片的材料,硅元素位于第周期,其原子结构示意图为 , 通过观察发现元素所在的周期数和它的原子结构中的相等。(2)、M2+和Ne原子具有相同的核外电子数,M2+的离子符号是。(3)、①和②两种元素组成的化合物的化学式为。19. 回答下列问题:(1)、Ga(NH4)(SO4)2中含有的带正电的原子团(根)是(填化学符号)。(2)、下图是某课外小组对教材实验进行的创新设计,请回答相关问题:
(1)、晶体硅是制造计算机芯片的材料,硅元素位于第周期,其原子结构示意图为 , 通过观察发现元素所在的周期数和它的原子结构中的相等。(2)、M2+和Ne原子具有相同的核外电子数,M2+的离子符号是。(3)、①和②两种元素组成的化合物的化学式为。19. 回答下列问题:(1)、Ga(NH4)(SO4)2中含有的带正电的原子团(根)是(填化学符号)。(2)、下图是某课外小组对教材实验进行的创新设计,请回答相关问题: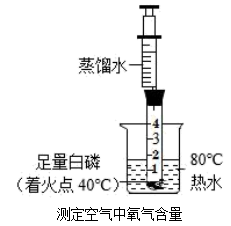
试管中观察到白磷燃烧的现象是。反应完全后,待冷却到室温,可观察到注射器中蒸馏水慢慢流入试管中,试管内液面最终上升至约刻度处。
(3)、 铝能与氢氧化钠和水发生反应,生成偏铝酸钠(NaAlO2)和一种气体单质(写化学方程式)。三、简答题(10分)(每个化学方程式2分)
-
20. 于海底的可燃冰的化学式为CH4•8H2O,其外观像冰一样但遇火即可燃烧。(1)、可燃冰属于(填“可”或“不可”)再生资源。为缓解能源危机,人们还必须积极开发利用新能源,请写出一种新能源。(2)、可燃冰经过处理可得到CH4 , 点燃CH4之前应。(3)、工业上,可以利用甲烷获得氢气,其反应的微观示意图如图:
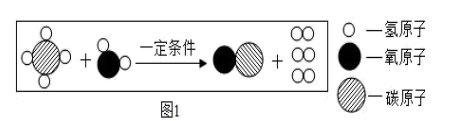
图1所示反应的化学方程式为。
(4)、“纸火锅”是用纸来代替铁锅,纸不会燃烧的原因是。21. A、B、C、D为初中化学常见物质,A为黑色粉末,C为紫红色固体,在一定条件下转化关系如图所示。 (1)、若常温下B、D均为气体,则B是(填化学式)。(2)、若常温下B为固体,D为气体,则A与B反应的化学方程式为 , 其化学基本反应类型是反应。
(1)、若常温下B、D均为气体,则B是(填化学式)。(2)、若常温下B为固体,D为气体,则A与B反应的化学方程式为 , 其化学基本反应类型是反应。四、实验探究题(15分)(每个化学方程式2分)
-
22. 根据下列实验装置图回答问题:
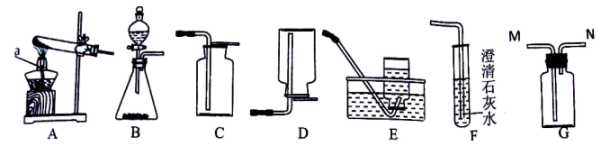 (1)、写出图中仪器a的名称:。(2)、实验室用高锰酸钾制取氧气应选用的发生装置为(填字母序号),写出该反应的化学方程式。若用充满水的G装置来测量产生的氧气体积,则要在(填M或N)端的右边连接(填一仪器名称)。(3)、实验室可利用装置F来检验生成的二氧化碳,请写出有关的化学方程式。(4)、如图中a、c为湿润的紫色石蕊小花,要证明二氧化碳与水反应,则b为。若观察到c比a先变红,说明二氧化碳具有的物理性质是。
(1)、写出图中仪器a的名称:。(2)、实验室用高锰酸钾制取氧气应选用的发生装置为(填字母序号),写出该反应的化学方程式。若用充满水的G装置来测量产生的氧气体积,则要在(填M或N)端的右边连接(填一仪器名称)。(3)、实验室可利用装置F来检验生成的二氧化碳,请写出有关的化学方程式。(4)、如图中a、c为湿润的紫色石蕊小花,要证明二氧化碳与水反应,则b为。若观察到c比a先变红,说明二氧化碳具有的物理性质是。 23. 某同学在实验室里发现了一种外观为银白色的金属M,他产生了探究这种金属活动性的兴趣。在老师的指导下,对M、锌和铜三种金属的活动性顺序进行了探究。
23. 某同学在实验室里发现了一种外观为银白色的金属M,他产生了探究这种金属活动性的兴趣。在老师的指导下,对M、锌和铜三种金属的活动性顺序进行了探究。【查找资料】金属M的硫酸盐溶液是无色的。
(1)、 【提出猜想】猜想l:锌>铜>M 猜想2:锌>M>铜 猜想3:
(2)、【实验探究】实验前,要先将金属M用砂纸打磨表面,理由是。
(3)、将打磨后的金属M放入硫酸铜溶液中,现象是 , 说明金属活动性:M>铜。(4)、将打磨后的金属M和锌分别放入稀硫酸中,稀硫酸与金属M反应比与锌反应剧烈,说明金属活动性:。(5)、【实验结论】猜想是正确的。
五、计算题(10分)
-
24. 钙是人体内含量最高的金属元素,缺钙者可以在医生的指导下口服葡萄糖酸钙溶液来补钙,如表为某品牌“葡萄糖酸钙口服溶液”的部分说明。
葡萄糖酸钙口服溶液
【成分】本品每毫升含葡萄糖酸钙【(CxH11O7)2Ca】100mg(相当于钙9.3mg)
【包装】每支装10mL,每盒12支。
葡萄糖酸钙的相对分子质量为430,请计算:
请计算:
(1)、x为。(2)、葡萄糖酸钙中钙的质量分数为。(保留一位小数)(3)、如果小明每天需摄入钙的量为1000mg,他通过食物的钙摄入量为721mg,你建议他每天应该服用该品牌口服液支来补充钙摄入量的不足。(写出计算过程)25. 某课外活动小组为了测定铜铁合金中铁的质量分数,现取铜铁合金样品20.0g,将80.0g稀硫酸平均分成4等份,分4次逐渐加入到样品中,每次充分反应后测得剩余固体质量如下表:次数
1
2
3
4
加入稀硫酸的质量/g
20.0
20.0
20.0
20.0
剩余固体质量/g
17.2
14.4
13.0
13.0
试求:
(1)、20.0g铜铁合金中,铜的质量为。(2)、铜铁合金中,铁的质量分数为。(3)、20.0g稀硫酸溶液中硫酸的质量分数。