人教版初中化学九年级下册 10.1 常见的酸和碱 同步分层训练培优题
试卷更新日期:2024-01-14 类型:同步测试
一、选择题
-
1. 下列实验操作中,正确的是( )A、
 加热液体
B、
加热液体
B、 用木炭代替红磷测空气中氧气含量
C、
用木炭代替红磷测空气中氧气含量
C、 稀释浓硫酸
D、
稀释浓硫酸
D、 验证铜、铁、镁的金属活动性顺序强弱
2. 下列物质常用于改良酸性土壤的是( )A、熟石灰 B、烧碱 C、食盐 D、大理石3. 蔬菜大棚中常增施二氧化碳肥以促进植物生长,增施过程的操作如下图所示。以下分析正确的是( )
验证铜、铁、镁的金属活动性顺序强弱
2. 下列物质常用于改良酸性土壤的是( )A、熟石灰 B、烧碱 C、食盐 D、大理石3. 蔬菜大棚中常增施二氧化碳肥以促进植物生长,增施过程的操作如下图所示。以下分析正确的是( ) A、①中烧杯里的试剂Y是浓硫酸 B、③中小孔越多生成二氧化碳越多 C、④中溶液所含硫酸铵少于78g D、④中塑料桶悬挂高低会影响肥效4. 下列实验现象描述正确的是( )。A、打开浓盐酸试剂瓶时,瓶口会出现白烟 B、向氢氧化钠溶液中加入一定量的石蕊溶液,溶液变为红色 C、铝丝伸入硫酸铜溶液中,银白色固体表面析出紫红色固体,溶液由无色变为蓝色 D、生石灰与水反应:放热,形成白色浆液5. 现有Mg和MgO的固体混合物3g,经测定镁元素的质量分数为80%,向固体混合物中加入100g一定溶质质量分数的稀硫酸,恰好完全反应,下列说法错误的是( )A、反应后溶液中的溶质只有MgSO4 B、反应中有气泡产生 C、所用稀硫酸中溶质的质量分数为19.6% D、生成MgSO4的质量为12g6. 逻辑推理是化学常用的思维方法,下列推理正确的是( )A、饱和溶液不能继续溶解某种溶质,其它物质也不能继续溶解在该饱和溶液中 B、酸与金属氧化物生成盐和水,则生成盐和水的反应不一定是酸与金属氧化物的反应 C、活泼金属与酸反应放出气体,所以能与酸反应放出气体的物质一定是活泼金属 D、溶液是均一、稳定的混合物,所以均一、稳定的物质一定是溶液7. 逻辑推理是一种重要的化学思维方法,以下推理合理的是()A、因为离子是带电的原子或原子团,所以带电的粒子一定就是离子 B、因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有C和H C、因为单质中只含一种元素,所以只含一种元素的物质一定是单质 D、因为金属和酸反应能生成气体,所以和酸反应生成气体的物质一定是金属8. 取氧化铁和铁的混合物,将其充分还原,固体质量减轻4.8g,将还原后的固体加入到200g盐酸中,恰好完全反应,得到溶液221.6g,则原固体中单质铁和氧化铁的质量比为( )A、2:1 B、10:7 C、1:1 D、7:109. 如图一所示,甲、乙烧杯中分别有等质量的铁和氧化铜粉末,再分别加入稀硫酸。加入的稀硫酸质量与烧杯中所得溶液的质量关系如图二所示。下列说法错误的是( )
A、①中烧杯里的试剂Y是浓硫酸 B、③中小孔越多生成二氧化碳越多 C、④中溶液所含硫酸铵少于78g D、④中塑料桶悬挂高低会影响肥效4. 下列实验现象描述正确的是( )。A、打开浓盐酸试剂瓶时,瓶口会出现白烟 B、向氢氧化钠溶液中加入一定量的石蕊溶液,溶液变为红色 C、铝丝伸入硫酸铜溶液中,银白色固体表面析出紫红色固体,溶液由无色变为蓝色 D、生石灰与水反应:放热,形成白色浆液5. 现有Mg和MgO的固体混合物3g,经测定镁元素的质量分数为80%,向固体混合物中加入100g一定溶质质量分数的稀硫酸,恰好完全反应,下列说法错误的是( )A、反应后溶液中的溶质只有MgSO4 B、反应中有气泡产生 C、所用稀硫酸中溶质的质量分数为19.6% D、生成MgSO4的质量为12g6. 逻辑推理是化学常用的思维方法,下列推理正确的是( )A、饱和溶液不能继续溶解某种溶质,其它物质也不能继续溶解在该饱和溶液中 B、酸与金属氧化物生成盐和水,则生成盐和水的反应不一定是酸与金属氧化物的反应 C、活泼金属与酸反应放出气体,所以能与酸反应放出气体的物质一定是活泼金属 D、溶液是均一、稳定的混合物,所以均一、稳定的物质一定是溶液7. 逻辑推理是一种重要的化学思维方法,以下推理合理的是()A、因为离子是带电的原子或原子团,所以带电的粒子一定就是离子 B、因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有C和H C、因为单质中只含一种元素,所以只含一种元素的物质一定是单质 D、因为金属和酸反应能生成气体,所以和酸反应生成气体的物质一定是金属8. 取氧化铁和铁的混合物,将其充分还原,固体质量减轻4.8g,将还原后的固体加入到200g盐酸中,恰好完全反应,得到溶液221.6g,则原固体中单质铁和氧化铁的质量比为( )A、2:1 B、10:7 C、1:1 D、7:109. 如图一所示,甲、乙烧杯中分别有等质量的铁和氧化铜粉末,再分别加入稀硫酸。加入的稀硫酸质量与烧杯中所得溶液的质量关系如图二所示。下列说法错误的是( ) A、曲线a表示稀硫酸与氧化铜的反应 B、当加入的硫酸质量为m1g时,将甲、乙烧杯混合充分反应,上层溶液中的溶质可能为一种 C、当加入的硫酸质量为m2g时,甲烧杯中硫酸亚铁的质量大于乙烧杯中硫酸铜的质量 D、当加入的硫酸质量为m3g时,甲、乙烧杯内溶液的质量差为产生的氢气质量10. 现有铜和氧化铜的混合物10g,向其中加入100g溶质质量分数为9.8%的稀硫酸,恰好完全反应。则该混合物中铜元素的质量分数为( )A、16% B、36% C、64% D、84%
A、曲线a表示稀硫酸与氧化铜的反应 B、当加入的硫酸质量为m1g时,将甲、乙烧杯混合充分反应,上层溶液中的溶质可能为一种 C、当加入的硫酸质量为m2g时,甲烧杯中硫酸亚铁的质量大于乙烧杯中硫酸铜的质量 D、当加入的硫酸质量为m3g时,甲、乙烧杯内溶液的质量差为产生的氢气质量10. 现有铜和氧化铜的混合物10g,向其中加入100g溶质质量分数为9.8%的稀硫酸,恰好完全反应。则该混合物中铜元素的质量分数为( )A、16% B、36% C、64% D、84%二、填空题
-
11. 请从B~D中任选两个作答,若均作答,按前两个计分。按要求从下列物质中选出两种放入瓶中,制作“彩色许愿瓶”。
①Fe ②稀盐酸 ③无色酚酞溶液 ④紫色石蕊溶液 ⑤Ca(OH)2溶液 ⑥ Fe2O3

序号
瓶内溶液颜色
选用的物质
A
蓝色
④⑤
B
浅绿色
C
黄色
D
红色
12. 在探究碱的性质时,用到了氢氧化钾,小铭在整理实验台时发现,盛有氢氧化钾固体的试剂瓶没有盖上瓶盖。他认为瓶中氢氧化钾已有部分变质,他推理的依据是(用化学方程式表示)。要证明氢氧化钾部分变质,请写出实验步骤、可能的现象及相关推理。三、综合题
-
13. 铜及其化合物广泛应用于生活生产中。(1)、青铜属于 填“金属单质”或“合金”。(2)、 , CuO、三种物质的转化关系如图甲所示:
①反应Ⅱ中,CuO与稀硫酸反应的现象是 。
②反应Ⅲ中, 填化学式可将CuO一步转化为Cu。
③图乙所示的实验中,将铜片浸入 填化学式溶液中,可根据现象证明Cu的金属活动性比Ag强。
(3)、往四个都装有15g样品只含Cu和的烧杯中,分别加入不同质量的稀硫酸,反应过程中的质量关系如下表所示,计算所用稀硫酸的溶质质量分数。烧杯序号
一
二
三
四
稀硫酸的质量
50
100
150
200
剩余固体质量
11
7
3
3

四、实验探究题
-
14. 某探究小组分别设计了有关“质量守恒定律”的两个验证实验,两套实验装置如图所示。回答下列问题:
甲
 乙
乙 (1)、利用A装置进行验证实验:甲装置中气球的作用是。瓶底的细砂能隔热,加热玻璃管至红热,引燃白磷,锥形瓶中产生的现象为 , 该反应的化学方程式为。待锥形瓶冷却后,将其放回原托盘上,天平保持平衡。(2)、利用B装置进行验证实验:烧杯中的现象是 , 当反应后可观察到天平不平衡,其原因是。该反应(填“遵守”或“不遵守”)质量守恒定律。(3)、通过对比分析甲和乙验证实验,在反应物不变的前提下,要保持天平平衡,使实验数据能真实反映质量守恒定律,对验证实验乙的改进措施为。
(1)、利用A装置进行验证实验:甲装置中气球的作用是。瓶底的细砂能隔热,加热玻璃管至红热,引燃白磷,锥形瓶中产生的现象为 , 该反应的化学方程式为。待锥形瓶冷却后,将其放回原托盘上,天平保持平衡。(2)、利用B装置进行验证实验:烧杯中的现象是 , 当反应后可观察到天平不平衡,其原因是。该反应(填“遵守”或“不遵守”)质量守恒定律。(3)、通过对比分析甲和乙验证实验,在反应物不变的前提下,要保持天平平衡,使实验数据能真实反映质量守恒定律,对验证实验乙的改进措施为。五、计算题
-
15. 氢氧化钠是一种重要的工业原料,同时也是实验室中常用的一种化学药品。(1)、制取少量氢氧化钠可以用如图所示的流程:

①上述步骤②的基本反应类型是 反应(填“化合”、“分解”、“置换”或“复分解”之一)。
②写出步骤③发生反应的化学方程式 。
③氢氧化钠有很强的腐蚀性,如果不小心沾到皮肤上,要立即用大量的水冲洗 ,然后涂上 (填选项序号之一)。
A.稀硫酸
B.3%﹣5%的碳酸氢钠溶液
C.硼酸溶液
D.石灰水
(2)、在一烧杯中盛有20gNa2CO3和NaCl组成的固体混合物,加100g水完全溶解,制成不饱和溶液。向其中逐渐滴加溶质质量分数为10%的稀盐酸 ,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答问题: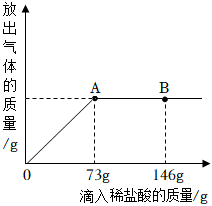
①当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质有 。
②当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求所得氯化钠溶液的质量。
-
-