山西省吕梁市交城县2023-2024学年九年级上学期期中化学试卷
试卷更新日期:2024-01-12 类型:期中考试
一、选择题:(在每小题给出的四个选项中,只有一项符合题目要求,请选出并将其字母标号填在下表相应题号的空格内。每小题2分,共20分)
-
1. 诗词是中华民族的文化瑰宝,下列诗句中隐含有化学变化的是()A、千锤万凿出深山 B、蜡炬成灰泪始干 C、只要功夫深,铁杵磨成针 D、夜来风雨声,花落知多少2. 制出第一张元素周期表的科学家是( )A、张青莲 B、道尔顿 C、门捷列夫 D、阿伏加德罗3. 食品包装袋内常用来防腐的气体是( )A、氧气 B、氮气 C、氢气 D、稀有气体4. 模型认知是化学核心素养之一,下列化学模型正确的是( )
A
B
C
D

物质的性质和用途
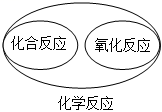
化学变化类型
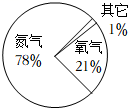
空气成分质量分数
四个氮原子模型
A、A B、B C、C D、D5. “化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xī)”,如今把这种“矽”元素命名为( )A、氧 B、硅 C、铝 D、铁6. 下列微粒结构示意图中,表示阴离子的是( )A、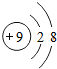 B、
B、 C、
C、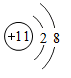 D、
D、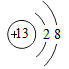 7. 下列基本实验操作正确的是( )A、
7. 下列基本实验操作正确的是( )A、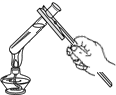 加热液体
B、
加热液体
B、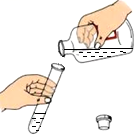 倾倒液体
C、
倾倒液体
C、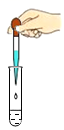 滴加液体
D、
滴加液体
D、 检查气密性
8. 科学家发现在负压和超低温条件下,水会像棉花糖一样,以蓬松轻盈的形式稳定存在,被称为“气凝胶水”。下列说法正确的是( )A、“气凝胶水”由氢气和氧气组成 B、“气凝胶水”在任何条件下都不会融化 C、结成“气凝胶水”后,分子停止运动 D、“气凝胶水”与水的化学性质相同9. 逻辑推理是化学学习中常用的思维方法,下列推理正确的是( )A、化学反应通常伴随着发光、放热等现象,有发光、放热现象的反应都是化学反应 B、同一化合物中,金属元素显正价,所以化合物中非金属元素一定都显负价 C、氧气由氧元素组成,所以制取氧气的反应物一定含有氧元素 D、单质是由同种元素组成的,则只含一种元素的物质一定是单质10. 某同学为了探究微粒性质,按图示进行实验,并借助传感器测得U型管a、b中氨气浓度随时间变化的曲线。下列关于该实验的说法错误的是( )
检查气密性
8. 科学家发现在负压和超低温条件下,水会像棉花糖一样,以蓬松轻盈的形式稳定存在,被称为“气凝胶水”。下列说法正确的是( )A、“气凝胶水”由氢气和氧气组成 B、“气凝胶水”在任何条件下都不会融化 C、结成“气凝胶水”后,分子停止运动 D、“气凝胶水”与水的化学性质相同9. 逻辑推理是化学学习中常用的思维方法,下列推理正确的是( )A、化学反应通常伴随着发光、放热等现象,有发光、放热现象的反应都是化学反应 B、同一化合物中,金属元素显正价,所以化合物中非金属元素一定都显负价 C、氧气由氧元素组成,所以制取氧气的反应物一定含有氧元素 D、单质是由同种元素组成的,则只含一种元素的物质一定是单质10. 某同学为了探究微粒性质,按图示进行实验,并借助传感器测得U型管a、b中氨气浓度随时间变化的曲线。下列关于该实验的说法错误的是( )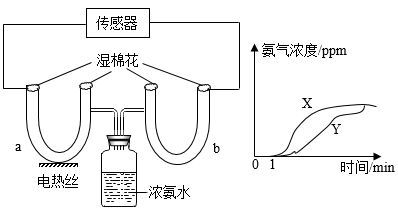 A、曲线X对应的U型管为a B、实验证明了微粒运动速率与温度有关 C、湿棉花的作用是吸收NH3 , 减少NH3对空气的污染 D、0﹣1分钟,因为微粒静止不动,所以氨气浓度为零
A、曲线X对应的U型管为a B、实验证明了微粒运动速率与温度有关 C、湿棉花的作用是吸收NH3 , 减少NH3对空气的污染 D、0﹣1分钟,因为微粒静止不动,所以氨气浓度为零二、工程、技术应用题(化学方程式每空2分,其余每空1分,共13分。)
-
11. 新型材料纳米级铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备流程如图所示:
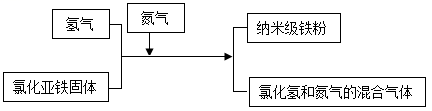 (1)、纳米级铁粉在氧气中能自发燃烧生成黑色固体,发生反应的化学反应方程式为 , 该反应的基本类型是。(2)、请补充完成上述制备工艺的化学方程式:H2+FeCl2Fe+12. 生活中离不开各种电池,从镍氢电池到锂电池,再到钠电池、钾电池,科学家在不断提升电池的性能。请根据如图回答问题:(1)、金属失去电子后形成 (填“阴”或“阳”)离子,锂、钠、钾等原子很容易失去电子变成离子,所以常被用作电池材料。这些元素具有相似的化学性质的原因 。(2)、研究表明,半径越大的离子越容易在电池正负极之间移动,充电速度越快。如图是锂、钠、钾三种金属的离子半径大小,电池容量相同的这三种电池,充满电的时间最短的 电池。
(1)、纳米级铁粉在氧气中能自发燃烧生成黑色固体,发生反应的化学反应方程式为 , 该反应的基本类型是。(2)、请补充完成上述制备工艺的化学方程式:H2+FeCl2Fe+12. 生活中离不开各种电池,从镍氢电池到锂电池,再到钠电池、钾电池,科学家在不断提升电池的性能。请根据如图回答问题:(1)、金属失去电子后形成 (填“阴”或“阳”)离子,锂、钠、钾等原子很容易失去电子变成离子,所以常被用作电池材料。这些元素具有相似的化学性质的原因 。(2)、研究表明,半径越大的离子越容易在电池正负极之间移动,充电速度越快。如图是锂、钠、钾三种金属的离子半径大小,电池容量相同的这三种电池,充满电的时间最短的 电池。 (3)、请画出钠离子的离子结构示意图 。13. 工业制取氧气
(3)、请画出钠离子的离子结构示意图 。13. 工业制取氧气空气中氧气约占21%,利用分离液态空气的方法得到氧气是工业上制取氧气的重要途径,下面是工业上制氧气流程图:
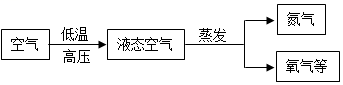 (1)、工业上分离液态空气制氧气的变化属于 (填“物理变化”或“化学变化”)。(2)、这样制得的氧气是 (填“纯净物“或“混合物”)。(3)、氮气的沸点﹣196℃,氧气的沸点﹣183℃,在蒸发的过程中 先被蒸发出来。(4)、任何物质我们都要辩证的看待,请分别从正反两面分析氧气。
(1)、工业上分离液态空气制氧气的变化属于 (填“物理变化”或“化学变化”)。(2)、这样制得的氧气是 (填“纯净物“或“混合物”)。(3)、氮气的沸点﹣196℃,氧气的沸点﹣183℃,在蒸发的过程中 先被蒸发出来。(4)、任何物质我们都要辩证的看待,请分别从正反两面分析氧气。利:。(写一点)
弊:。(写一点)
三、科普阅读题(化学方程式2分,其余每空1分,共6分)
-
14. 阅读下列科技短文,回答问题。
中国空间站天和核心舱可支持三名航天员长期在轨驻留,航天员在轨的每一天都离不开环控生保系统。首先,环控生保系统的再生生保系统利用循环水电解制氧气,保证航天员氧气需求,电解水产生的氢气与宇航员呼出的二氧化碳在特种反应器中进行催化反应,从而降低舱内二氧化碳的浓度。其次,环控生保系统的水处理系统主要是将水蒸气、汗液、尿液和生活废水等进行处理,经过该系统处理的水达到饮用水标准,且水的回收率达80%以上,回收的水用于航天员生活用水和电解制氧。
(1)、水和过氧化氢的化学性质的不同的原因是。(2)、再生生保系统利用循环水电解制氧气的化学方程式为;电解水前向水中加入少量氢氧化钠的目的是。(3)、氢气与二氧化碳在催化剂作用下的反应原理为 , 则X的化学式为。(4)、 环控生保系统的水处理系统的优点是。(写出一点即可)四、物质性质及应用题(每空1分,共8分。)
-
15. 从化学的视角认识消毒剂
二氧化氯消毒片是一种常用的消毒剂。该消毒片溶于水后可用于杀灭物体表面、空气中的细菌、病毒。常温常压下,二氧化氯(ClO2)是一种橙黄色气体,密度比空气大,有刺激性气味,易溶于水,遇热水能分解,光照时也易分解,腐蚀性很强。
根据上述资料,回答问题:
(1)、 上述描述中,二氧化氯的物理性质有 , 化学性质有 。二氧化氯消毒片的用途是 。(2)、二氧化氯中氯元素的化合价为 。其中,氯元素与氧元素的质量比是(填最简整数比) 。(3)、温度降为11℃时,二氧化氯液化为液体,请从微观角度解释这一过程 。(4)、使用二氧化氯时要十分小心,一旦粘在手上,应如何处理?。储存二氧化氯时,应放在 环境中。五、实验探究题(化学方程式每空2分,其余每空1分,共16分)
-
16. 氧气是维持人类生命的重要气体。(1)、实验一:实验室常用如下装置制取氧气。
实验室用高锰酸钾制取氧气,反应原理是 , 选用的发生装置为(填字母):用D装置收集氧气,证明氧气集满的方法为 , 用E装置收集氧气时,发现水槽中水呈现紫红色,你认为可能的原因是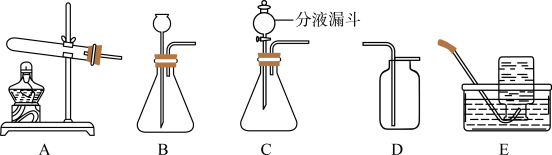 (2)、用C装置来制取氧气,分液漏斗中的药品可为。(3)、用B装置制取氧气时需要使用催化剂。下列关于催化剂说法正确的是____(填字母)。A、该反应不加催化剂就没有氧气生成 B、在化学反应前后催化剂的化学性质没有改变 C、加入催化剂不但可以加快反应速度,还可以增加生成氧气的质量(4)、实验二:家用制氧机可以获得“富氧空气”(氧气含量高于普通空气)
(2)、用C装置来制取氧气,分液漏斗中的药品可为。(3)、用B装置制取氧气时需要使用催化剂。下列关于催化剂说法正确的是____(填字母)。A、该反应不加催化剂就没有氧气生成 B、在化学反应前后催化剂的化学性质没有改变 C、加入催化剂不但可以加快反应速度,还可以增加生成氧气的质量(4)、实验二:家用制氧机可以获得“富氧空气”(氧气含量高于普通空气)用图3装置测定家用制氧机获得的“富氧空气”中氧气的含量(集气瓶中“富氧空气”体积为100mL,底部残留少量水,燃烧匙内有足量红磷),操作如下:
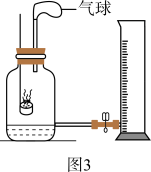
①往量筒内加入适量水,读出量筒内水的体积为100mL;
②点燃红磷,充分反应并冷却至室温;
③打开止水夹,待右侧量筒内液面不再变化时,调节两边液面在同一水平面上,读出量筒内水的体积为18mL。
检查装置气密性:关闭弹簧夹,两手紧握集气瓶。过一会儿,若观察到________,证明装置不漏气。(5)、本次实验测得“富氧空气”中氧气的体积分数为。(6)、实验三:研究“富氧空气”的应用通过重油、褐煤在氧气含量不同的空气中燃烧的实验,得到有关数据如图4。
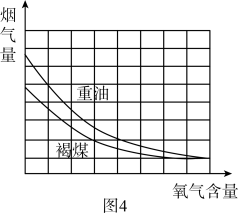
结合图4,简述减少燃料燃烧尾气污染的措施:。
17. 同学们为研究分子的性质做了如下三组实验:(已知氨气溶于水形成氨水,氨水具有挥发性,氨水能使酚酞溶液变红)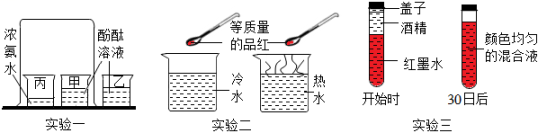 (1)、实验一中,可以看到的现象是 ;其中烧杯乙的作用 。(2)、实验二中,观察到品红在 (填“冷”或“热”)水中扩散更快,原因是 。(3)、实验三中,先在一支试管中装一部分红墨水,再在液面上注满酒精(缓缓注入),加盖密封后静置,30日后再观察,现象如图所示,这一现象说明了 、。
(1)、实验一中,可以看到的现象是 ;其中烧杯乙的作用 。(2)、实验二中,观察到品红在 (填“冷”或“热”)水中扩散更快,原因是 。(3)、实验三中,先在一支试管中装一部分红墨水,再在液面上注满酒精(缓缓注入),加盖密封后静置,30日后再观察,现象如图所示,这一现象说明了 、。六、定量分析题(共7分)
-
18. 根据化学方程式计算,制取4.8g氧气,至少需要过氧化氢的质量是多少?
-
-