北京市东城区教育集团2023-2024学年九年级上学期化学期末考试试卷
试卷更新日期:2024-01-12 类型:期末考试
一、第一部分共25题,每题1分,共25分。在每题列出的四个选项中,选出最符合题目要求的一项。
-
1. 第一个通过实验测定出空气中氧气含量的科学家是( )A、阿伏加德罗
 B、道尔顿
B、道尔顿 C、门捷列夫
C、门捷列夫 D、拉瓦锡
D、拉瓦锡 2. 空气的成分中,体积分数约占78%的是( )A、二氧化碳 B、氧气 C、氮气 D、水蒸气3. 下列过程中,一定发生了化学变化的是( )A、衣服晾干 B、食物腐败 C、冰雪融化 D、干冰升华4. 下列属于纯净物的是( )A、矿泉水 B、地下水 C、蒸馏水 D、地表水5. 分类观是化学学习中的一种思维方式。下列元素中,属于金属元素的是( )A、H B、C C、Na D、S6. 下列元素符号书写正确的是( )A、镁mg B、氮C C、钙Ca D、氦he7. 加碘食盐、高钙牛奶中的“碘”和“钙”是指A、单质 B、分子 C、原子 D、元素8. 下列物质中,属于氧化物的是( )A、氧气O2 B、水H2O C、碳酸钙CaCO3 D、高锰酸钾KMnO49. 地壳中含量最多的元素是( )A、Si B、Al C、O D、Fe10. 下列说法不合理的是( )A、1L水和1L酒精混合后体积小于2L,是由于分子之间有间隔 B、6000L氧气被压缩装入40L钢瓶中,是由于氧气分子之间间隔变小 C、花园中能闻到花香,是由于分子永不停息地做无规则运动 D、氧气在放电条件下生成臭氧()的过程中没有生成新的分子11. “中国天眼”射电望远镜使用了碳化硅(SiC)。碳元素和硅元素的本质区别是( )A、质子数不同 B、相对原子质量不同 C、中子数不同 D、最外层电子数不同12. 下列实验操作不正确的是( )
2. 空气的成分中,体积分数约占78%的是( )A、二氧化碳 B、氧气 C、氮气 D、水蒸气3. 下列过程中,一定发生了化学变化的是( )A、衣服晾干 B、食物腐败 C、冰雪融化 D、干冰升华4. 下列属于纯净物的是( )A、矿泉水 B、地下水 C、蒸馏水 D、地表水5. 分类观是化学学习中的一种思维方式。下列元素中,属于金属元素的是( )A、H B、C C、Na D、S6. 下列元素符号书写正确的是( )A、镁mg B、氮C C、钙Ca D、氦he7. 加碘食盐、高钙牛奶中的“碘”和“钙”是指A、单质 B、分子 C、原子 D、元素8. 下列物质中,属于氧化物的是( )A、氧气O2 B、水H2O C、碳酸钙CaCO3 D、高锰酸钾KMnO49. 地壳中含量最多的元素是( )A、Si B、Al C、O D、Fe10. 下列说法不合理的是( )A、1L水和1L酒精混合后体积小于2L,是由于分子之间有间隔 B、6000L氧气被压缩装入40L钢瓶中,是由于氧气分子之间间隔变小 C、花园中能闻到花香,是由于分子永不停息地做无规则运动 D、氧气在放电条件下生成臭氧()的过程中没有生成新的分子11. “中国天眼”射电望远镜使用了碳化硅(SiC)。碳元素和硅元素的本质区别是( )A、质子数不同 B、相对原子质量不同 C、中子数不同 D、最外层电子数不同12. 下列实验操作不正确的是( )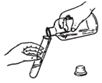
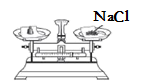
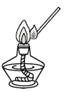
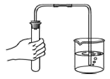
A.倾倒液体
B.称量固体
C.点燃酒精灯
D.检查气密性
A、A B、B C、C D、D13. 下列物质均可用作燃料,在中充分燃烧时,不会产生的是( )A、 B、 C、木炭 D、CO14. 下列物质中,含有氧分子的是( )A、O2 B、SO2 C、H2O2 D、H2CO315. 下列物质的化学式书写正确的是( )A、氧化镁MgO B、氢氧化钙CaOH C、硫酸铁 D、氧化铁16. 下列符号既能表示一种元素又能表示一种物质的是( )A、Fe B、 C、H D、17. “冷热双吸”材料中常含有钒元素。钒元素在元素周期表中的信息如图。完成下面小题。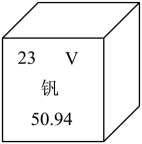
下列有关钒元素的说法不正确的是( )
A、原子序数是23 B、属于非金属元素 C、元素符号是V D、相对原子质量为50.9418. 钒原子的核外电子数是( )A、23 B、28 C、51 D、7419. 利用氢氟酸(HF)蚀刻玻璃,发生的化学方程式为:SiO2 +4HF =X↑+2H2O,物质X为( )A、SiO B、SiF4 C、SiF D、F220. 热干面是武汉的传统小吃。下列制作热干面的主要操作中,属于过滤的是( )A.调酱
B.煮面
C.捞面
D.拌面



 A、A B、B C、C D、D21. 物质的性质决定其用途。下列物质的性质与其用途相匹配的是( )A、稀有气体化学性质不活泼,用作焊接金属的保护气 B、氧气有可燃性,用于火箭推进剂 C、石墨具有导电性,用于制铅笔芯 D、金刚石无色透明,用于切割玻璃22. 下列化学反应中,属于分解反应的是( )A、 B、 C、 D、23. 歼-20是高态势感知、高机动性的隐形战斗机。其中隐身材料的合成原料之一为间苯二胺()。下列说法正确的是( )A、间苯二胺由16种元素组成 B、间苯二胺由16个原子构成 C、间苯二胺的相对分子质量是108g D、间苯二胺中碳、氢元素质量比为9:124. 光电材料吸收光产生电流能分解水。在吸收相同光照的条件下,二氧化硅薄膜中嵌入纳米镍(Ni)后,电流增大,产生氢气的速率加快。下列有关说法正确的是( )
A、A B、B C、C D、D21. 物质的性质决定其用途。下列物质的性质与其用途相匹配的是( )A、稀有气体化学性质不活泼,用作焊接金属的保护气 B、氧气有可燃性,用于火箭推进剂 C、石墨具有导电性,用于制铅笔芯 D、金刚石无色透明,用于切割玻璃22. 下列化学反应中,属于分解反应的是( )A、 B、 C、 D、23. 歼-20是高态势感知、高机动性的隐形战斗机。其中隐身材料的合成原料之一为间苯二胺()。下列说法正确的是( )A、间苯二胺由16种元素组成 B、间苯二胺由16个原子构成 C、间苯二胺的相对分子质量是108g D、间苯二胺中碳、氢元素质量比为9:124. 光电材料吸收光产生电流能分解水。在吸收相同光照的条件下,二氧化硅薄膜中嵌入纳米镍(Ni)后,电流增大,产生氢气的速率加快。下列有关说法正确的是( )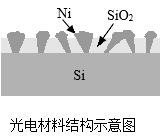 A、二氧化硅属于混合物 B、该材料可将电能转化为光能 C、纳米镍可提高二氧化硅薄膜的电阻 D、硅元素在地壳中的含量优势是其能用于光电材料的原因之一25. 下列实验方案不能达到相应目的是( )
A、二氧化硅属于混合物 B、该材料可将电能转化为光能 C、纳米镍可提高二氧化硅薄膜的电阻 D、硅元素在地壳中的含量优势是其能用于光电材料的原因之一25. 下列实验方案不能达到相应目的是( )A
B
C
D
实验方案
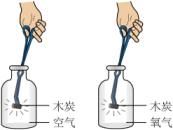
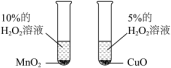
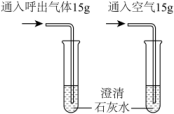
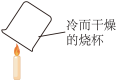
目的
探究的含量不同,对燃烧剧烈程度的影响
比较和CuO对分解的催化效果
证明呼出气体中的含量比吸入空气中多
证明蜡烛燃烧生成了水
A、A B、B C、C D、D二、第二部分共14题,共45分。
-
26. 请从A或B两题中任选一个作答,若两题均作答,按A计分。
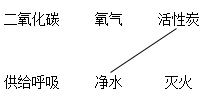
A补齐物质与其用途的连线
B补齐标识与其含义的连线
 27. 国家速滑馆“冰丝带”等冰上场馆,将采用CO2制冰技术,可实现CO2循环利用。(1)、固体二氧化碳俗称 , 能用作制冷剂的原理是。(2)、 再举出生活中减少碳排放的一个实例:。28. 北京冬奥会三大赛区所有场馆,实现了全部使用绿色电能。(1)、目前人们使用的燃料大多来自化石燃料,如煤、和天然气。(2)、天然气(主要成分)充分燃烧的化学方程式是。(3)、 除风能外,其他的新能源还有(举1例)。29. 阅读下面科普短文。
27. 国家速滑馆“冰丝带”等冰上场馆,将采用CO2制冰技术,可实现CO2循环利用。(1)、固体二氧化碳俗称 , 能用作制冷剂的原理是。(2)、 再举出生活中减少碳排放的一个实例:。28. 北京冬奥会三大赛区所有场馆,实现了全部使用绿色电能。(1)、目前人们使用的燃料大多来自化石燃料,如煤、和天然气。(2)、天然气(主要成分)充分燃烧的化学方程式是。(3)、 除风能外,其他的新能源还有(举1例)。29. 阅读下面科普短文。氢气燃烧热值高,约是煤的4倍,被视为理想的清洁燃料。我国氢能的利用还处于起步阶段,2022年中国各能源一次性消费占比如图1所示。
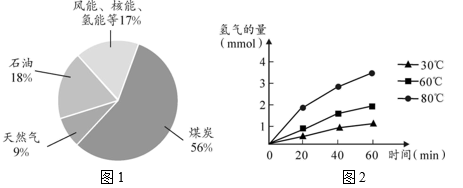
分解海水制氢被认为是最可行的清洁制氢技术,主要有以下两种研究方向。
光解水:在太阳光驱动下催化水发生分解反应。虽然这项技术操作简单,能耗低,无二次污染,但因光腐蚀,能量转换效率低等问题,目前并未实际投入生产。研究发现使用氮化铟镓/氮化镓作为催化剂进行光解水可以提高制氢效率。不同温度下使用该催化剂分解水的速率如图2所示。
电解水:利用电能将水分解。海水中成分复杂,电解时易对电极等材料造成腐蚀或生成不需要的副产物。针对上述问题,我国科学家研制了全球首套海上制氢平台,该平台将海水中的水以水汽的形式跨膜转移,实现了海水中的杂质完全分离。分解海水所需电能完全来自于风能和太阳能,向世界展示零碳能源的中国方案。
依据文章内容回答下列问题。
(1)、 由图1可知,2022年我国能源一次性消费占比最高的是。(2)、 光解水目前未实际投入生产,其原因是。(3)、 由图2可知,温度升高会加快使用氮化铟镓/氮化镓为催化剂进行光解水的反应速率,证据是。(4)、 电解水的化学方程式为。(5)、判断下列说法是否正确(填“对”或“错”)。①煤的热值没有氢气高。
②电解海水时,海水中溶解的物质会对电极造成腐蚀。。
30. 工业制硝酸的转化流程如下(部分反应条件省略):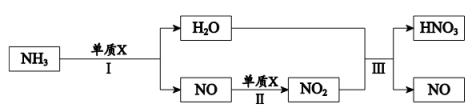 (1)、 单质X是一种常见气体,其化学式是。(2)、配平Ⅲ中反应的化学方程式:
(1)、 单质X是一种常见气体,其化学式是。(2)、配平Ⅲ中反应的化学方程式:。
(3)、为了提高氮原子的利用率,可循环利用的物质是。31. 利用钛精矿(主要成分为)制备金属钛(Ti)的主要工艺流程如下: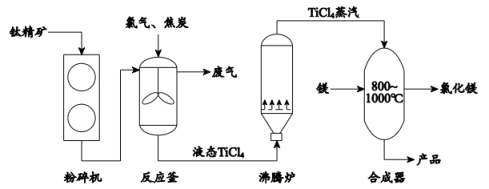 (1)、 中钛元素的化合价是。(2)、 粉碎机中粉碎的目的是。(3)、 推测反应釜废气中含CO,从元素守恒角度说明理由:。32. 下图是氧气的制取和性质实验。
(1)、 中钛元素的化合价是。(2)、 粉碎机中粉碎的目的是。(3)、 推测反应釜废气中含CO,从元素守恒角度说明理由:。32. 下图是氧气的制取和性质实验。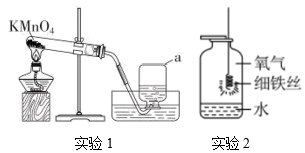 (1)、 实验1,仪器a的名称是 , 制取的化学方程式为。(2)、实验2,观察到铁丝剧烈燃烧、放热、、生成黑色固体。33. 用下图电解水实验研究水的组成。
(1)、 实验1,仪器a的名称是 , 制取的化学方程式为。(2)、实验2,观察到铁丝剧烈燃烧、放热、、生成黑色固体。33. 用下图电解水实验研究水的组成。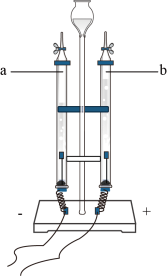 (1)、经检验a管中产生 , 由此得出关于水的组成的推论是。(2)、用带火星木条检验b管中气体为的现象是。34. 实验室用如图装置进行二氧化碳的制取和性质实验。
(1)、经检验a管中产生 , 由此得出关于水的组成的推论是。(2)、用带火星木条检验b管中气体为的现象是。34. 实验室用如图装置进行二氧化碳的制取和性质实验。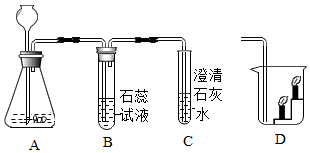 (1)、 A中发生反应的化学方程式是 。(2)、 B中的现象是 。(3)、 用化学方程式解释澄清石灰水变浑浊的原因是 。(4)、 将C中的导气管取出,伸入D中(如图所示),蜡烛由低到高依次熄灭。说明二氧化碳具有的性质是 。35. 如下图所示进行实验。
(1)、 A中发生反应的化学方程式是 。(2)、 B中的现象是 。(3)、 用化学方程式解释澄清石灰水变浑浊的原因是 。(4)、 将C中的导气管取出,伸入D中(如图所示),蜡烛由低到高依次熄灭。说明二氧化碳具有的性质是 。35. 如下图所示进行实验。 (1)、 实验1:如图所示,向盛有的软塑料瓶中倒入三分之一体积的澄清石灰水,旋紧瓶盖后振荡,观察到的现象是。(2)、 实验2:实验中,观察到U型管中液面a低于液面b,其原因用化学方程式表示为。36. 根据下图所示实验回答问题。
(1)、 实验1:如图所示,向盛有的软塑料瓶中倒入三分之一体积的澄清石灰水,旋紧瓶盖后振荡,观察到的现象是。(2)、 实验2:实验中,观察到U型管中液面a低于液面b,其原因用化学方程式表示为。36. 根据下图所示实验回答问题。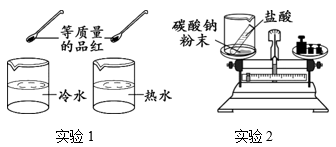 (1)、 实验1,品红在热水中扩散比冷水中快,说明影响分子运动速率的因素是。(2)、 用实验2不能验证质量守恒定律,因为装置不密闭,盐酸与碳酸钠粉末反应后生成逸散到空气中,未称量质量。37. 根据下图所示实验回答问题。
(1)、 实验1,品红在热水中扩散比冷水中快,说明影响分子运动速率的因素是。(2)、 用实验2不能验证质量守恒定律,因为装置不密闭,盐酸与碳酸钠粉末反应后生成逸散到空气中,未称量质量。37. 根据下图所示实验回答问题。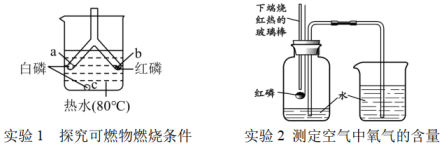
已知:白磷和红磷的着火点分别为40℃、240℃。
(1)、 实验1,a处白磷燃烧,b处红磷不燃烧,结论是。(2)、 实验1,能验证可燃物燃烧需要与接触的现象是。(3)、实验2,在250mL集气瓶中加入50mL水,用红热的玻璃棒引燃红磷,待装置冷却后,测得集气瓶中水的体积为91mL,则空气中氧气的含量为(写出计算式即可)。(4)、实验2,集气瓶中加入50mL水的作用是。38. 硬水加热时易产生水垢,很多工业用水需要对硬水进行软化处理。小组同学利用1.5%的肥皂水比较水的硬度。【查阅资料】硬水含较多可溶性钙、镁化合物;软水不含或含较少可溶性钙、镁化合物。
【查阅资料】硬水含较多可溶性钙、镁化合物;软水不含或含较少可溶性钙、镁化合物。
Ⅰ.探究水的硬度、肥皂水的用量与产生泡沫量的关系
【进行实验】向蒸馏水中加入CaCl2和MgCl2的混合溶液,配制两种不同硬度的硬水。
用蒸馏水和两种硬水完成三组实验,记录如表:组别 第1组 第2组 第3组 实验操作 
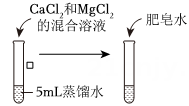
实验序号 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ 混合溶液用量/滴 0 0 0 1 x 1 2 2 2 肥皂水用量/滴 5 10 20 5 10 20 5 10 20 产生泡沫量 少 多 很多 无 少 多 无 无 少 【解释与结论】
(1)、 对比②和⑧可知,肥皂水能区分软水和硬水,依据的现象是。(2)、 设计第2组实验时,为控制水的硬度相同,⑤中x应为。(3)、 第2组实验的目的是。(4)、 由上述三组实验得到的结论是。(5)、Ⅱ.比较不同水样的硬度【进行实验】用四种水样完成实验,记录观察到泡沫产生时所需肥皂水的用量。
实验操作
水样
肥皂水用量/滴
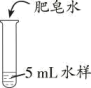
市售纯净水
2
煮沸后的自来水
6
自来水
9
湖水
14
【解释与结论】硬度最大的水样是。
(6)、继续实验,发现山泉水的硬度大于自来水的硬度,其实验方案为。39. 火力发电厂的烟气中含有大量氮氧化物,排放前需进行处理,主要反应之一为。若吸收23kgNO2 , 计算生成N2的质量(写出过程及结果)。