吉林省长春市宽城区2023-2024学年九年级上学期期末化学试题
试卷更新日期:2024-01-12 类型:期末考试
一、选择题(每小题只有一个选项符合题意。每小题 1 分,共10分)
-
1. 对蜡烛及其燃烧的探究活动中,下列说法错误的是( )A、石蜡“质软”这一性质属于物理性质 B、“石蜡熔化”属于物理变化 C、“能使澄清的石灰水变浑浊”属于CO₂的化学性质 D、“石蜡受热形成蒸气”属于化学变化2. 二百多年前拉瓦锡用定量的方法研究了空气的成分,后来人们又用实验方法精确地测定了空气的成分。其中约占空气体积78%的气体是( )A、氧气 B、氮气 C、二氧化碳 D、稀有气体3. 关于化学药品的“取用”和“存放”操作中,下列图示正确的是( )
 A、①③④ B、②④⑥ C、③④⑤ D、③④⑥4. 味精的主要成分为谷氨酸钠(C3H8NNaO4)和NaCl,可用于食品增鲜,但加热至 120℃以上时,便会失去鲜味。下列说法正确的是( )A、谷氨酸钠中含有5个元素 B、NaCl由钠原子和氯原子构成 C、应在菜或汤即将出锅时加入味精 D、谷氨酸钠中碳、氢元素的质量比为5:85. 分析推理能力是必备的科学素养,下列推理正确的是( )A、两种粒子属于同一种元素,则它们的原子核中质子数一定相同 B、两种粒子含有的质子数相同则它们一定属于同一种元素 C、物质中只含有一种元素,则这种物质一定是纯净物 D、化学变化中构成物质的分子改变,则变化前后原子的种类也一定改变6. 消防用自动感温喷淋头结构如下图所示。当喷淋头附近温度升高到喷淋头的设定值时,丙三醇将热敏玻璃球胀破,喷淋头自动喷水灭火。
A、①③④ B、②④⑥ C、③④⑤ D、③④⑥4. 味精的主要成分为谷氨酸钠(C3H8NNaO4)和NaCl,可用于食品增鲜,但加热至 120℃以上时,便会失去鲜味。下列说法正确的是( )A、谷氨酸钠中含有5个元素 B、NaCl由钠原子和氯原子构成 C、应在菜或汤即将出锅时加入味精 D、谷氨酸钠中碳、氢元素的质量比为5:85. 分析推理能力是必备的科学素养,下列推理正确的是( )A、两种粒子属于同一种元素,则它们的原子核中质子数一定相同 B、两种粒子含有的质子数相同则它们一定属于同一种元素 C、物质中只含有一种元素,则这种物质一定是纯净物 D、化学变化中构成物质的分子改变,则变化前后原子的种类也一定改变6. 消防用自动感温喷淋头结构如下图所示。当喷淋头附近温度升高到喷淋头的设定值时,丙三醇将热敏玻璃球胀破,喷淋头自动喷水灭火。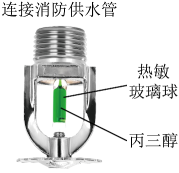
下列说法不正确的是
A、热敏玻璃球能迅速将外界的热量传递给丙三醇 B、玻璃球胀破的原因是丙三醇分子间的间隔变大 C、喷水灭火的原理是水降低了可燃物的着火点 D、日常生活中应避免热源靠近自动感温喷淋头7. 生活中燃料的变迁经历了“木柴→煤炭→煤气→天然气”等过程。下列说法正确的是( )A、能量转化:燃料燃烧时将化学能转化为内能 B、科学态度:上述燃料均属于可再生能源,可以任意使用 C、化学观念:上述燃料均含有碳元素,完全燃烧后均能生成空气污染物二氧化碳 D、科学思维:上述燃料燃烧时均有发光、放热现象,所以有发光、放热现象的一定是燃烧8. 以物质类别为横坐标,以化合价为纵坐标绘制的图像叫“类价二维图”。如图是碳元素的类价二维图,下列说法错误的是( ) A、a对应的物质所属类别是单质 B、b表示的物质具有毒性 C、c转化为 d 可通过化合反应 D、d表示的物质中碳元素呈+2 价9. 下列实验操作方法错误的是( )
A、a对应的物质所属类别是单质 B、b表示的物质具有毒性 C、c转化为 d 可通过化合反应 D、d表示的物质中碳元素呈+2 价9. 下列实验操作方法错误的是( )实验目的
操作方法
A
鉴别CO和CO2
将气体分别通入澄清的石灰水中
B
除去氮气中的少氧氧气
将气体通过灼热的木炭
C
检验二氧化碳是否集满
将燃着的木条放在集气瓶口处
D
区分水和过氧化氢溶液
取样,分别加入少量 MnO2
A、A B、B C、C D、D10. “控制变量法”是化学学习中的重要方法。下列实验方案的设计中能达到目的的是( )A、 比较温度对微粒运动速率的影响
B、
比较温度对微粒运动速率的影响
B、 比较空气与呼出气体中氧气含量
C、
比较空气与呼出气体中氧气含量
C、 探究分子的运动
D、
探究分子的运动
D、 验证二氧化锰是过氧化氢分解的催化剂
验证二氧化锰是过氧化氢分解的催化剂
二、非选择题(每空1分,共 40分)
-
11. 在联合国“国际青年化学家元素周期表”中,我国化学家蒋雪峰教授被选为硫元素“代言人”。请用化学用语回答下列问题。(1)、硫元素的符号;(2)、两个硫原子;(3)、二氧化硫分子。12. “嫦娥五号”月球采样返回,“天问一号”成功抵达火星,标志着我国航天事业取得突破性进展。(1)、月壤含有可作为核聚变燃料的氦-3等物质。如图为氦元素在周期表中的部分信息。氦-3 原子内质子数与中子数之和为3,则其所含中子数为。
 (2)、着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,请写出该反应的化学方程式;此反应与电解水反应相似,也可证明水由元素组成。(3)、火星拥有丰富的二氧化碳资源。火星低层大气的主要成分如下表:
(2)、着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,请写出该反应的化学方程式;此反应与电解水反应相似,也可证明水由元素组成。(3)、火星拥有丰富的二氧化碳资源。火星低层大气的主要成分如下表:气体成分
CO2
N2
Ar
O2
其他
体积分数/%
95.32
2.7
1.6
0.13
0.25
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是;
②若为满足人类未来在火星上生活,下列研究设想合理的是(填代号)。
A.将CO2转化为 O2 , 提高 O2含量
B.将 CO2分解转化为N2 , 提高 N2含量
C.寻找水的存在和开发水循环技术
13. 净水厂净水操作主要流程如下图所示,回答下列问题。 (1)、操作X的名称是 , 试剂A的名称是;(2)、输送到用户家中的水从物质的类别上看属于;(3)、2023 年 3 月 22~28 日是第三十六届“中国水周”,主题为“强化依法治水,携手共护母亲河”。下列有关水的说法和做法正确的是____(填代号)。A、农业要禁用化肥农药 B、工业废水处理达标后排放 C、节水中国,你我同行 D、生活污水直接排放 E、复苏河湖生态环境,维护河湖健康生命14. 我国向世界承诺:到2060年实现“碳中和”,达到相对“零排放”。(1)、化石燃料燃烧会释放CO2 , 请写出天然气燃烧的化学方程式 , 实现“碳中和”有利于缓解的环境问题是。(2)、我国科学家使用纳米纤维作催化剂实现了CO2转化为甲醇(CH3OH ),并于2023 年2月首次投产,反应的微观原理如下图所示,下列说法错误的是____。
(1)、操作X的名称是 , 试剂A的名称是;(2)、输送到用户家中的水从物质的类别上看属于;(3)、2023 年 3 月 22~28 日是第三十六届“中国水周”,主题为“强化依法治水,携手共护母亲河”。下列有关水的说法和做法正确的是____(填代号)。A、农业要禁用化肥农药 B、工业废水处理达标后排放 C、节水中国,你我同行 D、生活污水直接排放 E、复苏河湖生态环境,维护河湖健康生命14. 我国向世界承诺:到2060年实现“碳中和”,达到相对“零排放”。(1)、化石燃料燃烧会释放CO2 , 请写出天然气燃烧的化学方程式 , 实现“碳中和”有利于缓解的环境问题是。(2)、我国科学家使用纳米纤维作催化剂实现了CO2转化为甲醇(CH3OH ),并于2023 年2月首次投产,反应的微观原理如下图所示,下列说法错误的是____。 A、甲、乙、丙、丁都是由分子构成的物质 B、参加反应的甲与乙的分子个数比为1:1 C、反应后生成的丙是一种氧化物 D、丁物质由两个氢原子和一个氧原子构成(3)、下列措施有利于实现“碳中和”的是____。A、大量燃烧化石燃料 B、植树造林,增大绿化面积 C、利用化学技术捕捉CO2 并转化 D、开发、利用清洁能源15. 小明用如图所示装置测定空气中氧气的含量。集气瓶的容积为 350mL,实验时先在集气瓶中加入50mL水。
A、甲、乙、丙、丁都是由分子构成的物质 B、参加反应的甲与乙的分子个数比为1:1 C、反应后生成的丙是一种氧化物 D、丁物质由两个氢原子和一个氧原子构成(3)、下列措施有利于实现“碳中和”的是____。A、大量燃烧化石燃料 B、植树造林,增大绿化面积 C、利用化学技术捕捉CO2 并转化 D、开发、利用清洁能源15. 小明用如图所示装置测定空气中氧气的含量。集气瓶的容积为 350mL,实验时先在集气瓶中加入50mL水。 (1)、用弹簧夹夹紧橡皮管,点燃燃烧匙内足量的红磷后,立即伸入集气瓶中并把塞子塞紧,瓶内可观察到的现象为。(2)、待红磷熄灭并冷却后打开弹簧夹,最终集气瓶中水的体积大约为mL,说明实验成功。(3)、下列有关实验的说法中,正确的是____(填代号)。A、实验过程中可以不使用弹簧夹 B、燃烧匙内的红磷可以换成木炭 C、该实验可以说明氮气难溶于水 D、该实验可以说明空气是混合物16. 同学们学习了“燃烧与灭火”后,设计并完成了如图所示实验,探究灭火的原理。
(1)、用弹簧夹夹紧橡皮管,点燃燃烧匙内足量的红磷后,立即伸入集气瓶中并把塞子塞紧,瓶内可观察到的现象为。(2)、待红磷熄灭并冷却后打开弹簧夹,最终集气瓶中水的体积大约为mL,说明实验成功。(3)、下列有关实验的说法中,正确的是____(填代号)。A、实验过程中可以不使用弹簧夹 B、燃烧匙内的红磷可以换成木炭 C、该实验可以说明氮气难溶于水 D、该实验可以说明空气是混合物16. 同学们学习了“燃烧与灭火”后,设计并完成了如图所示实验,探究灭火的原理。实验方法:点燃 3 支蜡烛,在其中一支蜡烛上罩一个烧杯;将另外两支蜡烛分别放在两个烧杯中,然后向一个烧杯中加入适量的碳酸钠和稀盐酸。
 (1)、实验现象:Ⅱ中蜡烛正常燃烧,I和Ⅲ中蜡烛熄灭,Ⅲ中的实验现象还有。(2)、实验结论:由该实验得出灭火的原理是。(3)、反思:Ⅲ中的实验操作可能造成的后果是。17. 在分组实验课上,请你参与完成下列实验活动。(1)、选择方案:实验室可提供三种制取氧气的方案。
(1)、实验现象:Ⅱ中蜡烛正常燃烧,I和Ⅲ中蜡烛熄灭,Ⅲ中的实验现象还有。(2)、实验结论:由该实验得出灭火的原理是。(3)、反思:Ⅲ中的实验操作可能造成的后果是。17. 在分组实验课上,请你参与完成下列实验活动。(1)、选择方案:实验室可提供三种制取氧气的方案。A.加热高锰酸钾 B.加热混有二氧化锰的氯酸钾 C.用二氧化锰催化分解过氧化氢
请写出你所选择的方案对应的化学反应方程式 , 其基本反应类型属于。
(2)、 进行实验:小组决定选用 A 方案,完成如下任务:①小明负责选择仪器。除铁架台、带有导管的橡胶塞、水槽、玻璃片、试管,还应选择(填仪器名称)。
②你负责用排水法收集氧气。开始收集的时机是 , 你收集到了两瓶气体,均呈红色。实验结束,整理实验台。
(3)、反思与改进:实验过程存在不足,请提出 条改进意见。18. 通常状况下,CO2能溶于水(体积比1:1),CO2能否用排水法收集?同学们利用如下图所示的两套装置进行深入探究。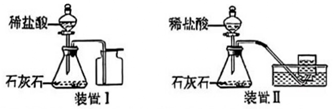 (1)、【定性实验】
(1)、【定性实验】按图实验后,装置Ⅱ水槽中的液体应该呈酸性,作出此猜想的原因可用化学方程式表示为;
(2)、取几次实验后的液体样品滴加紫色石蕊试液,均无明显变色现象,其可能的原因是:;(3)、CO2从水面逸出的速率远比其溶解和与水反应的速率。(4)、【定量实验】采用数字化实验测定排水法和向上排空气法收集的CO2纯净度的差异。
测出 CO2含量
结论
排空气法
69%
排水法收集到的CO2更纯净
排水法
80%
通过实验数据可知,可以使用排水法收集 CO2。
【反思拓展】
要全面、多角度看问题。
通常状况下 SO2是无色有刺激性气味的有毒气体,密度大于空气,易溶于水(体积比1:40)且能与水反应。综合分析,你认为SO2可否用排水法收集?。
19. 同学们在实验室中进行“人体吸入的空气和呼出气体成分”的探究。
【猜想与假设】
猜想Ⅰ.吸入空气中O2含量比呼出气体中O2含量高
猜想Ⅱ.吸入空气中CO2含量比呼出气体中CO2含量低
【实验与结论】
(1)、按图1所示完成实验。能说明猜想Ⅰ成立的实验现象是。(2)、【进行实验】用图2装置完成实验。
实验步骤
实验操作
实验现象
①
在饮料瓶中加水至没过长吸管底端,塞好瓶塞,对着短吸管缓慢吹气
水从长吸管一端流出
②
将装置内的水换成澄清石灰水,从短吸管端连续吸气10秒
澄清石灰水无明显变化
③
倒掉瓶中液体并清洗干净,重新加入等量的澄清石灰水,然后进行了一个操作
澄清石灰水变浑浊
在步骤③后,小明继续吹气一段时间后浑浊的石灰水又变澄清。于是他将瓶中重新加入等体积的石灰水,多次进行吹气实验,结果记录如下:
实验编号
石灰水浓度
持续吹气时间
实验现象
3-1
0.16%
30 秒
澄清石灰水变浑浊
3-2
0.16%
2分钟
澄清石灰水先变浑浊,后又变澄清
3-3
0.08%
30 秒
澄清石灰水先变浑浊,后又变澄清
3-4
0.08%
2分钟
澄清石灰水先变浑浊,后又变澄清
【解释与结论】
步骤①的作用是;
(3)、步骤③中进行的一个操作是:;(4)、能证明猜想Ⅱ成立的实验现象是;(5)、能说明石灰水重新变澄清与石灰水浓度有关的实验是(填实验编号)。(6)、【反思与评价】在步骤③后,有同学观察到浑浊的石灰水又变澄清,而有的同学却未观察到,产生现象差异的可能原因是(答1条即可)。
20. 为测定一份含杂质的石灰石样品中碳酸钙的质量分数(杂质不溶于水且不与盐酸反应),兴趣小组的同学进行了如下图所示的实验,请回答下列问题。 (1)、发生反应的化学方程式为;(2)、反应中产生二氧化碳的质量为;(3)、请列出根据二氧化碳的质量求解参加反应的碳酸钙质量(x)的比例式 , 解得x=20g;(4)、经实验和计算,测得该石灰石样品中碳酸钙的质量分数是。
(1)、发生反应的化学方程式为;(2)、反应中产生二氧化碳的质量为;(3)、请列出根据二氧化碳的质量求解参加反应的碳酸钙质量(x)的比例式 , 解得x=20g;(4)、经实验和计算,测得该石灰石样品中碳酸钙的质量分数是。