吉林省长春市二道区2023-2024学年九年级上学期12月期末化学试题
试卷更新日期:2024-01-12 类型:期末考试
一、选择题(共10分
-
1. 下列过程中涉及物质发生化学变化的是( )A、积雪融化 B、粮食酿酒 C、干冰升华 D、氧气液化2. 空气成分中含量最多的气体是( )A、二氧化碳 B、氢气 C、氮气 D、氧气3. 下列物质中,由原子直接构成的是( )A、氨气 B、氯化钠 C、金刚石 D、水4. 下列物质在氧气中燃烧,产生刺激性气味的是( )A、红磷 B、硫 C、木炭 D、铁丝5. 实验操作应严谨规范。下列实验操作正确的是( )A、
 读取液体体积
B、
读取液体体积
B、 检查装置气密性
C、
检查装置气密性
C、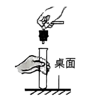 连接仪器
D、
连接仪器
D、 熄灭酒精灯
6. 下列做法不正确的是( )A、电器着火,用水灭火 B、低碳生活,绿色出行 C、植树造林,防沙降尘 D、生活垃圾,分类处理7. 下列涉及化学学科观点的说法,错误的是( )A、微粒观:一氧化碳分子是由碳原子和氧原子构成 B、元素观:由同种元素组成的物质一定是单质 C、分类观:空气和矿泉水都属于混合物 D、守恒观:化学反应前后各原子数目保持不变8. 如图是O2与其他物质之间的转化关系(“→”表示物质之间可发生转化,部分物质已省略),下列说法正确的是( )
熄灭酒精灯
6. 下列做法不正确的是( )A、电器着火,用水灭火 B、低碳生活,绿色出行 C、植树造林,防沙降尘 D、生活垃圾,分类处理7. 下列涉及化学学科观点的说法,错误的是( )A、微粒观:一氧化碳分子是由碳原子和氧原子构成 B、元素观:由同种元素组成的物质一定是单质 C、分类观:空气和矿泉水都属于混合物 D、守恒观:化学反应前后各原子数目保持不变8. 如图是O2与其他物质之间的转化关系(“→”表示物质之间可发生转化,部分物质已省略),下列说法正确的是( ) A、转化①:反应前后氧元素的化合价未发生改变 B、转化②:加入MnO2会使产生O2的质量增加 C、转化③:只有通过氢气的燃烧才能实现 D、转化④:若该反应是分解反应,X中一定含有氧元素9. 下列有关实验操作“先”与“后”的顺序,错误的是( )A、组装仪器时,一般遵循的原则是从左到右,先下后上 B、用滴管吸取液体时,先在空气中挤压胶帽排出空气,后伸入液体中吸取液体 C、实验室制取气体时,应先装入药品,后检查装置的气密性 D、加热试管中的固体时,应先使试管底部均匀受热,后固定在药品部位加热10. 将看不见的变化转换成看得见的变化是化学中研究物质的常用方法。如在验证二氧化碳能与水发生化学反应生成酸性物质的实验中,其实验过程如图所示:
A、转化①:反应前后氧元素的化合价未发生改变 B、转化②:加入MnO2会使产生O2的质量增加 C、转化③:只有通过氢气的燃烧才能实现 D、转化④:若该反应是分解反应,X中一定含有氧元素9. 下列有关实验操作“先”与“后”的顺序,错误的是( )A、组装仪器时,一般遵循的原则是从左到右,先下后上 B、用滴管吸取液体时,先在空气中挤压胶帽排出空气,后伸入液体中吸取液体 C、实验室制取气体时,应先装入药品,后检查装置的气密性 D、加热试管中的固体时,应先使试管底部均匀受热,后固定在药品部位加热10. 将看不见的变化转换成看得见的变化是化学中研究物质的常用方法。如在验证二氧化碳能与水发生化学反应生成酸性物质的实验中,其实验过程如图所示:
该实验验证了二氧化碳能与水反应生成酸性物质;在验证的过程中,与下列证据无关的是( )
A、能使紫色石蕊变红的物质都是酸性物质,如醋酸、盐酸等 B、在通常状况下,二氧化碳密度大于空气的密度 C、水不能使石蕊变红,二氧化碳也不能使石蕊变红 D、水和二氧化碳接触后能使石蕊变红,说明有酸性物质生成二、非选择题(共40分
-
11. 用化学用语回答问题:(1)、铝元素。(2)、两个硫原子。(3)、3个氢分子。12. 氟及其化合物常运用于原子弹制造、航天工业等领域。图1是氟元素在元素周期表中的信息。请回答下列问题:
 (1)、氟元素的原子序数为。(2)、氟元素的相对原子质量为。(3)、图2为氟分子的微观模型图,请写出氟气的化学式。
(1)、氟元素的原子序数为。(2)、氟元素的相对原子质量为。(3)、图2为氟分子的微观模型图,请写出氟气的化学式。 13. 尿素是一种常用的化肥。请阅读标签并回答下列问题:
13. 尿素是一种常用的化肥。请阅读标签并回答下列问题: (1)、尿素由种元素组成。(填数字)(2)、尿素中碳元素和氧元素的质量比是。(3)、从标签上看,尿素可能具有的物理性质是。14. “水是生存之本,文明之源”,请回答下列有关水的问题:(1)、爱水:为了人类和社会经济的可持续发展,我们必须爱护水资源,一方面要 , 另一方面要防治水体污染。(2)、净水:自来水厂常利用活性炭的性,除去水中的色素和异味。(3)、探水:电解水实验可以证明水的组成,请写出该反应的化学方程式。(4)、用水:水在化学实验中有多种用途,图中瓶底放水的目的是防止。
(1)、尿素由种元素组成。(填数字)(2)、尿素中碳元素和氧元素的质量比是。(3)、从标签上看,尿素可能具有的物理性质是。14. “水是生存之本,文明之源”,请回答下列有关水的问题:(1)、爱水:为了人类和社会经济的可持续发展,我们必须爱护水资源,一方面要 , 另一方面要防治水体污染。(2)、净水:自来水厂常利用活性炭的性,除去水中的色素和异味。(3)、探水:电解水实验可以证明水的组成,请写出该反应的化学方程式。(4)、用水:水在化学实验中有多种用途,图中瓶底放水的目的是防止。 15. 为探究分子运动现象,兴趣小组进行了以下实验。(1)、图1是按课本进行的实验,一段时间后,A烧杯中的溶液由无色变为色;通过该实验现象可验证哪种分子在不断运动?。
15. 为探究分子运动现象,兴趣小组进行了以下实验。(1)、图1是按课本进行的实验,一段时间后,A烧杯中的溶液由无色变为色;通过该实验现象可验证哪种分子在不断运动?。 (2)、图2与图1相比,图2优点是(写一条即可)。
(2)、图2与图1相比,图2优点是(写一条即可)。 16. 化学与生活、生产息息相关,请回答以下问题:(1)、全脂高钙奶粉中的“钙”是指(选填“分子”“原子”或“元素”)。(2)、“84”消毒液可用于防疫,其主要成分是次氯酸钠(NaClO),次氯酸钠中氯元素的化合价为。17. 从多角度认识化学反应,有助于形成系统思维。如图是甲烷燃烧的微观示意图,请回答下列问题:
16. 化学与生活、生产息息相关,请回答以下问题:(1)、全脂高钙奶粉中的“钙”是指(选填“分子”“原子”或“元素”)。(2)、“84”消毒液可用于防疫,其主要成分是次氯酸钠(NaClO),次氯酸钠中氯元素的化合价为。17. 从多角度认识化学反应,有助于形成系统思维。如图是甲烷燃烧的微观示意图,请回答下列问题: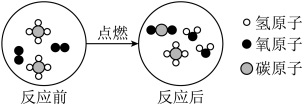 (1)、物质变化角度
(1)、物质变化角度从微观角度分析,反应后有(填数字)种分子生成,请写出该反应的化学方程式。
从宏观角度分析,该反应产生了新物质,为证明甲烷燃烧有二氧化碳生成,接下来的实验操作是:点燃从导管导出的纯净的甲烷气体,。
(2)、能量变化角度甲烷燃烧实现了从到热能和光能的转化。
(3)、定量分析角度请根据如图信息,计算参加反应的
 和
和 的质量之比是。18. 如图是实验室制取气体并验证气体化学性质的实验装置,请回答有关问题。
的质量之比是。18. 如图是实验室制取气体并验证气体化学性质的实验装置,请回答有关问题。 (1)、玻璃仪器①的名称是。(2)、实验室若用装置B制取气体,向长颈漏斗中加液体时液面高度至少应该在处。(填字母)(3)、某兴趣小组的同学连接B、F装置进行实验。若实验过程中F装置中蜡烛燃烧更剧烈,则装置B中反应的化学方程式为。(4)、加热高锰酸钾制取并收集一瓶较纯净的氧气,可选择的装置组合是(填字母)。19. 某小组以“探究燃烧的奥秘”为主题开展了项目式学习。(1)、【任务一】了解燃烧
(1)、玻璃仪器①的名称是。(2)、实验室若用装置B制取气体,向长颈漏斗中加液体时液面高度至少应该在处。(填字母)(3)、某兴趣小组的同学连接B、F装置进行实验。若实验过程中F装置中蜡烛燃烧更剧烈,则装置B中反应的化学方程式为。(4)、加热高锰酸钾制取并收集一瓶较纯净的氧气,可选择的装置组合是(填字母)。19. 某小组以“探究燃烧的奥秘”为主题开展了项目式学习。(1)、【任务一】了解燃烧通常情况下,可燃物与氧气发生的一种发光、放热的剧烈的氧化反应叫做燃烧。请写出木炭在氧气中充分燃烧的化学方程式。
(2)、【任务二】探究燃烧【查阅资料】①白磷的着火点为40℃,红磷的着火点为240℃;
②磷燃烧产生的白烟会刺激人的呼吸道。
同学们,设计了如图1所示的实验装置,请回答下列问题:
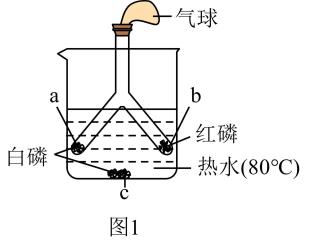
图1中a处的白磷燃烧,b处的红磷不燃烧,说明可燃物燃烧的条件之一是。
通过对比图1中(填字母)处的现象,可得出燃烧需要可燃物与氧气接触。
(3)、【任务三】再识燃烧①实验1:将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中(见图2),发现镁条剧烈燃烧,发出白光,放热,产生一种白色粉末和一种黑色粉末。

查阅资料,同学们了解到镁条在二氧化碳中燃烧后产生的白色粉末是氧化镁,则产生的黑色粉末中一定含有的元素是。
通过该实验,同学们对燃烧有了新的认识,燃烧是否一定需要氧气?
②实验2:同学们设计了图3装置来进行实验。在装置气密性良好的前提下,利用高能激光笔(照射时的光可产生高温)持续照射燃烧匙上足量的木炭,使其燃烧,同时利用传感器对该密闭体系中木炭燃烧到熄灭过程中氧气的浓度变化进行了记录(见图4):
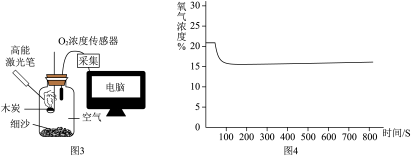
结合图3、图4分析:可燃物在温度达到着火点且与氧气接触时,(选填“一定”或“不一定”)会产生燃烧。
已知甲烷、乙醇、木炭等含碳元素的物质在浓度较低的氧气中燃烧,会产生一氧化碳气体。请思考足量的木炭在充满氧气的密闭容器中燃烧,待其熄灭后,瓶内含有的气体有。
(4)、【任务四】防控燃烧在加油站、油库、煤矿矿井内,需要张贴的图标是____(填字母序号)。
A、 B、
B、 C、
C、 D、
D、 20. 我国力争在2060年前实现“碳中和”。实现“碳中和”可采取如下措施:(1)、“碳”减排:控制二氧化碳的排放,主要是为了减缓____(填字母)。A、温室效应加剧 B、白色污染 C、空气污染(2)、“碳”捕捉:实际生产中常采用足量的氢氧化钠溶液来“捕捉”二氧化碳,其原理如下:CO2+2NaOH=Na2CO3+X,其中X的化学式为。(3)、 “碳”利用:本次杭州亚运会的主火炬所用燃料是首次采用废碳再生的甲醇(CH₃OH),二氧化碳转化为甲醇的原理是:CO2+3H2CH3OH+H2O。若要制得64t甲醇,请计算理论上需要多少吨二氧化碳? (计算过程及结果请在答题卡上补充完整)
20. 我国力争在2060年前实现“碳中和”。实现“碳中和”可采取如下措施:(1)、“碳”减排:控制二氧化碳的排放,主要是为了减缓____(填字母)。A、温室效应加剧 B、白色污染 C、空气污染(2)、“碳”捕捉:实际生产中常采用足量的氢氧化钠溶液来“捕捉”二氧化碳,其原理如下:CO2+2NaOH=Na2CO3+X,其中X的化学式为。(3)、 “碳”利用:本次杭州亚运会的主火炬所用燃料是首次采用废碳再生的甲醇(CH₃OH),二氧化碳转化为甲醇的原理是:CO2+3H2CH3OH+H2O。若要制得64t甲醇,请计算理论上需要多少吨二氧化碳? (计算过程及结果请在答题卡上补充完整)