广东省惠州市惠阳区重点中学2023-2024学年九年级上学期期中化学试题
试卷更新日期:2024-01-05 类型:期中考试
一、选择题:本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1. 下列成语涉及的变化主要为化学变化的是( )A、滴水成冰 B、星火燎原 C、积土成山 D、沙里淘金2. 黑乎乎的石油可以变成绚丽多彩的衣物。下面提出的问题中不属于化学研究范畴的是( )A、石油的组成成分是什么 B、石油通过怎样的变化才能变成做衣物的纤维 C、石油可以燃烧,那么由它制成的衣物能否燃烧 D、通过什么方法从地下得到石油3. 下列用途利用了物质物理性质的是( )A、木炭用作吸附剂 B、木炭用作燃料 C、氧气用作助燃剂 D、氮气用作保护气4. 下列实验操作正确的是( )A、
 B、
B、 C、
C、 D、
D、 5. “小马虎”小明,下面是从他的实验报告中摘录的实验现象,你认为描述正确的是A、红磷在空气中燃烧产生大量的白雾 B、木炭在氧气中燃烧发出淡蓝色火焰 C、铁丝在氧气中剧烈燃烧,火星四射 D、硫在氧气中燃烧生成二氧化硫气体6. 空气是多种气体的混合物,下列生产生活中用到的气体来自空气的是( )A、做火箭燃料用到的液氢 B、制硝酸用到的二氧化氮 C、炼铁用到的一氧化碳 D、填充气球用到的氦气7. “掬水月在手,弄花香满衣”。“弄花香满衣”是因为( )A、分子之间有间隔 B、分子的体积很小 C、分子在不断运动 D、分子的质量很小8. 原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )A、中子数为145 B、核电荷数为239 C、质子数为94 D、核外电子数为949. 将质量完全相等的氯酸钾固体分别装入、、三支试管中,向中再加入二氧化锰,向中再加入高锰酸钾,分别加热三支试管,产生氧气质量最多和产生氧气速率最慢的分别是( )A、、 B、、 C、、 D、、10. 铪可用作航天材料,在元素周期表中的信息如图所示。下列有关铪元素的说法正确的是( )
5. “小马虎”小明,下面是从他的实验报告中摘录的实验现象,你认为描述正确的是A、红磷在空气中燃烧产生大量的白雾 B、木炭在氧气中燃烧发出淡蓝色火焰 C、铁丝在氧气中剧烈燃烧,火星四射 D、硫在氧气中燃烧生成二氧化硫气体6. 空气是多种气体的混合物,下列生产生活中用到的气体来自空气的是( )A、做火箭燃料用到的液氢 B、制硝酸用到的二氧化氮 C、炼铁用到的一氧化碳 D、填充气球用到的氦气7. “掬水月在手,弄花香满衣”。“弄花香满衣”是因为( )A、分子之间有间隔 B、分子的体积很小 C、分子在不断运动 D、分子的质量很小8. 原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )A、中子数为145 B、核电荷数为239 C、质子数为94 D、核外电子数为949. 将质量完全相等的氯酸钾固体分别装入、、三支试管中,向中再加入二氧化锰,向中再加入高锰酸钾,分别加热三支试管,产生氧气质量最多和产生氧气速率最慢的分别是( )A、、 B、、 C、、 D、、10. 铪可用作航天材料,在元素周期表中的信息如图所示。下列有关铪元素的说法正确的是( )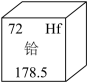 A、核电荷数为72 B、属于非金属元素 C、相对原子质量为 178.5g D、二氧化铪的化学式为O2Hf11. 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆代表纯净物,下列选项正确的是( )
A、核电荷数为72 B、属于非金属元素 C、相对原子质量为 178.5g D、二氧化铪的化学式为O2Hf11. 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆代表纯净物,下列选项正确的是( ) A、①单质③氧化物 B、②化合物④氧化物 C、①单质③化合物 D、②含氧化合物④氧化物12. 英国科学家法拉第曾用蜡烛(主要成分为石蜡)做过一个有趣的“母子火焰”实验,如图所示。下列有关分析错误的是( )
A、①单质③氧化物 B、②化合物④氧化物 C、①单质③化合物 D、②含氧化合物④氧化物12. 英国科学家法拉第曾用蜡烛(主要成分为石蜡)做过一个有趣的“母子火焰”实验,如图所示。下列有关分析错误的是( ) A、母火焰的外焰部分石蜡燃烧充分,无石蜡蒸气 B、若导管太长,石蜡蒸气易冷凝,不能从导管末端导出 C、导管的一端要插入母火焰的中心部位,是因为该处氧气充足 D、实验现象说明石蜡的沸点较低,受热易变成气态13. 罗红霉素是某药品的主要成分,下列有关罗红霉素的说法错误的是 ( )A、罗红霉素中氢元素的质量分数最大 B、罗红霉素由碳、氢、氮、氧四种元素组成 C、罗红霉素中氮、氧原子的个数比为2∶15 D、一个罗红霉素分子由41个碳原子、76个氢原子、2个氮原子、15个氧原子构成14. 如图是某元素一种粒子的结构示意图,据此推断下列相关说法中合理的是()
A、母火焰的外焰部分石蜡燃烧充分,无石蜡蒸气 B、若导管太长,石蜡蒸气易冷凝,不能从导管末端导出 C、导管的一端要插入母火焰的中心部位,是因为该处氧气充足 D、实验现象说明石蜡的沸点较低,受热易变成气态13. 罗红霉素是某药品的主要成分,下列有关罗红霉素的说法错误的是 ( )A、罗红霉素中氢元素的质量分数最大 B、罗红霉素由碳、氢、氮、氧四种元素组成 C、罗红霉素中氮、氧原子的个数比为2∶15 D、一个罗红霉素分子由41个碳原子、76个氢原子、2个氮原子、15个氧原子构成14. 如图是某元素一种粒子的结构示意图,据此推断下列相关说法中合理的是() A、该粒子是阴离子 B、该元素原子核内质子数为12 C、该元素在化学反应中不易失去电子 D、该元素原子的最外层上有8个电子15. 下列图像能正确反映对应变化关系的是( )
A、该粒子是阴离子 B、该元素原子核内质子数为12 C、该元素在化学反应中不易失去电子 D、该元素原子的最外层上有8个电子15. 下列图像能正确反映对应变化关系的是( )A
B
C
D




利用红磷燃烧测定空气中氧气的含量
加热氯酸钾和二氧化锰制氧气
用等质量、等浓度的双氧水分别制取氧气
向一定量的二氧化锰固体中加入一定量的过氧化氢溶液
A、A B、B C、C D、D二、非选择题:本题共6个小题,共55分,符号表达式每个2分,其余每空1分。
-
16. 人类的日常生活和工农业生产离不开水。为探究水的组成及变化,某小同学设计下图装置进行电解水实验,先在电解器玻璃管里加满水(含少量硫酸钠),再接通直流电源。回答下列问题:
 (1)、电解时,向水中加入硫酸钠其目的是 , 乙玻璃管中产生气泡的位置在(填“a”“b”或“c”)处。(2)、甲、乙两支玻璃管中生成气体的体积比约为。(3)、切断电源后,用燃着的木条在乙玻璃管尖嘴口检验产生的气体,观察到的现象是。(4)、电解时,水分于分解示意图如下,补全横线上的模型图。
(1)、电解时,向水中加入硫酸钠其目的是 , 乙玻璃管中产生气泡的位置在(填“a”“b”或“c”)处。(2)、甲、乙两支玻璃管中生成气体的体积比约为。(3)、切断电源后,用燃着的木条在乙玻璃管尖嘴口检验产生的气体,观察到的现象是。(4)、电解时,水分于分解示意图如下,补全横线上的模型图。 (5)、电解纯水速率较慢,为探究不同电压和不同浓度NaOH溶液对电解水速率的影响,小组同学进行多次实验,测得产生20mL氢气所需时间如下图:
(5)、电解纯水速率较慢,为探究不同电压和不同浓度NaOH溶液对电解水速率的影响,小组同学进行多次实验,测得产生20mL氢气所需时间如下图:
①电解溶质质量分数为5%的NaOH溶液时,改变电压对电解水速率的影响。
②上述实验中,电解水速率最快的条件是。
17. 化学用语是学习化学的基本工具。(1)、请用化学用语填空:①2个汞原子;
②2个镁离子;
③四氧化三铁;
④标出二氧化氮中氮元素的化合价;
⑤地壳中含量最多的金属元素;
⑥生物细胞中含量最多的元素;
⑦两个氮气分子。
(2)、写出下列化学用语中数字“2”的含义:①中“2”表示;
②中“2”表示。
18. 化学是以实验为基础的学科,正确选择实验装置是实验成功的关键。下图所示装置常用于实验室制取气体,请回答下列问题。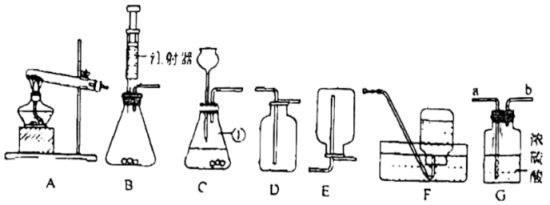 (1)、标号①的仪器名称是。(2)、你认为选用B作发生装置,优点是;请指出装置C中存在的一处错误。(3)、改进上述装置图中存在的错误,并以过氧化氢溶液为原料,在实验室中制取并收集干燥的氧气(可用浓硫酸干燥氧气)。按照要求选择实验装置,连接仪器后,先 , 再装入药品,进行实验。
(1)、标号①的仪器名称是。(2)、你认为选用B作发生装置,优点是;请指出装置C中存在的一处错误。(3)、改进上述装置图中存在的错误,并以过氧化氢溶液为原料,在实验室中制取并收集干燥的氧气(可用浓硫酸干燥氧气)。按照要求选择实验装置,连接仪器后,先 , 再装入药品,进行实验。①所选装置的连接顺序为(从左到右填写装置序号字母)。
②上述方法制氧气的符号表达式为。
③若把G装置中的浓硫酸换成水并盛满,用来收集难溶于水的气体时,气体从(填“a”或“b”)端通入。
(4)、实验室选用分解高锰酸钾制取一瓶较纯净的氧气,选用的收集装置是(填序号),上述方法制氧气的符号表达式为。19. 某化学兴趣小组对实验制取氧气的催化剂展开了探究。请回答下列问题:(1)、【探究一】影响过氧化氢分解速率的因素有哪些?实验数据如下表:
能说明过氧化氢的分解速率与其浓度有关的实验是(填实验序号)。实验
溶液的浓度
溶液的体积
温度
的用量
收集的体积
反应时间
①
5%
1mL
20℃
0.1g
4mL
16s
②
15%
1mL
20℃
0.1g
4mL
6s
③
30%
5mL
35℃
0g
4mL
98min
④
30%
5mL
55℃
0g
4mL
20min
(2)、实验③、④,实验目的是。(3)、为完成上述实验中收集氧气及数据的测定需要用到的部分装置如图所示,与c连接的是(填“a”或“b”)端,进行操作时,集气瓶中未装满水,对实验测量结果(填“会”或“不会”)产生影响。 (4)、兴趣小组探究了不同的金属氧化物对过氧化氢分解速率的影响。他们在等体积的三个锥形瓶中加入40mL5%的溶液,分别加入等量、、CuO后,根据实验数据绘制了产生的氧气体积和时间变化的曲线如图。观察该图回答问题:
(4)、兴趣小组探究了不同的金属氧化物对过氧化氢分解速率的影响。他们在等体积的三个锥形瓶中加入40mL5%的溶液,分别加入等量、、CuO后,根据实验数据绘制了产生的氧气体积和时间变化的曲线如图。观察该图回答问题:
通过该图可得出结论:(写出1条即可)。
(5)、【探究二】二氧化锰粒径大小对氯酸钾分解催化效果的影响。取两份等质量的氯酸钾,分别加入等质量、粒径大小不同的二氧化锰进行加热,用传感器测得固体残留率(反应剩余固体质量与反应前固体质量之比)如图:
该探究中,氯酸钾制取氧气的符号表达式为。 (6)、分析图像,对氯酸钾分解的催化效果更好的为(选填“分析纯”或“纳米”)二氧化锰。20. 某兴趣小组探究分子的特性时做了以下三组实验。已知:碱性溶液能使酚酞变红,而氨水呈碱性,打开盛装浓氨水的试剂瓶时能够闻到强烈刺激性气味。请回答实验中的有关问题:(1)、取上述溶液置于试管中,向其中慢慢滴加氨水,观察到的现象是: , 通过上述实验,得出的结论是。(2)、将烧杯中的酚酞溶液分别倒入A、B两个小烧杯中,另取一个烧杯C,向其中加入约5mL浓氨水。用个大烧杯罩住A、C两个小烧杯,烧杯B置于大烧杯外(如图乙),观察几分钟,烧杯A、B发生的现象分别是 , 这一现象说明 , B烧杯的作用是。
(6)、分析图像,对氯酸钾分解的催化效果更好的为(选填“分析纯”或“纳米”)二氧化锰。20. 某兴趣小组探究分子的特性时做了以下三组实验。已知:碱性溶液能使酚酞变红,而氨水呈碱性,打开盛装浓氨水的试剂瓶时能够闻到强烈刺激性气味。请回答实验中的有关问题:(1)、取上述溶液置于试管中,向其中慢慢滴加氨水,观察到的现象是: , 通过上述实验,得出的结论是。(2)、将烧杯中的酚酞溶液分别倒入A、B两个小烧杯中,另取一个烧杯C,向其中加入约5mL浓氨水。用个大烧杯罩住A、C两个小烧杯,烧杯B置于大烧杯外(如图乙),观察几分钟,烧杯A、B发生的现象分别是 , 这一现象说明 , B烧杯的作用是。 (3)、乙同学将实验进行改进(如图丙)后进行有关分子性质的探究实验:在试管中的滤纸条上相间滴有无色酚酞溶液,试管口塞上一团蘸有浓氨水的棉花,试管中看到的现象是。(4)、丙同学设计实验如图丁所示,在一个玻璃杯中放入约50mL水,向水中放入一大块糖块,在容器外壁沿液面画一条水平线,当糖块消失后,液面比水平线(填“高”“低”或“相平”),这一现象说明了 , 同时还可以说明。21. 请回答下列问题。(1)、(一)水是一种宝贵的自然资源,自来水厂的净水流程如下:
(3)、乙同学将实验进行改进(如图丙)后进行有关分子性质的探究实验:在试管中的滤纸条上相间滴有无色酚酞溶液,试管口塞上一团蘸有浓氨水的棉花,试管中看到的现象是。(4)、丙同学设计实验如图丁所示,在一个玻璃杯中放入约50mL水,向水中放入一大块糖块,在容器外壁沿液面画一条水平线,当糖块消失后,液面比水平线(填“高”“低”或“相平”),这一现象说明了 , 同时还可以说明。21. 请回答下列问题。(1)、(一)水是一种宝贵的自然资源,自来水厂的净水流程如下:
吸附池内常用吸附色素和异味。 (2)、自来水厂常用氯气杀菌消毒,在此过程中发生了反应 , HClO中氯元素的化合价为。(3)、某同学取自来水于试管中,加入适量 , 振荡,发现有较多浮渣产生,说明该自来水属于硬水。(4)、在日常生活中,常采用的方法降低水的硬度。(5)、下列实验能证明水是由氢元素和氧元素组成的是____(填字母序号)。A、氢气在氧气中燃烧 B、水的蒸发 C、水的电解 D、水的净化(6)、(二)已知一般条件下,氧气的密度1.43g/L,空气的密度1.29g/L。
(2)、自来水厂常用氯气杀菌消毒,在此过程中发生了反应 , HClO中氯元素的化合价为。(3)、某同学取自来水于试管中,加入适量 , 振荡,发现有较多浮渣产生,说明该自来水属于硬水。(4)、在日常生活中,常采用的方法降低水的硬度。(5)、下列实验能证明水是由氢元素和氧元素组成的是____(填字母序号)。A、氢气在氧气中燃烧 B、水的蒸发 C、水的电解 D、水的净化(6)、(二)已知一般条件下,氧气的密度1.43g/L,空气的密度1.29g/L。某同学用氯酸钾制取了8g的氧气,则这些氧气的体积是L。若这些氧气来自于空气则需要空气L。
(7)、某原子的核电荷数为26,相对原子质量为56,则它的中子数与电子数之差是。若1个A原子的质量为akg,1个碳12原子(含有6个质子和6个中子)质量为bkg。A原子的相对原子质量为(列出计算式,用含a、b的式子表示)。