吉林省长春市农安县2023-2024学年高二上学期期中考试化学试题
试卷更新日期:2024-01-02 类型:期中考试
一、选择題(每小题仅有一个正确答案,共15个小题,每小题3分)
-
1. 下列应用与盐类水解无关的是( )。A、纯碱溶液去油污 B、明矾做净水剂 C、用氧化铁溶液制氢氧化铁胶体 D、用做沉淀剂,除去溶液中的2. NO和CO都是汽车尾气中的有害物质,它们能缓慢反应生成和 , 为控制汽车尾气污染,下列措施最合理的是( )。A、增大压强 B、降低压强 C、使用催化剂 D、升高反应温度3. 下列各组热化学方程式中,化学反应的前者大于后者的是( )。A、 , B、 , C、 , D、 ,4. 反应在四种不同情况下的反应速率如下。其中表示反应速率最快的是( )。A、 B、 C、 D、5. 25℃时,水的电离达到平衡: , 下列叙述正确的( )。A、将水加热,增大,pH变小 B、向水中加入稀氨水,平衡逆向移动,减小,减小 C、向水中加入少量气体,平衡逆向移动,减小,减小 D、向水中加入少量固体碳酸氢钠,增大,变大6. 反应 , 在密闭容器中投入和的 , 2分钟后NO的物质的量增加了 , 下列说法错误的是( )。A、2分钟末 B、2分钟内的转化率是50% C、 D、2分钟反应放出的热量值等于7. 一定温度下,在容积不变的密闭容器中进行如下可逆反应: , 下列能表明该反应已达到化学平衡状态的是( )。
① ②的体积分数不再变化 ③容器内气体压强不再变化
④键断裂的同时,有键断裂 ⑤混合气体的体积不再变化
A、①②③ B、②④⑤ C、②③ D、③④⑤8. 在相同温度下,的醋酸溶液与的醋酸溶液相比较,下列数值前者大于后者的是( )。A、中和时所需的量 B、电离的程度 C、的物质的量浓度 D、的物质的量9. 某温度下气体反应体系达到化学平衡,平衡常数K= , 恒容时,若温度适当降低,F的浓度增加,下列说法正确的是( )A、该反应的化学方程式为2E(g)+F(g)A(g)+2B(g) B、降低温度,正反应速率增大 C、该反应的焓变为负值 D、增大c(A)、c(B),K增大10. 相同温度下,根据三种酸的电离常数,下列判断正确的是( )。酸
HA
HB
HC
电离常数K
A、三种酸的酸性强弱关系:HA>HB>HC B、相同物质的量浓度的盐溶液、、 , 水解程度最大 C、反应能够发生 D、相同物质的量浓度的盐溶液、、 , pH值依次增大11. 在一密闭容器中的一定量混合气体发生反应:平衡时测得A的浓度为 , 保持温度不变。将容器的容积扩大到原来的两倍。再达到平衡时,A的浓度为。下列有关判断正确的是( )。A、物质B的转化率降低 B、平衡向正反应方向移动 C、 D、物质Z的体积分数增大12. 在3种不同条件下。分别向容积为的恒容密闭容器中充入和 , 发生反应: , 相关条件和数据见表:实验编号
实验Ⅰ
实验Ⅱ
实验Ⅲ
反应温度/℃
700
700
750
达平衡时间/min
40
5
30
平衡时
1.5
1.5
1
化学平衡常数
下列说法正确的是( ).
A、 B、升高温度能加快反应速率的原因是降低了反应的活化能 C、实验Ⅱ比实验Ⅰ达平衡所需时间小的可能原因是使用了催化剂 D、实验Ⅲ达平衡后,恒温下再向容器中通入和 , 平衡正向移动13. 25℃时,若溶液中由水电离产生的 , 则下列说法正确的是( )。A、该溶液中水的电离被促进 B、该溶液中、、、可以大量共存 C、该溶液pH一定为2 D、该溶液一定是碱溶液14. 溶液的pH、体积相同的盐酸和醋酸两种溶液。下列叙述错误的是( )。A、它们分别与足量反应时,放出的一样多 B、它们与完全中和时,醋酸溶液所消耗的多 C、两种溶液中相同 D、分别用水稀释相同倍数时,醋酸溶液中比盐酸溶液中的大15. 已知反应: 。某温度下,将置于密闭容器中,一定时间后反应达到平衡。则下列说法正确的是( )。 A、图甲中表示A的转化率,、表示温度,则可推断出: B、图乙中c表示A的浓度,则可推断出:、为平衡状态 C、图丙中(%)表示A的平衡转化率,p表示体系总压强,则推断出:M点平衡常数为 D、达平衡后,降低温度,则反应速率变化图象可以用图丁表示
A、图甲中表示A的转化率,、表示温度,则可推断出: B、图乙中c表示A的浓度,则可推断出:、为平衡状态 C、图丙中(%)表示A的平衡转化率,p表示体系总压强,则推断出:M点平衡常数为 D、达平衡后,降低温度,则反应速率变化图象可以用图丁表示二、填空题(共55分)
-
16. 按要求填空:(1)、是一种无色气体,在空气中能发生爆炸性自燃生成固态和液态。已知室温下自燃放出热量。写出室温下自燃的热化学方程式。(2)、在时,在中完全燃烧生成液态水,放出的热量,表示燃烧热的热化学方程式为。(3)、在25℃、下,一定质量的无水乙醇完全燃烧时放出热量 , 燃烧生成的用过量电和石灰水吸收可得沉淀,则在此条件下,乙醇完全燃烧的。(4)、可转化为 , 在空气中加热反应可制得铁系氧化物材料。已知25℃、时:
则 。
17.(1)、Ⅰ.某探究性学习小组利用溶液和酸性溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
通过实验A、B可探究(填外部因素)的改变对反应速率的影响,其中;;通过实验可探究温度变化对化学反应速率的影响。实验
序号
实验温度/K
溶液(含硫酸)
溶液
溶液颜色褪至无色时所需时间/s
A
293
2
0.02
5
0.1
5
B
2
0.02
4
0.1
8
C
313
2
0.02
0.1
6
(2)、若 , 则由此实验可以得出的结论是;利用实验B中数据计算,用的浓度变化表示的反应速率为。(3)、Ⅱ.在密闭容器中进行反应: , 式中m、n、p、q为化学计量数。在内,各物质物质的量的变化如下表所示:X
Y
Z
Q
起始/mol
1.2
0
末/mol
0.8
2.7
0.8
2.7
末/mol
0.8
已知内 , 。
确定以下物质的物质的量:起始时 , 。18. 甲醇是重要的化工原料。利用合成气(主要成分为CO、和)在催化剂的作用下合成甲醇,发生的主要反应如下:Ⅰ.
Ⅱ.
在恒容密闭容器进行反应Ⅰ,测得其化学平衡常数K和温度t的关系如表:
t/℃
700
800
830
1000
1200
K
0.6
0.9
1.0
1.7
2.6
(1)、①0,其理由是。(2)、②能判断该反应达到化学平衡状态的依据是。A. B.容器内的体积分数保持不变
C.容器内气体密度保持不变 D.容器中压强保持不变
(3)、③图甲、图乙分别表示反应在时刻达到平衡,在时刻因改变某个条件而发生变化的情况。图甲中时刻发生改变的条件是 , 图乙中时刻发生改变的条件是。
 (4)、④若1200℃时,在某时刻平衡体系中、、、的浓度分别为、、、 , 此时v(正)v(逆)(填大于、小于或等于),其理由是。19. 酸碱中和滴定是一种重要的实验方法,用溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
(4)、④若1200℃时,在某时刻平衡体系中、、、的浓度分别为、、、 , 此时v(正)v(逆)(填大于、小于或等于),其理由是。19. 酸碱中和滴定是一种重要的实验方法,用溶液滴定未知浓度的盐酸,其操作可分解为如下几步:A.检查滴定管是否漏水
B.用蒸馏水洗干净滴定管
C.用待测定的溶液润洗酸式滴定管
D.用酸式滴定管取稀盐酸 , 注入锥形瓶中,加入酚酞溶液
E.取下碱式滴定管,用标准溶液润洗后,将标准液注入碱式滴定管“0”刻度以上处,再把碱式滴定管固定好,并排出尖嘴部分的气泡,调节液面至“0”刻度或“0刻度以下,记下滴定管液面所在刻度
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
0.另取锥形瓶,再重复操作2~3次
完成以下填空。
(1)、判断滴定终点的现象:锥形瓶中溶液从 , 且半分钟内不变色。(2)、如图是第一次滴定时的滴定管中的液面,其读数为 , 。 (3)、根据下表数据计算待测盐酸的浓度:。
(3)、根据下表数据计算待测盐酸的浓度:。滴定次数
待测盐酸体积(mL)
标准溶液体积(mL)
滴定前读数
滴定后读数
第一次
20.00
0.60
x
第二次
20.00
2.00
24.10
第三次
20.00
4.00
24.00
(4)、在上述实验过程中,出现了以下操作(其他操作均正确),其中会造成测定结果(待测液浓度值)偏高的有____(填字母)A、量取标准液的碱式滴定管未润洗 B、锥形瓶水洗后直接装待测液 C、酸式滴定管水洗后未用待测稀盐酸润洗 D、滴定到达终点时,俯视液面读数 E、碱式滴定管尖嘴部分有气泡,滴定后消失20. 我国《生活饮用水卫生标准》中规定生活用水中锅的排放量不超过。处理含镉废水可采用化学沉淀法。(1)、写出磷酸镉沉淀溶解平衡常数的表达式:。(2)、一定温度下,的 , 的 , 该温度下(填“”或“”]的饱和溶液中浓度较大。(3)、向某含镉废水中加入 , 当浓度达到时,废水中的浓度为[已知],此时(填“符合”或“不符合”)《生活饮用水卫生标准》。(4)、如图是氨氧燃料电池示意图。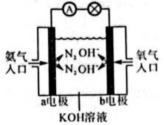
该电池负极的电极反应式为。
21. 其它选做29℃时,如果溶液测得混合溶液的。回答以下问题:
(1)、依据题意推测HA酸为(填强酸或弱酸)。(2)、该溶液的的原因:(用离子方程式表示)。(3)、该溶液中由水电离出的(填“>”“<”或“=”)溶液中由水电离出的。(4)、该溶液中各离子浓度的大小比较。(5)、同温度下,等浓度的四种盐溶液中由大到小的顺序是(填字母)。A. B. C. D.