人教版高中化学2023-2024学年必修一期末模拟试卷(三)
试卷更新日期:2023-12-25 类型:期末考试
一、选择题
-
1. 下列物质中,只含有非极性键的是A、 B、 C、 D、2. 用NA表示阿伏加德罗常数的值,下列说法中正确的是A、在常温常压下,NA个氧气分子的体积为11.2L B、标准状况下,11.2L水含有的分子数为0.5NA C、32gO3和O2的混合气体所含原子数为2NA D、含有2NA个氖原子的氖气在标准状况下的体积约为22.4L3. 下列说法正确的是A、食物腐败、胶体净水、植物光合作用都与氧化还原反应有关 B、可用于文物鉴定,与互为同素异形体 C、既能与酸反应又能与碱反应的化合物属于两性氧化物 D、镧镍合金能大量吸收形成金属氢化物,可作储氢材料4. 下列说法中正确的是( )
①酸性氧化物在一定条件下均能与碱发生反应
②金属氧化物不一定都是碱性氧化物,但碱性氧化物一定都是金属氧化物
③蔗糖和硫酸钡均属于电解质
④盐酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
⑤因为胶粒比溶液中溶质粒子大,所以胶体可以用过滤的方法把胶粒分离出来
⑥氢氧化铁胶体稳定存在的主要原因是胶粒直径介于1~100nm
A、5个 B、4个 C、3个 D、2个5. 甲、乙澄清溶液同时喷洒到白纸上出现红色印迹,对两溶液可能包含离子判断正确的是选项
甲
乙
A
、、、
、、、
B
、、、
、、、
C
、、、
、、、
D
、、、
、、、
A、A B、B C、C D、D6. 向1Lc1Ba(OH)2溶液中匀速滴入c2H2SO4溶液,测得混合溶液的导电能力随时间变化曲线如图所示。下列分析正确的是 A、反应的离子方程式 B、xy段溶液导电能力减弱,说明BaSO4和H2O均为弱电解质 C、y点Ba(OH)2与H2SO4完全反应,溶液没有自由移动的离子 D、由图可知:c1<c27. ClO2气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒,工业制取方法为:。下列分析错误的是A、该反应为氧化还原反应,只有氯元素化合价发生了变化 B、ClO2为氧化反应的产物 C、HCl在该反应中既表现还原性又表现酸性 D、氧化性:NaClO3>Cl28. 有下列氧化还原反应:①2I-+Cl2=I2+2Cl-;②2Fe3++2I-=2Fe2++I2;③2Fe2++Cl2=2Fe3++2Cl-;④2MnO+10Cl-+16H+=2Mn2++5Cl2↑+8H2O,根据上述反应,下列结论中正确的是( )A、要除去含有Fe2+、Cl-和I-的混合溶液中的杂质离子I- , 应通入过量的氯气 B、氧化性强弱顺序为MnO>Cl2>Fe3+>I2 C、Mn2+是MnO的氧化产物,I2是I-的还原产物 D、在溶液中不可能发生反应:MnO+5Fe2++8H+=Mn2++5Fe3++4H2O9. 下列实验操作、现象能够支撑相应结论的是A、用铂丝蘸取某样品进行焰色试验,观察到黄色火焰,说明该样品所所含金属元素只有钠 B、向饱和溶液持续通 , 溶液变浑浊,说明常温下溶解度比大 C、向装有鲜花的集气瓶中通入 , 鲜花变色,说明具具有漂白性 D、将少量固体加入稀盐酸中,产生无色气体,说明非金属性强于C10. 抗疫居家期间,同学们在参与家务劳动的过程中体会到化学知识无处不在。下列劳动与所涉及的化学知识不相符的是
A、反应的离子方程式 B、xy段溶液导电能力减弱,说明BaSO4和H2O均为弱电解质 C、y点Ba(OH)2与H2SO4完全反应,溶液没有自由移动的离子 D、由图可知:c1<c27. ClO2气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒,工业制取方法为:。下列分析错误的是A、该反应为氧化还原反应,只有氯元素化合价发生了变化 B、ClO2为氧化反应的产物 C、HCl在该反应中既表现还原性又表现酸性 D、氧化性:NaClO3>Cl28. 有下列氧化还原反应:①2I-+Cl2=I2+2Cl-;②2Fe3++2I-=2Fe2++I2;③2Fe2++Cl2=2Fe3++2Cl-;④2MnO+10Cl-+16H+=2Mn2++5Cl2↑+8H2O,根据上述反应,下列结论中正确的是( )A、要除去含有Fe2+、Cl-和I-的混合溶液中的杂质离子I- , 应通入过量的氯气 B、氧化性强弱顺序为MnO>Cl2>Fe3+>I2 C、Mn2+是MnO的氧化产物,I2是I-的还原产物 D、在溶液中不可能发生反应:MnO+5Fe2++8H+=Mn2++5Fe3++4H2O9. 下列实验操作、现象能够支撑相应结论的是A、用铂丝蘸取某样品进行焰色试验,观察到黄色火焰,说明该样品所所含金属元素只有钠 B、向饱和溶液持续通 , 溶液变浑浊,说明常温下溶解度比大 C、向装有鲜花的集气瓶中通入 , 鲜花变色,说明具具有漂白性 D、将少量固体加入稀盐酸中,产生无色气体,说明非金属性强于C10. 抗疫居家期间,同学们在参与家务劳动的过程中体会到化学知识无处不在。下列劳动与所涉及的化学知识不相符的是选项
家务劳动
化学知识
A
用白醋除去水壶中的水垢
白醋可溶解沉淀
B
用小苏打粉作膨松剂焙制糕点
加热容易分解放出
C
用含NaClO的84消毒液拖地
NaClO有还原性
D
用洁厕灵洗马桶
洁厕灵中含有盐酸,可以与尿垢反应
A、A B、B C、C D、D11. 红热的铁与水蒸气反应及其部分产物的验证实验装置如图所示,夹持装置已略去,下列有关该实验的说法错误的是 A、浓硫酸的作用是干燥生成的气体 B、实验过程中,可观察到盛有氧化铜的硬质玻璃管中固体颜色由红色变为黑色 C、实验过程中,干燥管中无水硫酸铜由白色变为蓝色,是由于氢气与氧化铜反应生成的水使其变蓝 D、该实验中涉及的反应不一定均为氧化还原反应12. 溶液中,所含的总质量为 , 往该溶液中逐滴滴入的溶液,当沉淀量达到最大时(不考虑水的电离及与水发生的反应),共消耗溶液,下列说法正确的是A、 B、沉淀量达到最大时,反应的离子方程式为 C、原溶液中, D、该反应生成的沉淀均不溶于稀硫酸13. 已知 、 、 、 为短周期元素, 、 同族, 、 、 同周期, 的气态氢化物的稳定性的大于 的气态氢化物的稳定性, 、 为金属元素, 的阳离子的氧化性小于 的阳离子的氧化性。下列说法正确的是A、、、、的原子半径依次减小 B、与形成的化合物中只含离子键 C、的气态氢化物的沸点一定高于的气态氢化物的沸点 D、若 与 的原子序数相差 , 则二者形成化合物的化学式一定为14. 用硫酸渣(主要成分为、)制备铁基颜料铁黄()的一种工艺流程如图。已知:“还原”时,发生反应;、均与不反应。下列有关说法不正确的是
A、浓硫酸的作用是干燥生成的气体 B、实验过程中,可观察到盛有氧化铜的硬质玻璃管中固体颜色由红色变为黑色 C、实验过程中,干燥管中无水硫酸铜由白色变为蓝色,是由于氢气与氧化铜反应生成的水使其变蓝 D、该实验中涉及的反应不一定均为氧化还原反应12. 溶液中,所含的总质量为 , 往该溶液中逐滴滴入的溶液,当沉淀量达到最大时(不考虑水的电离及与水发生的反应),共消耗溶液,下列说法正确的是A、 B、沉淀量达到最大时,反应的离子方程式为 C、原溶液中, D、该反应生成的沉淀均不溶于稀硫酸13. 已知 、 、 、 为短周期元素, 、 同族, 、 、 同周期, 的气态氢化物的稳定性的大于 的气态氢化物的稳定性, 、 为金属元素, 的阳离子的氧化性小于 的阳离子的氧化性。下列说法正确的是A、、、、的原子半径依次减小 B、与形成的化合物中只含离子键 C、的气态氢化物的沸点一定高于的气态氢化物的沸点 D、若 与 的原子序数相差 , 则二者形成化合物的化学式一定为14. 用硫酸渣(主要成分为、)制备铁基颜料铁黄()的一种工艺流程如图。已知:“还原”时,发生反应;、均与不反应。下列有关说法不正确的是 A、“酸溶”时加速搅拌可加快反应速率 B、“过滤Ⅰ”所得滤液中存在的阳离子主要有和 C、“还原”时还原产物与氧化产物的物质的量之比为 D、“氧化”时离子方程式:15. 物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子序数的关系如图所示,N和Z的原子序数之差为8。下列说法正确的是
A、“酸溶”时加速搅拌可加快反应速率 B、“过滤Ⅰ”所得滤液中存在的阳离子主要有和 C、“还原”时还原产物与氧化产物的物质的量之比为 D、“氧化”时离子方程式:15. 物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子序数的关系如图所示,N和Z的原子序数之差为8。下列说法正确的是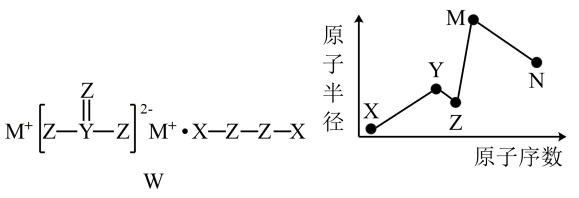 A、X、Z形成的化合物与M、N形成的化合物可以发生氧化还原反应 B、可通过比较Y单质与N单质的还原性强弱来判断Y、N的非金属性强弱 C、Z的氢化物的沸点一定大于Y的氢化物的沸点 D、化合物W常用作氧化剂,宜在高温下使用
A、X、Z形成的化合物与M、N形成的化合物可以发生氧化还原反应 B、可通过比较Y单质与N单质的还原性强弱来判断Y、N的非金属性强弱 C、Z的氢化物的沸点一定大于Y的氢化物的沸点 D、化合物W常用作氧化剂,宜在高温下使用二、非选择题
-
16. 现有以下几种物质(或微粒):
①丝 ② ③ ④液态 ⑤稀 ⑥熔融 ⑦溶液 ⑧饱和溶液 ⑨消毒酒精
回答下列问题:
(1)、②和③之间互为。(2)、以上物质中属于能导电的电解质是。(填代号)(3)、⑤中溶质的电离方程式为。(4)、利用⑧制备胶体的操作方法是。(用文字描述)(5)、向⑤中逐渐加入固体,其溶液的导电性变化情况是。(6)、根据酸能电离出的数目可将酸分为一元酸(如)、二元酸(如)、三元酸(如)。二元酸能与碱反应生成一种正盐(如)和一种酸式盐(如),三元酸能与碱反应生成一种正盐(如)和两种酸式盐(如、)。①属于二元酸,写出它与反应生成酸式盐的化学方程式;
②与溶液反应生成的酸式盐只有一种,则是元酸;若反应生成正盐,则该正盐的化学式为。
17. 疫情防控期间,含氯消毒剂功不可没。(1)、实验室用和浓盐酸制取的离子方程式为。(2)、 是新型的自来水消毒剂,某研究小组用如图装置制备少量(夹持装置已略去)。
已知:常温下极不稳定,为易溶于水但不与水反应的易挥发、易爆气体,沸点11℃。
①产物中的化合价是。
②以和为原料,制得和 , 反应的化学方程式为。
③盛放仪器的名称为 , 冰水浴的作用是。
④产物气被集气瓶B中盛放的稳定剂(某混合盐溶液)吸收,稳定剂的作用是。
⑤烧杯中混合液的作用是吸收尾气,试配平离子方程式:
。
(3)、有效氯可用于衡量含氯消毒剂的消毒能力,的有效氯=有效系数×含氯量 , 其中2是有效系数即夺取电子数,含氯量为氯的相对原子量与消毒剂分子量的比值。已知理论上杀菌消毒的最终产物为 , 则的有效系数为 , 其有效氯为(保留1位小数)。(4)、 在杀菌消毒过程中会产生副产物亚氯酸盐 , 需将其转化为除去。下列试剂中,可将转化为的是_______(填字母序号)。A、 B、 C、18. “鲜花保鲜剂”能延长鲜花的寿命,使人愉悦身心。如表是500mL“鲜花保鲜剂”中含有的成分,阅读后完成以下问题:成分
质量(g)
蔗糖(C12H22O11)
25.000
硫酸钾
0.870
阿司匹林
0.180
高锰酸钾
0.316
硝酸银
0.075
(1)、“鲜花保鲜剂”的下列成分中,不属于电解质的是____。A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银(2)、计算,500mL“鲜花保鲜剂”中硫酸钾的物质的量是 , 其中K+的物质的量浓度是 , 溶液中含个SO。(3)、写出“鲜花保鲜剂”中高锰酸钾的电离方程式。(4)、鉴定“鲜花保鲜剂”中含有K+的实验方法为____。A、显色法 B、沉淀法 C、气体法 D、焰色反应(5)、某同学在配制500mL“鲜花保鲜剂”溶液时,向容量瓶中转移溶液的操作如图所示,请指出图中的两处不正确。
①;②。
(6)、本实验中,会用到胶头滴管,作用是。(7)、在溶液配制过程中,下列操作造成所得溶液浓度偏小的是____。A、定容时俯视容量瓶刻度线 B、容量瓶未干燥,里面有少量蒸馏水 C、溶液由烧杯转移到容量瓶时有少量溶液溅到瓶外 D、定容摇匀后发现液面低于容量瓶的刻度线,未做处理19. 153年前门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。如图为现代元素周期表的一部分,请回答下列问题:(以下问题均用相应的化学用语表达)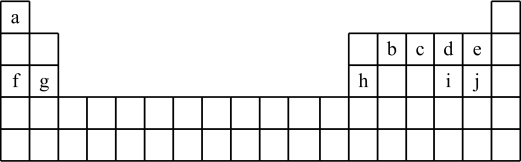 (1)、在这10种元素中,非金属性最强的元素在周期表中的位置是。(2)、由a、d、f三种元素形成的化合物含有的化学键有(填写化学键类型),属于化合物。(3)、元素b、c形成的简单气态氢化物中较稳定的是;d、h、i、j的简单离子半径由大到小的顺序排列为。(4)、用电子式表示c2的形成过程。(5)、在含有a、g、h简单阳离子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:
(1)、在这10种元素中,非金属性最强的元素在周期表中的位置是。(2)、由a、d、f三种元素形成的化合物含有的化学键有(填写化学键类型),属于化合物。(3)、元素b、c形成的简单气态氢化物中较稳定的是;d、h、i、j的简单离子半径由大到小的顺序排列为。(4)、用电子式表示c2的形成过程。(5)、在含有a、g、h简单阳离子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:
①沉淀减少时发生的离子方程式:。
②a点的数值为:mL。