2023-2024学年 浙教版科学 八年级上册 期末复习重难点提升练 专题06 饱和溶液与不饱和溶液
试卷更新日期:2023-12-21 类型:复习试卷
一、选择题
-
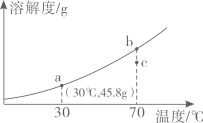
1. 为探究硝酸钾(KNO3)的溶解性,进行了如图所示实验(实验过程)结合硝酸钾在不同温度下的溶解度,判断下列说法不正确的是( )

温度/℃
10
20
30
40
50
60
KNO3溶解度/g
20.9
31.6
45.8
63.9
85.5
110.0
A、①③中的溶液均为不饱和溶液 B、②③中溶液的质量:③>② C、②③④中溶液的溶质质量分数:③>②>④ D、④中析出晶体的质量是0.9g2. 常温下,对100mL氯化钠饱和溶液进行图示实验。下列分析错误的是( ) A、实验1后,甲、乙中溶液的溶质质量分数相等 B、实验2后,乙比甲溶液的溶质质量分数大 C、实验2后,乙中溶液所含溶质质量变大 D、实验2后,甲中溶液为氯化钠的不饱和溶液3. 要想使一瓶接近饱和的石灰水变为饱和,具体的措施有:①加入氢氧化钙;②升高温度;③降低温度;④加入水;⑤蒸发水。其中措施正确的是( )A、①② B、①③④ C、①③⑤ D、①②⑤4. 某同学在进行硫酸铜晶体的制备和生长实验时,配制了某温度时硫酸铜热饱和溶液。下列能判断硫酸铜溶液已饱和的方法是( )A、观察颜色,溶液蓝色较深 B、溶液冷却,有蓝色晶体析出 C、蒸发少量水,有蓝色晶体析出 D、加入硫酸铜晶体,晶体质量不变5. 在一定温度下向某饱和溶液加水稀释时,下列各量中不变的是( )A、溶质质量 B、溶液中溶质的质量分数 C、溶液质量 D、溶剂质量6. 在学校科技节中,小科制作了一个“天气瓶”。该天气瓶通过樟脑在酒精溶液中的溶解情况反映温度变化。如图为该天气瓶在三种不同气温下的状况,下列分析正确的是( )
A、实验1后,甲、乙中溶液的溶质质量分数相等 B、实验2后,乙比甲溶液的溶质质量分数大 C、实验2后,乙中溶液所含溶质质量变大 D、实验2后,甲中溶液为氯化钠的不饱和溶液3. 要想使一瓶接近饱和的石灰水变为饱和,具体的措施有:①加入氢氧化钙;②升高温度;③降低温度;④加入水;⑤蒸发水。其中措施正确的是( )A、①② B、①③④ C、①③⑤ D、①②⑤4. 某同学在进行硫酸铜晶体的制备和生长实验时,配制了某温度时硫酸铜热饱和溶液。下列能判断硫酸铜溶液已饱和的方法是( )A、观察颜色,溶液蓝色较深 B、溶液冷却,有蓝色晶体析出 C、蒸发少量水,有蓝色晶体析出 D、加入硫酸铜晶体,晶体质量不变5. 在一定温度下向某饱和溶液加水稀释时,下列各量中不变的是( )A、溶质质量 B、溶液中溶质的质量分数 C、溶液质量 D、溶剂质量6. 在学校科技节中,小科制作了一个“天气瓶”。该天气瓶通过樟脑在酒精溶液中的溶解情况反映温度变化。如图为该天气瓶在三种不同气温下的状况,下列分析正确的是( ) A、甲瓶中溶液一定是饱和溶液 B、溶液中溶质的质量甲>乙>丙 C、溶液中溶质的质量分数甲<乙<丙 D、樟脑在酒精溶液中的溶解度随温度升高而减小7. 20℃时,向100g水中不断加入固体甲或改变温度,得到相应的溶液①③。下列说法正确的是( )
A、甲瓶中溶液一定是饱和溶液 B、溶液中溶质的质量甲>乙>丙 C、溶液中溶质的质量分数甲<乙<丙 D、樟脑在酒精溶液中的溶解度随温度升高而减小7. 20℃时,向100g水中不断加入固体甲或改变温度,得到相应的溶液①③。下列说法正确的是( ) A、甲是一种微溶物质 B、②中溶质与溶剂的质量比一定为 1:5 C、只有②中的溶液为饱和溶液 D、①~③中溶液的溶质质量分数③>②≥①8. 某温度下,一杯饱和的硝酸钾溶液,欲使其溶质的质量分数改变,下列四位同学提出的措施可行的是( )A、加入硝酸钾晶体 B、降低温度 C、恒温蒸发溶剂 D、升高温度9. 将接近饱和的硝酸钾溶液变成饱和溶液,可采取的方法是( )A、加入硝酸钾 B、升高温度 C、加水 D、加入同温度的硝酸钾饱和溶液10. 小金自制了一个“气象瓶”,其密闭玻璃容器内装有硝酸钾和氯化铵及蒸馏水,当外界温度改变,物质溶解度相应变化,会展现出不同形态的结晶。当澄清透明的气象瓶中出现大量晶体时,相关描述正确的是( )
A、甲是一种微溶物质 B、②中溶质与溶剂的质量比一定为 1:5 C、只有②中的溶液为饱和溶液 D、①~③中溶液的溶质质量分数③>②≥①8. 某温度下,一杯饱和的硝酸钾溶液,欲使其溶质的质量分数改变,下列四位同学提出的措施可行的是( )A、加入硝酸钾晶体 B、降低温度 C、恒温蒸发溶剂 D、升高温度9. 将接近饱和的硝酸钾溶液变成饱和溶液,可采取的方法是( )A、加入硝酸钾 B、升高温度 C、加水 D、加入同温度的硝酸钾饱和溶液10. 小金自制了一个“气象瓶”,其密闭玻璃容器内装有硝酸钾和氯化铵及蒸馏水,当外界温度改变,物质溶解度相应变化,会展现出不同形态的结晶。当澄清透明的气象瓶中出现大量晶体时,相关描述正确的是( ) A、溶液变为不饱和溶液 B、溶解度不变 C、溶剂质量变小 D、溶质质量变小
A、溶液变为不饱和溶液 B、溶解度不变 C、溶剂质量变小 D、溶质质量变小二、填空题
-
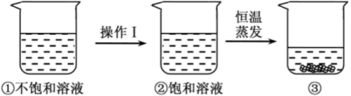
11. 如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,则甲原溶液是(选填:“饱和”或“不饱和”)溶液;按照图中规律,20℃时5克水中最多能溶解甲物质克,X的数值是。
 12. 某同学进行硫酸铜晶体(化学式为CuSO4·5H2O)的制备和生长实验,配制了某温度时的硫酸铜热饱和溶液,静置、冷却到室温,观察晶体的生长,如图。
12. 某同学进行硫酸铜晶体(化学式为CuSO4·5H2O)的制备和生长实验,配制了某温度时的硫酸铜热饱和溶液,静置、冷却到室温,观察晶体的生长,如图。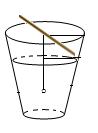 (1)、能判断原硫酸铜溶液已饱和的方法是____。A、观察颜色,溶液蓝色较深 B、溶液冷却,有蓝色晶体析出 C、蒸发少量水,有蓝色晶体析出 D、加入硫酸铜晶体,晶体质量不变(2)、现称取49克无水硫酸铜溶于水,配成150克某温度时的热饱和溶液,再冷却到室温,共析出50克硫酸铜晶体,请计算该室温时硫酸铜饱和溶液的溶质质量分数。13. 小科在室温20℃时探究硝酸钾(KNO3)溶于水的情况,他进行了如图所示实验,其中烧杯A盛有20mL水。整个过程溶剂质量不变,根据有关资料回答下列问题:
(1)、能判断原硫酸铜溶液已饱和的方法是____。A、观察颜色,溶液蓝色较深 B、溶液冷却,有蓝色晶体析出 C、蒸发少量水,有蓝色晶体析出 D、加入硫酸铜晶体,晶体质量不变(2)、现称取49克无水硫酸铜溶于水,配成150克某温度时的热饱和溶液,再冷却到室温,共析出50克硫酸铜晶体,请计算该室温时硫酸铜饱和溶液的溶质质量分数。13. 小科在室温20℃时探究硝酸钾(KNO3)溶于水的情况,他进行了如图所示实验,其中烧杯A盛有20mL水。整个过程溶剂质量不变,根据有关资料回答下列问题:
下表为硝酸钾在不同温度时的溶解度
温度(℃)
10
20
60
100
溶解度(g)
20.9
31.6
110
246
(1)、A→B、B→C操作中需要用到的玻璃仪器除了烧杯,还有。(2)、上述实验过程中属于不饱和溶液的是(填字母)。(3)、在B、C、D、E中,溶液的溶质质量最小是(填字母)。14. 20℃时,向100g水中不断加入固体甲或改变温度,得到相应的溶液①②③。(如图1)(固体甲的溶解度曲线如图2所示,横坐标表示温度,对应的纵坐标表示该温度下的溶解度)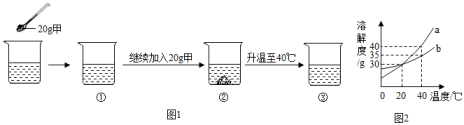 (1)、②中溶质与溶剂的质量比为。(2)、固体甲的溶解度曲线可用图2中的表示(填a或b)。(3)、以上溶液中一定为饱和溶液的是(填写序号)。15. 硝酸钾的溶解度随温度升高而增大。如图所示是对硝酸钾溶液的实验操作及变化情况,以及同一小球在三种溶液中的浮沉情况。请回答下列问题:
(1)、②中溶质与溶剂的质量比为。(2)、固体甲的溶解度曲线可用图2中的表示(填a或b)。(3)、以上溶液中一定为饱和溶液的是(填写序号)。15. 硝酸钾的溶解度随温度升高而增大。如图所示是对硝酸钾溶液的实验操作及变化情况,以及同一小球在三种溶液中的浮沉情况。请回答下列问题: (1)、操作I可能是 (选填字母)。A、降低温度 B、加入硝酸钾 C、蒸发水分(2)、小球所受的浮力F①、F②、F③的大小关系正确的是 。A、F①<F②=F③ B、F①<F②<F③ C、F①>F②=F③ D、F①=F②=F③(3)、从②到③,烧杯底析出硝酸钾晶体5克,整个装置总质量减少了20克,可知②中的溶质质量分数是。
(1)、操作I可能是 (选填字母)。A、降低温度 B、加入硝酸钾 C、蒸发水分(2)、小球所受的浮力F①、F②、F③的大小关系正确的是 。A、F①<F②=F③ B、F①<F②<F③ C、F①>F②=F③ D、F①=F②=F③(3)、从②到③,烧杯底析出硝酸钾晶体5克,整个装置总质量减少了20克,可知②中的溶质质量分数是。三、实验探究题
-
16. 由128克硝酸钾、60克氯化钠组成的混合物投入200g热水溶解,对该溶液进行如图实验(假设实验过程中无损耗)。

温度(℃)
10
20
30
40
60
80
100
溶解度
硝酸钾
20.9
31.6
45.8
64
110
169
248
氯化钠
35.8
36
36.3
35.4
37
38.4
39.8
(1)、两种物质溶解在水中,用玻璃棒搅拌的目的是。(2)、实验时温度t的范围为。(3)、操作1用到的实验仪器有 。A、酒精灯 B、铁架台 C、漏斗 D、玻璃棒 E、蒸发皿(4)、定量述晶体1的组成。(5)、溶液2为 (填物质名称) 的饱和溶液。(6)、关于溶液中NaCl的质量分数:溶液1 溶液2(选填“>“、“<”或“=“)(7)、关于上述实验说法错误的是 。A、晶体1与晶体2比较,晶体1中KNO3的纯度更高 B、溶液1中KNO3为饱和溶液,NaCl为不饱和溶液 C、溶液1恒温蒸发90g水后,与溶液2的成分相同 D、溶液2将水蒸干就可得到纯净的KNO3固体17. 在一定温度下,向100 g水中依次加入一定质量的氯化钾固体,充分溶解。加入氯化钾的质量与得到的相应溶液质量的关系如图B1-5-6所示。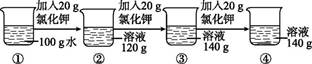 (1)、该温度下氯化钾的溶解度是g。(2)、④中的溶液是不是饱和溶液?(填“是”“不是”或“无法判断”)。18. 图中的四个圆分别表示浓溶液、稀溶液、饱和溶液、不饱和溶液。
(1)、该温度下氯化钾的溶解度是g。(2)、④中的溶液是不是饱和溶液?(填“是”“不是”或“无法判断”)。18. 图中的四个圆分别表示浓溶液、稀溶液、饱和溶液、不饱和溶液。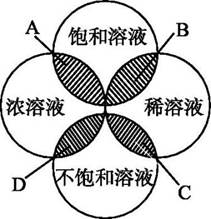 (1)、通过对阴影B、D的分析,你可以得出的结论有。(2)、0.9%的医用生理盐水可归于图中(填“A”“B”“C”或“D”)。 现有一瓶接近饱和的氯化钠溶液,若要使它变为饱和溶液,一般采用的方法是或。19. 根据氯化钠和硝酸钾的溶解度表,回答下列问题。
(1)、通过对阴影B、D的分析,你可以得出的结论有。(2)、0.9%的医用生理盐水可归于图中(填“A”“B”“C”或“D”)。 现有一瓶接近饱和的氯化钠溶液,若要使它变为饱和溶液,一般采用的方法是或。19. 根据氯化钠和硝酸钾的溶解度表,回答下列问题。10℃
20℃
30℃
40℃
50℃
60℃
70℃
氯化钠的质量(克)
35.8
36.0
36.3
36.6
37.0
37.3
37.8
硝酸钾的质量(克)
20.9
31.6
45.8
63.9
85.5
110
138
(1)、在60℃时,硝酸钾的溶解度为克。(2)、在60℃时,在100克水中加入105克硝酸钾,充分搅拌,所得溶液为60℃时硝酸钾的(选填“饱和”或“不饱和")溶液。(3)、欲将40℃时氯化钠的饱和溶液变为不饱和溶液,可采用的方法有。(4)、当温度在范围内时,硝酸钾和氯化钠可能具有相同的溶解度。四、解答题
-
20. 用氯化镁溶液喷洒路面可融雪、防尘。已知20℃时,氯化镁的溶解度为54.6g,在该温度下按下表数据配制溶液。
序号
①
②
③
④
氯化镁的质量/g
30
40
50
60
水的质量/g
100
100
100
100
(1)、所得溶液中,溶质与溶剂的质量比为1:2的是 ;(选填序号,下同)(2)、所得溶液中,属于饱和溶液的是;(3)、 方法可以将上述不饱和溶液转化为饱和溶液;(4)、求序号为④所得溶液中溶质的质量分数。(结果保留到0.1%)21. 在探究物质溶解能力的实验中,小明将60g某固体物质放入盛有50g水的烧杯中充分溶解,测得溶液质量随温度变化的曲线如图。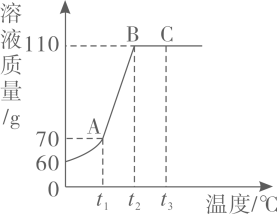 (1)、ABC三点中,一定属于饱和溶液的是。(2)、分析图像,求:t1℃时所得溶液的溶质质量分数为多少(结果保留到0.1%)?(3)、将t3℃时的110g溶液稀释成30%,需加水的质量为多少?
(1)、ABC三点中,一定属于饱和溶液的是。(2)、分析图像,求:t1℃时所得溶液的溶质质量分数为多少(结果保留到0.1%)?(3)、将t3℃时的110g溶液稀释成30%,需加水的质量为多少?