浙江省杭州市杭西高2023-2024学年高一上学期10月月考化学试题
试卷更新日期:2023-11-17 类型:月考试卷
一、选择题Ⅰ(本大题共 15 小题,每小题 2 分,共 30 分。每小题只有一个选项符合题意,
-
1. 下列属于酸性氧化物的是( )A、CO B、Al2O3 C、H2O D、SO32. 下列实验仪器的名称正确的是( )A、酒精灯
 B、铁三角
B、铁三角 C、三角架
C、三角架 D、蒸发皿
D、蒸发皿 3. 下列物质对应的组成不正确的是( )A、干冰: CO 2 B、生石灰: CaSO 4 .2H 2 O C、胆矾: CuSO 4 .5H 2 O D、小苏打: NaHCO 34. 下表中所列物质贴错包装标签的是( )
3. 下列物质对应的组成不正确的是( )A、干冰: CO 2 B、生石灰: CaSO 4 .2H 2 O C、胆矾: CuSO 4 .5H 2 O D、小苏打: NaHCO 34. 下表中所列物质贴错包装标签的是( )选项
A
B
C
D
物质的化学式
HNO3 (浓)
N2
P4
H2
危险警告标识



 A、A B、B C、C D、D5. 古诗是古人为我们留下的宝贵精神财富。下列诗句中不涉及氧化还原反应的是( )A、野火烧不尽,春风吹又生 B、粉身碎骨浑不怕,要留清白在人间 C、春蚕到死丝方尽,蜡炬成灰泪始干 D、爆竹声中一岁除,春风送暖入屠苏6. 下列物质在水溶液中的电离方程式不正确的是( )A、KHCO3 = K+ + HCO3- B、KHSO4 =K+ + H+ + SO42- C、CaCl2 = Ca 2+ + Cl- D、Ba ( OH )2 = Ba 2+ + 2OH-7. 现有下列四个转化, 其中不可能通过一步反应实现的是( )A、Na2CO3→NaOH B、CuO→CuCl2 C、Fe2O3→FeCl2 D、CO2→Na2CO38. 新型冠状病毒可通过咳嗽、打喷嚏、说话等形成的飞沫传播,飞沫直径在 1- 100nm 之间, 进入到空气中形成的分散系属于气溶胶, 口罩可以预防和降低感染的风险性。对此说法,下列叙述正确的是( )A、胶体的本质特征是具有丁达尔效应 B、依据分散质粒子的直径大小可将分散系分为溶液、胶体与浊液 C、向饱和 FeCl3 溶液中滴加过量的 NaOH 溶液可以制备 Fe(OH)3 胶体 D、酒精用于消毒时, 浓度越高,消毒效果越好9. 下列关于碳酸钠和碳酸氢钠的比较中, 正确的是( )A、两者在水中的溶解度不同, 碳酸氢钠的溶解度大于碳酸钠 B、两者热稳定性不同,碳酸钠的热稳定性小于碳酸氢钠 C、两者与足量盐酸反应, 都会产生气泡, 现象一定相同 D、两者都能和澄清石灰水反应,现象一样10. 下列实验操作对应的现象预测正确或能达到有关实验目的的是( )
A、A B、B C、C D、D5. 古诗是古人为我们留下的宝贵精神财富。下列诗句中不涉及氧化还原反应的是( )A、野火烧不尽,春风吹又生 B、粉身碎骨浑不怕,要留清白在人间 C、春蚕到死丝方尽,蜡炬成灰泪始干 D、爆竹声中一岁除,春风送暖入屠苏6. 下列物质在水溶液中的电离方程式不正确的是( )A、KHCO3 = K+ + HCO3- B、KHSO4 =K+ + H+ + SO42- C、CaCl2 = Ca 2+ + Cl- D、Ba ( OH )2 = Ba 2+ + 2OH-7. 现有下列四个转化, 其中不可能通过一步反应实现的是( )A、Na2CO3→NaOH B、CuO→CuCl2 C、Fe2O3→FeCl2 D、CO2→Na2CO38. 新型冠状病毒可通过咳嗽、打喷嚏、说话等形成的飞沫传播,飞沫直径在 1- 100nm 之间, 进入到空气中形成的分散系属于气溶胶, 口罩可以预防和降低感染的风险性。对此说法,下列叙述正确的是( )A、胶体的本质特征是具有丁达尔效应 B、依据分散质粒子的直径大小可将分散系分为溶液、胶体与浊液 C、向饱和 FeCl3 溶液中滴加过量的 NaOH 溶液可以制备 Fe(OH)3 胶体 D、酒精用于消毒时, 浓度越高,消毒效果越好9. 下列关于碳酸钠和碳酸氢钠的比较中, 正确的是( )A、两者在水中的溶解度不同, 碳酸氢钠的溶解度大于碳酸钠 B、两者热稳定性不同,碳酸钠的热稳定性小于碳酸氢钠 C、两者与足量盐酸反应, 都会产生气泡, 现象一定相同 D、两者都能和澄清石灰水反应,现象一样10. 下列实验操作对应的现象预测正确或能达到有关实验目的的是( ) A、①可比较Na2CO3 、 NaHCO3 的稳定性 B、②焰色试验检验 K 元素 C、③分离氯化铁溶液和氢氧化铁胶体 D、④制备氢氧化铁胶体11. 下列各组离子在对应条件下一定能在大量共存的是( )A、遇石蕊变红的溶液: Na+ 、 CO32- 、 NO3- 、 Ba2+ B、无色溶液: Na+ 、 Fe2+ 、 ClO- 、 Cl- C、遇酚酞变红的溶液: K+ 、 NH4+ 、 OH- 、 HCO3- D、在 pH=1 的溶液中: K+ 、 Na+ 、 SO42- 、 NO3-12. 节日燃放的烟花利用了“焰色试验 ”的原理。下列说法中正确的是 ( )A、焰色试验属于化学变化 B、焰色试验时铂丝应用盐酸清洗并在外焰上灼烧至与原来颜色相同时,再蘸取样品灼烧 C、某样品的焰色颜色为黄色,则该样品仅含有钠元素 D、实验时最好选择颜色较深的火焰13. 如图装置,试管中盛有水, 气球 a 中盛有干燥的 Na2O2 粉末, U 形管中注有红色的墨水。 将气球用橡皮筋紧缚在试管口。实验时将气球中的 Na2O2粉末抖落到试管 b 中的水中,将发生的现象是( )
A、①可比较Na2CO3 、 NaHCO3 的稳定性 B、②焰色试验检验 K 元素 C、③分离氯化铁溶液和氢氧化铁胶体 D、④制备氢氧化铁胶体11. 下列各组离子在对应条件下一定能在大量共存的是( )A、遇石蕊变红的溶液: Na+ 、 CO32- 、 NO3- 、 Ba2+ B、无色溶液: Na+ 、 Fe2+ 、 ClO- 、 Cl- C、遇酚酞变红的溶液: K+ 、 NH4+ 、 OH- 、 HCO3- D、在 pH=1 的溶液中: K+ 、 Na+ 、 SO42- 、 NO3-12. 节日燃放的烟花利用了“焰色试验 ”的原理。下列说法中正确的是 ( )A、焰色试验属于化学变化 B、焰色试验时铂丝应用盐酸清洗并在外焰上灼烧至与原来颜色相同时,再蘸取样品灼烧 C、某样品的焰色颜色为黄色,则该样品仅含有钠元素 D、实验时最好选择颜色较深的火焰13. 如图装置,试管中盛有水, 气球 a 中盛有干燥的 Na2O2 粉末, U 形管中注有红色的墨水。 将气球用橡皮筋紧缚在试管口。实验时将气球中的 Na2O2粉末抖落到试管 b 中的水中,将发生的现象是( ) A、U 形管内红色墨水褪色 B、试管内溶液变红 C、气球 a 被吹大 D、U 形管水位: c>d14. 下列氧化还原反应中,电子转移的方向和数目均正确的是( )A、
A、U 形管内红色墨水褪色 B、试管内溶液变红 C、气球 a 被吹大 D、U 形管水位: c>d14. 下列氧化还原反应中,电子转移的方向和数目均正确的是( )A、 B、
B、 C、
C、 D、
D、 15. 合成新物质是化学研究的主要目的之一。意大利科学家最近合成了一种新型的氧分子O4 ,下列关于 O4 的说法正确的是( )A、O4 是一种新型化合物 B、1 个 O4 分子由两个 O2 分子构成 C、O4 、O2 、O3 都是氧元素的同素异形体 D、O4 和 O2 可通过氧化还原反应实现转化
15. 合成新物质是化学研究的主要目的之一。意大利科学家最近合成了一种新型的氧分子O4 ,下列关于 O4 的说法正确的是( )A、O4 是一种新型化合物 B、1 个 O4 分子由两个 O2 分子构成 C、O4 、O2 、O3 都是氧元素的同素异形体 D、O4 和 O2 可通过氧化还原反应实现转化二、选择题Ⅱ(本大题共 10 小题,每小题 3 分,共 30 分。每小题只有一个选项符合题意,
-
16. 下列化学反应的离子方程式中正确的是( )A、向 Ca(HCO3)2 溶液加入过量的 NaOH 溶液: Ca2+ +HCO3- +OH-=CaCO3 ↓ +H2O B、向 NH4HCO3 溶液中滴入少量 NaOH 溶液: NH4+ +OH -=NH3·H2O C、澄清石灰水与少量小苏打溶液混合: Ca2+ +HCO3- +OH- =CaCO3 +H2O D、少量氢氧化钡溶液与过量硫酸氢钠混合: Ba2+ +OH- +H+ +SO42- =BaSO4+H2O17. 如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )
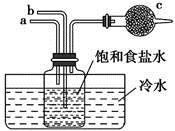 A、a通入CO2 , 然后b通入NH3 , c中放碱石灰 B、b通入NH3 , 然后a通入CO2 , c中放碱石灰 C、a通入NH3 , 然后b通入CO2 , c中放蘸稀硫酸的脱脂棉 D、b通入CO2 , 然后a通入NH3 , c中放蘸稀硫酸的脱脂棉18. 图 a~c 分别为氯化钠在不同状态下的导电实验(X、Y 均表示石墨电极,X 与电源正极相
A、a通入CO2 , 然后b通入NH3 , c中放碱石灰 B、b通入NH3 , 然后a通入CO2 , c中放碱石灰 C、a通入NH3 , 然后b通入CO2 , c中放蘸稀硫酸的脱脂棉 D、b通入CO2 , 然后a通入NH3 , c中放蘸稀硫酸的脱脂棉18. 图 a~c 分别为氯化钠在不同状态下的导电实验(X、Y 均表示石墨电极,X 与电源正极相连, Y 与电源负极相连)微观示意图。下列说法正确的是( )
 A、图示中
A、图示中 代表的是水合钠离子
B、氯化钠只有在通电条件下才能电离
C、图 b 表示熔融状态下氯化钠的导电过程
D、氯化钠在不同状态下均能导电
19. 已知Co2O3 在酸性溶液中易被还原成 Co2+ ,且还原性: I- >Fe2+ >Cl- >Co2+ 。下列反应在水溶液中不可能发生的是( )A、3Cl2 +6FeI2 =2FeCl3 +4FeI3 B、3Cl2 +2FeI2 =2FeCl3 +2I2 C、Co2O3 +6HCl=2CoCl2 +Cl2 ↑ +3H2O D、2Fe3+ +2I- =2Fe2+ +I220. 向一定体积的 Ba(OH)2 溶液中逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化的曲线如图所示, 下列说法正确的是( )
代表的是水合钠离子
B、氯化钠只有在通电条件下才能电离
C、图 b 表示熔融状态下氯化钠的导电过程
D、氯化钠在不同状态下均能导电
19. 已知Co2O3 在酸性溶液中易被还原成 Co2+ ,且还原性: I- >Fe2+ >Cl- >Co2+ 。下列反应在水溶液中不可能发生的是( )A、3Cl2 +6FeI2 =2FeCl3 +4FeI3 B、3Cl2 +2FeI2 =2FeCl3 +2I2 C、Co2O3 +6HCl=2CoCl2 +Cl2 ↑ +3H2O D、2Fe3+ +2I- =2Fe2+ +I220. 向一定体积的 Ba(OH)2 溶液中逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化的曲线如图所示, 下列说法正确的是( )
①XY 段溶液的导电能力不断减弱,说明生成的 BaSO4 不是电解质
②YZ 段溶液的导电能力不断增大,主要是由于过量的 Ba(OH)2 电离出的离子导电
③Y 处溶液的导电能力约为 0,说明溶液中几乎没有自由移动的离子
④a 时刻 Ba(OH)2 溶液与稀硫酸恰好完全中和
A、①② B、①③ C、③④ D、②④21. 元素的价类二维图指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二 维平面图象。下图为钠元素的价类二维图,其中的箭头表示部分物质间的转化关系,下列说法不正确 的是( ) A、氢氧化钠溶液可以与过量二氧化碳反应实现转化关系① B、Na2O2 发生④⑤的转化均有O2产生 C、碳酸钠溶液中不断滴加盐酸依次发生反应③和⑧生成氯化钠 D、反应②只能通过加热才能实现物质转化22. 2019 年诺贝尔化学奖颁给几位在锂离子电池研发领域做出贡献的科学家, 锂单质化学 性质与钠类似, 活泼性比钠略差。它的密度为 0.534g/cm3 , 锂元素的焰色为紫红色, 将绿豆大的锂投入水中,下列实验现象合理的有( )
A、氢氧化钠溶液可以与过量二氧化碳反应实现转化关系① B、Na2O2 发生④⑤的转化均有O2产生 C、碳酸钠溶液中不断滴加盐酸依次发生反应③和⑧生成氯化钠 D、反应②只能通过加热才能实现物质转化22. 2019 年诺贝尔化学奖颁给几位在锂离子电池研发领域做出贡献的科学家, 锂单质化学 性质与钠类似, 活泼性比钠略差。它的密度为 0.534g/cm3 , 锂元素的焰色为紫红色, 将绿豆大的锂投入水中,下列实验现象合理的有( )①锂沉入水中 ②锂浮在水面上 ③水中不会有大量气泡 ④反应后在水中加入几滴石蕊试液, 溶液变红 ⑤反应剧烈, 发出紫红色火焰 ⑥锂四处游动
A、②⑥ B、①③ C、②③⑤ D、②④⑤⑥23. 已知三个氧化还原反应: ①2FeCl3+2KI=2FeCl2+2KCl+I2 ,②2FeCl2+Cl2=2FeCl3 ,③ 2KMnO4+16HCl(浓)= 2KCl+2MnCl2+8H2O+5Cl2 ↑。若某溶液中有 Fe2+、I-、Cl-共存,要将 I-氧化除去而不氧化 Fe2+和 Cl- ,则可加入的试剂是( )A、Cl2 B、KMnO4 C、FeCl3 D、HCl24. 某溶液中只含有大量的下列离子:Mg2+ 、 NO3- 、K+和 M 离子, 经测定 Mg2+ 、 NO3-、 K+和 M 离子的个数之比为 3:5: 1: 1,则 M 离子可能是( )A、CO32 - B、SO42 - C、Ca2+ D、Na+25. 某溶液只含下表离子中的几种, 且各离子的物质的量浓度相等(不考虑水的电离与离子水解)。某同学进行了如下实验(必要时可加热):阳离子
K+ 、NH4+ 、Fe2+ 、Mg2+ 、Cu2+
阴离子
OH- 、Cl- 、CO32- 、SO42-

下列说法正确的是( )
A、由沉淀 A 推断原溶液中一定含有SO42- B、滤液 A 中可能含有 K+ C、原溶液中只含有 NH4+ 、Fe2+ 、Cl- 、SO42- D、沉淀 B 中一定含有 Mg(OH)2三、非选择题(本题共 5 小题,共 40 分)
-
26. 现有以下物质: ①铜; ②盐酸; ③明矾晶体;④熔融NaHSO4 ;⑤ Fe ( OH )3 胶体; ⑥ NaHCO3 粉末;⑦CO2 ;⑧ Ba( OH )2 晶体;⑨蔗糖; ⑩冰水混合物(1)、以上物质中属于电解质的是 (填序号),以上纯净物中能导电的有 (填序号)。(2)、写出制备物质⑤的化学方程式。(3)、在④的水溶液中加入少量⑧ , 发生反应的离子方程式为。27. 储氢纳米碳管具有广泛的用途, 电弧法合成的碳纳米管常伴有大量的杂质碳纳米颗粒,这种碳纳来颗粒可用氧化气化法提纯,反应的化学方程式如下(未配平): C + K2Cr2O7 + H2SO4 = CO2+K2SO4+Cr2(SO4)3+H2O
回答下列问题:
(1)、配平上述反应方程式,并用双线桥标出电子转移方向和数目。(2)、 H2SO4 在该反应中表现出____ (填标号)。A、只有酸性 B、只有氧化性 C、酸性和氧化性 D、酸性和还原性(3)、磷酸(H3PO4 )、次磷酸(H3PO2 )是精细磷化工产品,均属于中强酸,磷酸为三元酸,而次磷酸为一元酸。回答下列问题:H3PO2 及 NaH2PO2 均可将溶液中的Ag+还原为银,从而可用于化学镀银。从物质的分类来看,NaH2PO2属于 (填标号)。
a.正盐 b.酸式盐 c.钠盐 d.氧化物
28. 将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子: K+ 、 Mg2+ 、 Fe3+ 、 Ba2+ 、 SO42- 、 OH- 、 CO32- 和 Cl- ,取该溶液进行如下实验:Ⅰ.取少量溶液滴入紫色石蕊试液, 溶液呈蓝色。
Ⅱ.取少许溶液滴入BaCl2 溶液, 无白色沉淀产生。
Ⅲ.取少许溶液先滴加硝酸再加AgNO3 溶液, 产生白色沉淀。
Ⅳ.再取少许原溶液滴入少量H2SO4 溶液,有白色沉淀产生。
(1)、根据以上现象判断, 原溶液中肯定不存在的离子是 ;肯定存在的离子是 。(2)、如溶液中各种离子的浓度相等,确定溶液中 (填有或无)K+ ,判断依据是 。29. 从物质分类的角度看,Na2O和 Na2O2 都属于氧化物, 但二者的性质存在很大差异。查阅资料得知,Na 2 O 2 可在呼吸面具和潜水艇中做供氧剂,某实验小组欲通过实验探究Na2O2 的性质与用途。(1)、【实验 I】探究Na2O2与水的反应
如图,将 1~2mL 水滴入盛有 1~2g 过氧化钠固体的试管中,立即把带火星的小木条伸 入试管中, 观察到带火星的小木条复燃, 说明生成了 , 用手触摸试管外壁, 感觉发烫,说明该反应是 (填“吸热”或“放热”)反应。 (2)、【实验 II】探究 Na2O2 与CO2的反应
(2)、【实验 II】探究 Na2O2 与CO2的反应
装置 A 中盛装碳酸钙的仪器名称是。
(3)、写出 D 中发生反应的化学方程式: 。(4)、装置 E 的作用是除去过量的CO2 ,则装置 E 中盛装的试剂是。(5)、G 中得到的物质是 ,证明 Na2O2可用作呼吸面具和潜水艇的供氧剂。30. 将某碳酸钠和碳酸氢钠混合物2.43g加热到质量不再变化时,剩余物质的质量为2.12g,求:(1)、写出加热过程中发生反应的化学方程式。(2)、碳酸氢钠的质量为克?(3)、碳酸钠的质量分数为(保留三位有效数字)?