浙江省舟山市定海二中教育集团2023-2024学年九年级上册科学10月月考试卷
试卷更新日期:2023-11-06 类型:月考试卷
一、选择题(本题有15小题,每小题3分,共45分。请选出一个符合题意的正确选项,不选、多选、错选,均不给分)。
-
1. 化学在人类生活生产中扮演着重要角色,以下说法或应用正确的是:( )A、为提高农作物的产量和质量,应大量使用化肥和农药 B、为改善食物的色、香、味并防止变质,可在其中加入大量食品添加剂 C、在汽车排气管上加装“催化转化器”是为了减少有害气体的排放 D、废旧电池应集中回收,并填埋处理2. 熏艾柱是中医调理身体常用的手段,下列制作艾柱过程中主要发生化学变化的是( )A、清洗艾叶
 B、晒干艾叶
B、晒干艾叶 C、卷成艾柱
C、卷成艾柱 D、燃烧艾柱
D、燃烧艾柱 3. 近年来,杭州新能源电动车(如图所示)迅猛发展。下列用电器能量转换的形式与新能源电动车相同的是( )
3. 近年来,杭州新能源电动车(如图所示)迅猛发展。下列用电器能量转换的形式与新能源电动车相同的是( ) A、电风扇 B、电灯 C、收音机 D、电饭锅4. 实验是学习初中科学的重要途径。下列实验操作正确的是( )A、给液体加热
A、电风扇 B、电灯 C、收音机 D、电饭锅4. 实验是学习初中科学的重要途径。下列实验操作正确的是( )A、给液体加热 B、过滤浊液
B、过滤浊液 C、检查装置的气密性
C、检查装置的气密性 D、稀释浓硫酸
D、稀释浓硫酸 5. 久置NaOH易变质,为检验一瓶久置NaOH溶液是否已完全变质,有以下几种验证方法,其中正确的是( )
5. 久置NaOH易变质,为检验一瓶久置NaOH溶液是否已完全变质,有以下几种验证方法,其中正确的是( )①用pH试纸测得反应后的溶液pH大于7,表示NaOH未完全变质;
②不断滴加稀盐酸,如果一段时间后出现气泡,表示NaOH未完全变质;
③滴加过量 , 过滤后在滤液中滴加酚酞,如果变红,表示NaOH未完全变质;
④滴加过量反应后取上层清液,滴加无沉淀生成,表示NaOH完全变质。
A、①② B、②③ C、②④ D、③④6. 在研究稀硫酸性质时,分别将一定量的稀硫酸滴入盛有锌粒、氧化铜粉末、氢氧化铜粉末和氯化钡溶液的4支试管中。有关实验的说法错误的是( ) A、反应①中有气泡产生 B、反应②中铜的化合价升高 C、反应③中将生成蓝色溶液 D、反应④属于复分解反应7. 现有铁粉、二氧化锰、硫酸钡和铁矿石四种固体,为了区分它们,小科照二歧分类法,制作了如图的检索表,下列叙述错误的是( )
A、反应①中有气泡产生 B、反应②中铜的化合价升高 C、反应③中将生成蓝色溶液 D、反应④属于复分解反应7. 现有铁粉、二氧化锰、硫酸钡和铁矿石四种固体,为了区分它们,小科照二歧分类法,制作了如图的检索表,下列叙述错误的是( ) A、甲表示的是铁矿石 B、乙表示的是铁粉 C、表中“ ”应该表示为“黑色固体” D、也可根据是否含有氧元素对丙、丁分类8. 如图是稀硫酸与甲、乙、丙、丁、戊五种常见物质反应出现的不同现象。下列有关说法正确的是( )
A、甲表示的是铁矿石 B、乙表示的是铁粉 C、表中“ ”应该表示为“黑色固体” D、也可根据是否含有氧元素对丙、丁分类8. 如图是稀硫酸与甲、乙、丙、丁、戊五种常见物质反应出现的不同现象。下列有关说法正确的是( ) A、甲可能是无色酚酞试液 B、乙、戊一定是金属单质 C、稀硫酸与丙生成的白色沉淀不可能属于盐 D、稀硫酸与丁的反应类型可能是置换反应9. 模型能够直观反映化学变化的结果。将一定质量的镁条放入某一溶液(如图),其溶质硫酸铜和硫酸亚铁的质量相同,充分反应后烧杯内固体的组成和质量大小关系不可能的是( )
A、甲可能是无色酚酞试液 B、乙、戊一定是金属单质 C、稀硫酸与丙生成的白色沉淀不可能属于盐 D、稀硫酸与丁的反应类型可能是置换反应9. 模型能够直观反映化学变化的结果。将一定质量的镁条放入某一溶液(如图),其溶质硫酸铜和硫酸亚铁的质量相同,充分反应后烧杯内固体的组成和质量大小关系不可能的是( ) A、
A、 B、
B、 C、
C、 D、
D、 10. 南京理工大学胡炳成团队用新方法制得了 , 该化合物中含有等微粒,已知为7号元素,则下列有关说法正确的是( )A、是一种氧化物 B、1个共含有35个质子 C、1个带五个单位的负电荷 D、1个中共含有35个电子11. 小金将一定量的氢氧化钠溶液与稀硫酸混合,如图1所示,发现没有明显的现象。小金分别取图烧杯中溶液进行以下实验,结果如图2所示。以下说法正确的是( )
10. 南京理工大学胡炳成团队用新方法制得了 , 该化合物中含有等微粒,已知为7号元素,则下列有关说法正确的是( )A、是一种氧化物 B、1个共含有35个质子 C、1个带五个单位的负电荷 D、1个中共含有35个电子11. 小金将一定量的氢氧化钠溶液与稀硫酸混合,如图1所示,发现没有明显的现象。小金分别取图烧杯中溶液进行以下实验,结果如图2所示。以下说法正确的是( ) A、实验一能证明图1中的反应已经发生 B、D中溶液为无色,说明溶液中没有 C、将试管C静置,上层清液中一定含有的溶质是 D、根据实验一、二,可以判断氢氧化钠与硫酸恰好完全反应12. 如图为桌球运动员击打白球后,白球撞击黑球的运动轨迹图,其中乙和丁点为两球撞击后的瞬间,最终分别停留在丙点和戊点。假设黑白两球完全一样,桌面粗糙程度相同。下列有关不同点对应小球机械能大小关系错误的是( )
A、实验一能证明图1中的反应已经发生 B、D中溶液为无色,说明溶液中没有 C、将试管C静置,上层清液中一定含有的溶质是 D、根据实验一、二,可以判断氢氧化钠与硫酸恰好完全反应12. 如图为桌球运动员击打白球后,白球撞击黑球的运动轨迹图,其中乙和丁点为两球撞击后的瞬间,最终分别停留在丙点和戊点。假设黑白两球完全一样,桌面粗糙程度相同。下列有关不同点对应小球机械能大小关系错误的是( ) A、乙>丁 B、乙>丙 C、甲>乙+丁 D、丙=戊13. 如图所示,围棋棋盘上有五枚棋子,代表铁、稀盐酸、氢氧化钡、碳酸钙、硝酸银五种物质,相邻棋子间的连线表示物质间可以反应。已知与戊的反应中,甲 -戊的反应类型不同于其他几个反应;丙﹣戊反应能产生一种气体,且该气体还能与丁反应生成沉淀。则下列对应关系正确的是( )
A、乙>丁 B、乙>丙 C、甲>乙+丁 D、丙=戊13. 如图所示,围棋棋盘上有五枚棋子,代表铁、稀盐酸、氢氧化钡、碳酸钙、硝酸银五种物质,相邻棋子间的连线表示物质间可以反应。已知与戊的反应中,甲 -戊的反应类型不同于其他几个反应;丙﹣戊反应能产生一种气体,且该气体还能与丁反应生成沉淀。则下列对应关系正确的是( )
甲
乙
丙
丁
戊
A
铁
硝酸银
碳酸钙
氢氧化钡
稀盐酸
B
硝酸银
铁
稀盐酸
氢氧化钡
碳酸钙
C
硝酸银
铁
碳酸钙
氢氧化钡
稀盐酸
D
铁
氢氧化钡
碳酸钙
硝酸银
稀盐酸
A、A B、B C、C D、D14. 下列实验方案,能达到实验目的的是( )选项
实验目的
实验方案
A
稀释浓
将水倒入浓中并用玻璃棒不断搅拌
B
分离铜粉和锌粉的混合物
加入足量的稀硫酸,过滤、洗涤、干燥
C
检验散口放置的NaOH溶液是否变质
取样,滴加酚酞溶液,观察颜色
D
从KCl和的混合物中回收
加水充分溶解、过滤、洗涤、干燥
A、A B、B C、C D、D15. 图像能直观表达变量之间的关系。往一定量NaOH和BaCl2的混合溶液中逐滴加入稀硫酸直至过量,下列图像表达的变量关系正确的是( )A、 B、
B、 C、
C、 D、
D、
二、填空题(本题有9小题,20空格,每空格2分,共40分)
-
16. 科学与人类生产、生活息息相关,阅读并回答下列问题:(1)、 2022年,中国科学家不利用光合作用,直接以二氧化碳和氢气为原料,经过一系列反应成功合成了淀粉。淀粉属于七大营养素中的(2)、小金同学帮妈妈做饭,刮山药皮时手上皮肤奇痒难忍(山药中含有的碱性皂角素所致)。可以用厨房中的(填调味品名称)来止痒。17. 下表是几种家用清洁剂的功能和有效成分。
清洁剂

洁厕灵

彩漂液

漂白水
功能
清除污垢,除异味
漂洗衣物,使色彩鲜艳
漂除衣物污渍
有效成分
HCl
H2O2
NaClO
(1)、厕所污垢的主要成分是尿碱,通常用洁厕灵进行清洗,由此可推测尿碱是一种具有(选填“酸性”或“碱性”)的物质;(2)、各取适量三种清洁剂于试管中,加入少许二氧化锰,有大量气泡产生的清洁剂是18. 小滨向Na2SO4溶液中滴入Ba(NO3)2溶液至恰好完全反应。(1)、从四大基本反应类型看,该反应属于。(2)、若反应前后溶液中存在的离子种类如图所示,其中“ ”“
”“  ”“
”“  ”“
”“  ”表示不同种类的离子,则“
”表示不同种类的离子,则“  ”表示(填离子符号)。
”表示(填离子符号)。
 19. 氢是实现碳中和的能源载体。(1)、1781年,普里斯特利用金属M与稀盐酸反应制得一定量的氢气。M可能是锌、铜、银三种金属中的;该反应的微观示意图如图,其中表示反应后溶液中金属离子的微粒是。(选填“A”“B”或“C”)。
19. 氢是实现碳中和的能源载体。(1)、1781年,普里斯特利用金属M与稀盐酸反应制得一定量的氢气。M可能是锌、铜、银三种金属中的;该反应的微观示意图如图,其中表示反应后溶液中金属离子的微粒是。(选填“A”“B”或“C”)。 (2)、煤制氢的原理可表示为 , 则X中肯定含有的元素是。20. 人类对能源的需求日益增长,环境问题和新能源的开发备受关注。(1)、充分燃烧相同质量的天然气和煤,所产生的CO2和SO2气体的质量如图甲所示,则燃烧产生的气体更易导致酸雨。
(2)、煤制氢的原理可表示为 , 则X中肯定含有的元素是。20. 人类对能源的需求日益增长,环境问题和新能源的开发备受关注。(1)、充分燃烧相同质量的天然气和煤,所产生的CO2和SO2气体的质量如图甲所示,则燃烧产生的气体更易导致酸雨。 (2)、实现“碳中和”的措施之一是“碳转化”,其反应原理如图乙所示。即一定条件下,将二氧化碳分子和氢分子在催化剂表面转化成某种有机清洁燃料,在该化学反应的反应物和生成物中,共出现种氧化物。21. 竖直向上抛出一物块,物块在空中运动的过程中受到的阻力大小恒定,其动能和重力势能随高度变化的图线如图所示,则物块在运动过程中受到的阻力大小为N,物块再次回到抛出点时,动能大小为J。
(2)、实现“碳中和”的措施之一是“碳转化”,其反应原理如图乙所示。即一定条件下,将二氧化碳分子和氢分子在催化剂表面转化成某种有机清洁燃料,在该化学反应的反应物和生成物中,共出现种氧化物。21. 竖直向上抛出一物块,物块在空中运动的过程中受到的阻力大小恒定,其动能和重力势能随高度变化的图线如图所示,则物块在运动过程中受到的阻力大小为N,物块再次回到抛出点时,动能大小为J。 22. 2019年诺贝尔化学奖表彰锂离子电池的研发。这种质量轻、可充电、功能强大的电池现在被广泛应用于手机、笔记本电脑和电动汽车等各种产品。(1)、锂电池充电时,电能转化为能。(2)、碳酸乙烯酯()是锂电池电解液的一种成分,其中碳元素和氢元素的质量比为。(3)、下图为某款锂电池手机在不同温度下的电压随时间变化的图像,该电池的放电终止电压为3伏,低于3伏之后不宜再继续放电。请结合图像分析手机夏天比冬天耐用的原因是:。
22. 2019年诺贝尔化学奖表彰锂离子电池的研发。这种质量轻、可充电、功能强大的电池现在被广泛应用于手机、笔记本电脑和电动汽车等各种产品。(1)、锂电池充电时,电能转化为能。(2)、碳酸乙烯酯()是锂电池电解液的一种成分,其中碳元素和氢元素的质量比为。(3)、下图为某款锂电池手机在不同温度下的电压随时间变化的图像,该电池的放电终止电压为3伏,低于3伏之后不宜再继续放电。请结合图像分析手机夏天比冬天耐用的原因是:。 23. 在水平地面上有一长方体木箱。小林用水平推力F把木箱向前推,如图甲所示。此过程中,推力F随时间t的变化情况如图乙所示,木块前进的速度v的大小随时间t的变化情况如图丙所示。
23. 在水平地面上有一长方体木箱。小林用水平推力F把木箱向前推,如图甲所示。此过程中,推力F随时间t的变化情况如图乙所示,木块前进的速度v的大小随时间t的变化情况如图丙所示。 (1)、0~1秒内,推力F对木箱是否做功(选填“是”或“否”);(2)、3~5秒内,推力F对木箱做功焦。24. “登高取物”游戏规则:梯子上下相邻的物质之间能发生反应的,游戏者可以上升一格, 最终登顶者可以获得“足球”奖励。甲同学根据规则能顺利获奖,乙同学根据规则从 CaCO3、CuSO4、KNO3、BaCl2 中选择合适物质填入①、②两处,也顺利获奖。
(1)、0~1秒内,推力F对木箱是否做功(选填“是”或“否”);(2)、3~5秒内,推力F对木箱做功焦。24. “登高取物”游戏规则:梯子上下相邻的物质之间能发生反应的,游戏者可以上升一格, 最终登顶者可以获得“足球”奖励。甲同学根据规则能顺利获奖,乙同学根据规则从 CaCO3、CuSO4、KNO3、BaCl2 中选择合适物质填入①、②两处,也顺利获奖。 (1)、②是。(2)、写出图中有 CuO 参加的一个化学反应方程式。
(1)、②是。(2)、写出图中有 CuO 参加的一个化学反应方程式。三、实验探究题(本题有5小题,15空格,每空格2分,共30分)
-
25. 如图所示为探究影响物体动能大小因素所做的实验。(M和m分别代表小木块和小钢球)
 (1)、让同一小钢球在斜面的不同高度自由释放,目的是为了探究对动能大小的影响;(2)、本实验中小钢球的动能大小是通过来体现的。26. 一次实验中,同学们发现了一瓶标签受损的无色溶液,如图所示。这瓶是什么溶液呢?同学们进行了以下探究:
(1)、让同一小钢球在斜面的不同高度自由释放,目的是为了探究对动能大小的影响;(2)、本实验中小钢球的动能大小是通过来体现的。26. 一次实验中,同学们发现了一瓶标签受损的无色溶液,如图所示。这瓶是什么溶液呢?同学们进行了以下探究:【提出猜想】这瓶溶液可能是①氯化钠溶液 ②硝酸钠溶液 ③碳酸钠溶液 ④氢氧化钠溶液
【查阅资料】硝酸钠溶液呈中性
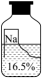 (1)、【实验探究】
(1)、【实验探究】取少量该溶液于试管,向其中滴加几滴紫色石蕊试液,试液变蓝色,则猜想不成立。
(2)、将该溶液滴加到稀盐酸中,观察到(填现象),猜想③成立。【反思评价】
有同学指出该结论不够严密,理由是若该溶液为氢氧化钠溶液,发生部分变质后也能产生上述现象。为此,同学们认为,往该无色溶液中加入过量的溶液排除干扰,再检验氢氧化钠即可。
27. 小舟在学习“常见的碱”过程中,将新配制的饱和 , 溶液滴入到溶液中,发现没有出现预期的红褐色沉淀。这是为什么呢?小舟查阅资料,获取如下信息:①微溶于水;②溶液呈酸性。于是他提出以下猜想:
猜想一:没有参加化学反应。
猜想二:滴入的溶液中数量太少。
猜想三:溶液呈酸性,沉淀不能存在。
 (1)、小舟用pH试纸测和混合液的酸碱度,测得 , 说明溶液中没有。该现象(选填“支持”或“不支持”)猜想一。(2)、为增加的数量,换用浓NaOH溶液滴加到溶液中(如图甲),若猜想二正确,则观察到的现象是。(3)、经过实验,猜想三验证成立。然后,小舟将溶液逐滴滴加到饱和溶液中(如图乙),先观察到红褐色沉淀产生,持续滴加后沉淀又消失了。请你解释沉淀会消失的原因。28. 小宁在课外资料中获悉:在锌和稀硫酸的反应中,加入硫酸铜溶液会影响反应的快慢。为此,他进行了探究。实验装置如图甲所示。
(1)、小舟用pH试纸测和混合液的酸碱度,测得 , 说明溶液中没有。该现象(选填“支持”或“不支持”)猜想一。(2)、为增加的数量,换用浓NaOH溶液滴加到溶液中(如图甲),若猜想二正确,则观察到的现象是。(3)、经过实验,猜想三验证成立。然后,小舟将溶液逐滴滴加到饱和溶液中(如图乙),先观察到红褐色沉淀产生,持续滴加后沉淀又消失了。请你解释沉淀会消失的原因。28. 小宁在课外资料中获悉:在锌和稀硫酸的反应中,加入硫酸铜溶液会影响反应的快慢。为此,他进行了探究。实验装置如图甲所示。【实验步骤】
①在规格相同的A、B试管中分别放入大小相近、数量相同的锌粒,胶头滴管吸入等量的溶液,如图甲所示。塞紧橡胶塞。
②将两个胶头滴管中的溶液同时挤入试管后,立即开启数据采集器。
③约后,停止采集数据。电脑显示气压p随时间t变化的关系如图乙。
 (1)、【实验分析】
(1)、【实验分析】图甲中“★”处应填。
(2)、要确保实验成功,实验前应检查反应装置的(3)、实验中,锌和稀硫酸反应的快慢通过采集到的试管内值的变化快慢来反映。【实验结论】
在锌和稀硫酸的反应中,加入硫酸铜溶液可以(填“减慢”或“加快”)反应速度。
29. 如图甲所示是我们常见的按压式圆珠笔。小明利用圆珠笔开展了以下实验研究。
实验一:研究弹簧弹力与压缩量的关系,实验数据记录如下表:
序号
钩码质量(g)
弹簧压缩量×(mm)
弹簧弹力F(N)
k
1
50
2
0.5
0.25
2
100
4
1
0.25
实验二:先将笔倒立向下按压然后放手,笔将向上弹起一定的高度。弹跳过程可以分为三个阶段:
①把笔竖直倒立于水平硬桌面,下压外壳使其下端接触桌面(见位置a);
②由静止释放,外壳竖直上升,弹簧恢复到原长(见位置b);
③笔继续上升到离桌面2cm的最高处(见位置c)开始下落。
(1)、实验一表中的“k”应该填入的项目是:;(2)、笔在上升过程中,笔的外壳的最大速度处于位置之间;(选填“ab”或“bc”)(3)、若不计一切摩擦,请说明从a到b到c位置笔的内芯的机械能变化情况?。四、解答题(本题有5小题,第30题6分,第31-33题各9分,第35小题12分,共45分)
-
30. 食盐是一种重要的化工原料,请回答下列问题。(1)、如图1为实验室除去粗盐中泥沙等难溶性杂质的实验步骤,其中操作I所用的玻璃仪器有:漏斗、烧杯和。
 (2)、由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等可溶性杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如图2.
(2)、由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等可溶性杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如图2.
①加BaCl2是为了除去;
②操作IV中加入一定量的盐酸调pH=7的目的是。
31. 工业上常采用“天然苛化法”制取氢氧化钠,部分流程如下: (1)、生产工艺中可以回收再利用的物质是。(2)、由天然碱得到碳酸钠溶液时,将天然碱粉碎的目的。(3)、制备氢氧化钠的化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。将530千克溶质质量分数为20%的碳酸钠溶液与足量的石灰乳混合,反应生成的氢氧化钠的质量为多少千克?32. 为测定某含有杂质的锌粒样品中锌的质量分数,取一定量锌粒样品于锥形瓶中,分3次每次加入100.0g溶质质量分数相同的稀硫酸,实验过程和数据如图所示。(杂质不参加反应)
(1)、生产工艺中可以回收再利用的物质是。(2)、由天然碱得到碳酸钠溶液时,将天然碱粉碎的目的。(3)、制备氢氧化钠的化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。将530千克溶质质量分数为20%的碳酸钠溶液与足量的石灰乳混合,反应生成的氢氧化钠的质量为多少千克?32. 为测定某含有杂质的锌粒样品中锌的质量分数,取一定量锌粒样品于锥形瓶中,分3次每次加入100.0g溶质质量分数相同的稀硫酸,实验过程和数据如图所示。(杂质不参加反应)请回答下列问题:
 (1)、第次加入100.0g稀硫酸过量。(2)、计算锌粒样品中锌的质量分数?(3)、实验后反思,锥形瓶中若有氢气残留,会导致锌的质量分数测量值(选填“偏大”、“不变”或“偏小”)。33. 某同学为探究铜铁合金中铁的质量分数,先后进行了四次实验,实验数据如表。请分析与计算:
(1)、第次加入100.0g稀硫酸过量。(2)、计算锌粒样品中锌的质量分数?(3)、实验后反思,锥形瓶中若有氢气残留,会导致锌的质量分数测量值(选填“偏大”、“不变”或“偏小”)。33. 某同学为探究铜铁合金中铁的质量分数,先后进行了四次实验,实验数据如表。请分析与计算:第一次
第二次
第三次
第四次
所取合金的质量/g
10
10
20
20
所加稀硫酸的质量/g
100
120
80
180
生成氢气的质量/g
0.2
0.2
0.2
X
(1)、表中X=;(2)、第次实验中,稀硫酸过量;(3)、求铜铁合金中铁的质量分数;(4)、求所加稀硫酸的溶质质量分数。34. 2021年5月15日“天问一号”火星探测器,成功软着陆于火星表面,实现了“绕和落”,不久首辆火星车“祝融号”也将驶离着陆平台,开展巡视探测等工作。如图所示为我国“天问一号”火星车。目前探明火星大气的密度约为地球的1%,火星重力约为地球重力的0.36倍。 (1)、若火星车的质量为240kg,在火星表面火星车受到的重力为;火星探测器降落到火星表面,需要用到降落伞减速,但是月球探测器降落到月球表面却不能用降落伞,其原因是。(2)、探测发射前,在水平地面上进行了测试,火星车匀速直线行驶240m用时60min,若车的质量为240kg,受到地面的摩擦阻力为300N,网状轮子与地面接触的总面积为0.04m2。
(1)、若火星车的质量为240kg,在火星表面火星车受到的重力为;火星探测器降落到火星表面,需要用到降落伞减速,但是月球探测器降落到月球表面却不能用降落伞,其原因是。(2)、探测发射前,在水平地面上进行了测试,火星车匀速直线行驶240m用时60min,若车的质量为240kg,受到地面的摩擦阻力为300N,网状轮子与地面接触的总面积为0.04m2。①火星车的行驶速度是多少?
②火星车对水平地面的压强为多少?
③火星车在地面行驶60min克服做了多少功?