“高效课堂”1.5 酸和碱之间发生的反应(基础版)--2023-2024学年浙教版科学九年级上册
试卷更新日期:2023-11-01 类型:同步测试
一、选择题
-
1. 如图所示是硫酸和氢氧化钠溶液反应时pH的变化图象,下列说法正( )
 A、图中a点所示溶液中,含有的溶质是硫酸钠和硫酸 B、图中b点时,硫酸和氢氧化钠恰好完全反应 C、图中c点所示溶液呈碱性 D、该实验是将氢氧化钠溶液滴到硫酸溶液中2. SO2是形成酸雨的主要物质,能有效吸收SO2的溶液是( )A、NaOH B、Na2SO4 C、H2SO4 D、NaCl3. 胃酸可以帮助食物的消化,但是胃酸过多,就会伤及胃、十二指肠黏膜,造成胃溃疡或十二指肠溃疡等疾病。药物治疗可以口服抑酸剂,饮食治疗可以适当食用的食物是( )A、苹果pH=3.4
A、图中a点所示溶液中,含有的溶质是硫酸钠和硫酸 B、图中b点时,硫酸和氢氧化钠恰好完全反应 C、图中c点所示溶液呈碱性 D、该实验是将氢氧化钠溶液滴到硫酸溶液中2. SO2是形成酸雨的主要物质,能有效吸收SO2的溶液是( )A、NaOH B、Na2SO4 C、H2SO4 D、NaCl3. 胃酸可以帮助食物的消化,但是胃酸过多,就会伤及胃、十二指肠黏膜,造成胃溃疡或十二指肠溃疡等疾病。药物治疗可以口服抑酸剂,饮食治疗可以适当食用的食物是( )A、苹果pH=3.4 B、萝卜pH=4.6
B、萝卜pH=4.6  C、土豆pH=5.4
C、土豆pH=5.4  D、板栗pH=8.8
D、板栗pH=8.8  4. 关于中和反应的说法,错误的是( )A、一定是复分解反应 B、一定有氧化物生成 C、一定是放热反应 D、一定没有沉淀生成5. 下列关于酸和碱反应的说法中,错误的是( )A、酸碱的反应要放出热量 B、酸碱的反应一定有盐生成 C、酸碱的反应一定有水生成 D、酸碱恰好完全反应后溶液的pH=06.
4. 关于中和反应的说法,错误的是( )A、一定是复分解反应 B、一定有氧化物生成 C、一定是放热反应 D、一定没有沉淀生成5. 下列关于酸和碱反应的说法中,错误的是( )A、酸碱的反应要放出热量 B、酸碱的反应一定有盐生成 C、酸碱的反应一定有水生成 D、酸碱恰好完全反应后溶液的pH=06.根据图,判断以下说法错误的是( )
 A、取液后的滴管不能倒置 B、用玻璃棒搅拌使反应充分 C、用酚酞溶液判断该反应是否发生 D、生成盐和水的反应都是中和反应7. 家庭生活中一些常见物质的pH如下:
A、取液后的滴管不能倒置 B、用玻璃棒搅拌使反应充分 C、用酚酞溶液判断该反应是否发生 D、生成盐和水的反应都是中和反应7. 家庭生活中一些常见物质的pH如下:物质
食醋
牛奶
食盐水
牙膏
肥皂水
pH
2~3
6~7
7
8~9
9~10
当我们被蚊虫叮咬后,蚊虫能在人的皮肤内分泌蚁酸(具有酸的性质),从而使皮肤肿痛。要减轻痛痒,应在叮咬处涂抹下列物质中的( )
A、食醋 B、牛奶 C、食盐水 D、牙膏或肥皂水8. 推理是化学学习中一种重要的方法,但应具体问题具体对待,否则就会产生错误的结论。下列推理中结论正确的是( )A、酸与碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 B、原子在化学变化中不能再分,则分子在化学变化中也不能再分 C、点燃H2与O2的混合气体可能爆炸,则点燃CH4与O2的混合气体也可能爆炸 D、CuO不能与水反应,则CaO也不能与水反应9. 稀NaOH溶液与稀盐酸反应过程中温度和pH的变化如图所示,下列说法正确的是( )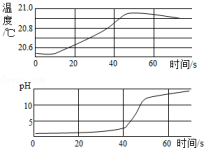 A、该实验是将稀NaOH溶液滴入稀盐酸 B、稀NaOH溶液与稀盐酸反应为吸热反应 C、40s时,溶液中溶质为HCl、NaOH和NaCl D、在20s到40s之间某一时刻,两溶液恰好完全反应10. 稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,下列操作及实验现象(或结果),不能证明反应发生的是( )
A、该实验是将稀NaOH溶液滴入稀盐酸 B、稀NaOH溶液与稀盐酸反应为吸热反应 C、40s时,溶液中溶质为HCl、NaOH和NaCl D、在20s到40s之间某一时刻,两溶液恰好完全反应10. 稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,下列操作及实验现象(或结果),不能证明反应发生的是( ) A、在混合液中加金属Zn,无气泡产生 B、在混合液中加无色酚酞,溶液呈无色 C、在混合液中加AgNO3溶液,有白色沉淀 D、用pH试纸测混合液的pH,测得pH=7
A、在混合液中加金属Zn,无气泡产生 B、在混合液中加无色酚酞,溶液呈无色 C、在混合液中加AgNO3溶液,有白色沉淀 D、用pH试纸测混合液的pH,测得pH=7二、填空题
-
11. 用下列物质前的序号填空。
①食盐②熟石灰③稀盐酸④氢氧化铝⑤甲烷
(1)、工业上通常用来除铁锈的是。(2)、医疗上可用于治疗胃酸过多的是。(3)、农业上可用来改良酸性土壤的是。12. 硫酸和盐酸时实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.(1)它们水溶液的pH都7(填“>”、“=”或“<”符合).
(2)它们都能除铁锈,写出盐酸与铁锈的主要成分反应的化学方程式: .
(3)它们都能与碱反应生成盐和水,该类反应叫反应.
(4)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是盛有的试剂瓶.
(5)写出把硫酸转化为盐酸的化学方程式: .
13. 盐酸、硫酸、氢氧化钠和氢氧化钙是初中化学中常见的物质,它们有着较广泛的用途.(1)酸与碱之间能发生 反应,写出一个上述四种物质之间能发生反应的化学方程式: .
(2)氢氧化钙可以用来调节土壤的 性,它的水溶液常用来检验气体的存在.
(3)将一定量的稀硫酸与氢氧化钠溶液混合,滴入几滴酚酞溶液,混合液显红色,可推断该溶液的pH7(填“>”、“<”或“=”).要准确测定该溶液的pH,需要用到的仪器是 .
14.分类、类比是学习化学变化常用的方法.
(1)初中化学有许多实验,若按照实验主要目的可将实验分为:探究化学反应前后物质的质量关系、探究物质的性质、探究物质的含量等.据此应将下列实验中的D与 (填“A”或“B”或“C”)归为一类,依据是 .


A
B


C
D
(2)许多物质的命名与元素的化合价高地有关,如锰酸钾、高锰酸钾,其中锰元素的化合价分别为+6、+7.氯元素常见的化合价有+7、+5、+1、﹣1等,由此推测钠元素、氧元素和+7价氯元素三种元素组成的化合物的名称为 , 化学式为 .
三、实验探究题
-
15. 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
(1)、【学生板演】该反应的化学方程式 .(2)、【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下,请你补上猜想四.
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH
猜想四:
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是 ,
理由是 .
(3)、【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有 .
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用了老师提供的pH试纸、Na2CO3溶液、BaCl2溶液,进行如下三个方案的探究.
实验方案
测溶液的pH
滴加Na2CO3溶液
滴加BaCl2溶液
实验操作



实验现象
试纸变色,对比比色卡,pH<7
产生白色沉淀
实验结论
溶液中有H2SO4
溶液中有H2SO4
溶液中有H2SO4
(4)、【得出结论】通过探究,全班同学一致确定猜想二是正确的.【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予了肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了如下两处错误:
①实验操作中的错误是 ;
②实验方案中也有一个是错误的,错误的原因是 .
四、解答题
-
16. 酸和碱反应是一类重要的化学反应。某同学利用图1实验研究稀盐酸与氢氧化钠溶液反应的过程,并测量反应过程中溶液的pH和温度的变化情况,得到图2和图3,请回答下列问题:
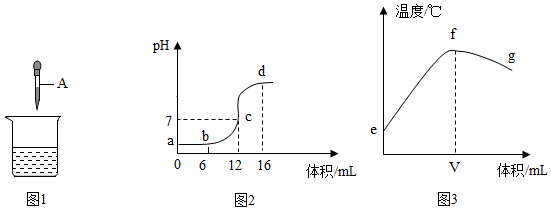 (1)、胶头滴管中A溶液的溶质是:(填化学式)。(2)、要配制50克15%的稀盐酸,需要质量分数为30%的浓盐酸克。(3)、该兴趣小组同学推断出图3中V的值为12,他的理由是:。(4)、下列说法正确的是____。A、图2中b点所示溶液中的溶质是NaCl和HCl B、取图2中d点所示溶液加热蒸干所得固体为纯净物 C、图2中c→d所示溶液中NaCl的质量不断增加 D、图3中e→f变化趋势可说明该反应是放热反应17. 科学小组利用图1装置研究酸碱中和反应,选用溶质质量分数为3.65%的稀盐酸与100g氢氧化钾溶液进行反应,图2和图3分别是用pH传感器和温度传感器精确测量反应过程中相关量的变化情况。
(1)、胶头滴管中A溶液的溶质是:(填化学式)。(2)、要配制50克15%的稀盐酸,需要质量分数为30%的浓盐酸克。(3)、该兴趣小组同学推断出图3中V的值为12,他的理由是:。(4)、下列说法正确的是____。A、图2中b点所示溶液中的溶质是NaCl和HCl B、取图2中d点所示溶液加热蒸干所得固体为纯净物 C、图2中c→d所示溶液中NaCl的质量不断增加 D、图3中e→f变化趋势可说明该反应是放热反应17. 科学小组利用图1装置研究酸碱中和反应,选用溶质质量分数为3.65%的稀盐酸与100g氢氧化钾溶液进行反应,图2和图3分别是用pH传感器和温度传感器精确测量反应过程中相关量的变化情况。 (1)、分析图像可知,实验前图1烧杯中所盛溶液乙是(填“稀盐酸”或“氢氧化钾”)。(2)、图2中c点应与图3中的(填“b”、“e”或“f”)点对应。(3)、根据相关数据计算氢氧化钾溶液中溶质的质量分数(写出计算过程)。
(1)、分析图像可知,实验前图1烧杯中所盛溶液乙是(填“稀盐酸”或“氢氧化钾”)。(2)、图2中c点应与图3中的(填“b”、“e”或“f”)点对应。(3)、根据相关数据计算氢氧化钾溶液中溶质的质量分数(写出计算过程)。
-