人教版初中化学2023-2024学年九年级上学期课堂达标训练试卷 第二单元 课题3 制取氧气 (一)
试卷更新日期:2023-10-26 类型:同步测试
一、单选题
-
1. 研究表明,许多金属氧化物对氯酸钾的分解有催化作用。下表是不同金属氧化物作催化剂,使氯酸钾剧烈反应时的温度:
氧化物
Fe2O3
Al2O3
CuO
MgO
剧烈反应
时的温度
490℃
540℃
350℃
545℃
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用( )A、Fe2O3 B、Al2O3 C、CuO D、MgO2. 下列反应属于分解反应的是( )A、硫 + 氧气 二氧化硫 B、酒精 + 氧气 二氧化碳 + 水 C、高锰酸钾 锰酸钾 + 二氧化锰 + 氧气 D、铜 + 氧气 氧化铜3.如图所示的装置,其中可以收集氧气的是( )
 A、① 和② B、② 和 ③ C、① 和 ④ D、① 和 ⑤4. 用向上排空气法收集氧气,检验氧气是否集满的最简便的方法是( )A、看集气瓶口是否有气体冒出 B、将带火星的木条伸入集气瓶中,看木条是否复燃 C、将带火星的木条伸到集气瓶口,看木条是否复燃 D、倒入澄清的石灰水,看是否变浑浊5. 用“W”形玻璃管进行微型实验。将注射器中的过氧化氢溶液推入管中与二氧化锰接触,下列说法不正确的是( )
A、① 和② B、② 和 ③ C、① 和 ④ D、① 和 ⑤4. 用向上排空气法收集氧气,检验氧气是否集满的最简便的方法是( )A、看集气瓶口是否有气体冒出 B、将带火星的木条伸入集气瓶中,看木条是否复燃 C、将带火星的木条伸到集气瓶口,看木条是否复燃 D、倒入澄清的石灰水,看是否变浑浊5. 用“W”形玻璃管进行微型实验。将注射器中的过氧化氢溶液推入管中与二氧化锰接触,下列说法不正确的是( )
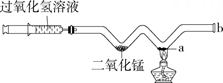 A、过氧化氢溶液遇到二氧化锰,立刻产生大量气泡 B、若a处粉末是木炭粉,能看到白光 C、若a处粉末是镁粉,b处会出现白雾 D、若a处粉末是铜粉,能看到粉末由红色变为黑色6. 实验室利用分解过氧化氢制氧气时,忘记加入二氧化锰,其结果是( )
A、过氧化氢溶液遇到二氧化锰,立刻产生大量气泡 B、若a处粉末是木炭粉,能看到白光 C、若a处粉末是镁粉,b处会出现白雾 D、若a处粉末是铜粉,能看到粉末由红色变为黑色6. 实验室利用分解过氧化氢制氧气时,忘记加入二氧化锰,其结果是( )
A、不能产生氧气 B、生成氧气的速率慢 C、产生氧气的总量减少 D、过氧化氢不能分解7. 利用下列原理制取氧气,具有反应快、操作简便、能耗少、无污染的是( )
A、高锰酸钾 锰酸钾+二氧化锰+氧气 B、氧化汞 汞+氧气 C、氯酸钾 氯化钾+氧气 D、过氧化氢 水+氧气8. 实验室用加热高锰酸钾或双氧水与二氧化锰混合的方法制取氧气,其共同点是( )A、都需要加热 B、都使用二氧化锰作催化剂 C、都发生了分解反应 D、都生成了两种物质9. 工业上制取大量氧气的方法是( )A、加热氯酸钾 B、加热高锰酸钾 C、分离液态空气 D、加热二氧化锰10. 下列有关催化剂的说法中正确的是( )A、二氧化锰可使氯酸钾在较低温度下产生氧气 B、催化剂能加快物质的反应速率 C、二氧化锰是所有反应的催化剂 D、加入二氧化锰可使氯酸钾产生更多的氧气二、填空题
-
11. 由于氧气的密度比空气 , 收集氧气可用法。由于氧气溶于水,收集氧气可用法。要得到纯净的氧气最好选用法收集。
12. 检验氧气的方法:将的木条伸入集气瓶中,若木条则证明集气瓶中的气体是氧气。
13. 工业上制备大量的氧气是采用的方法,其原理是利用液态氮的沸点比液态氧的沸点的性质.蒸发液态空气时,首先蒸发出来,剩下的主要是.此变化属于.工业上为了便于贮存.运输和使用,常把氧气加压到1.5×107 Pa,并贮存在钢瓶中.14. 收集氧气可采用排水法,是因为 , 排水法收集氧气时不需验满,看到瓶口气泡向外冒,表示氧气已收集满;氧气还可采用向上排空气法,是因为 , 用向上排空气法收集氧气需验满,将带火星的木条置于瓶口,木条复燃,氧气已收集满。15. 在实验室里加热氯酸钾制氧气,为了加快反应速率常选用二氧化锰作催化剂,当氯酸钾完全分解后,试管里的固体物质是和;在这个反应前后,二氧化锰的和都没有改变.
三、简答题
-
16. 某同学在实验室里用高锰酸钾和二氧化锰加热制取氧气,实验结束时发现大试管已破裂,请你帮他分析造成试管破裂的可能原因是什么?(写出三条即可)17. 用向上排空气法收集氧气时,怎样证明瓶内的氧气已收集满?
四、综合题
-
18. 我们人类每时每刻都离不开空气,没有空气就没有生命,也没有生机勃勃的地球。(1)、空气中稀有气体的体积分数约为(用百分比表示)。(2)、下列过程中,能产生氧气的有(填字母)。
 (3)、潜水员水下作业时要携带“富氧空气”,是因为氧气能。(4)、空气是工业上制取大量氧气的原料,空气中主要组分的沸点如下表:
(3)、潜水员水下作业时要携带“富氧空气”,是因为氧气能。(4)、空气是工业上制取大量氧气的原料,空气中主要组分的沸点如下表:组分
氮气
氧气
二氧化碳
沸点/℃
-195.8
-183.0
-78.5
工业制氧气是根据空气中氧气和氮气的不同,此过程属于(填“物理”或“化学”)变化。将液态空气升温,最先逸出的物质主要是(填化学符号)。
五、实验探究题
-
19. 实验学校的同学们在学习了催化剂的知识后提出:氧化铁固体(Fe2O3 , 难溶于水)在双氧水制氧气的反应中能否起到类似二氧化锰的催化作用呢?于是进行了以下探究:(1)、【猜想】
Ⅰ、Fe2O3既不是催化剂,也不是反应物,反应前后质量和化学性质不变;
Ⅱ、Fe2O3是反应物,要生成O2 , 反应前后质量和化学性质要改变;
Ⅲ、Fe2O3是该反应的催化剂,反应前后 ;
(2)、【实验】用天平称量1g Fe2O3固体,取10mL10%的双氧水于试管中,进行实验:

实验过程中记录现象如下:步骤①现象
步骤③现象
步骤⑥
结论
无明显变化
称得固体质量为1g
猜想Ⅲ成立.
(3)、老师指出上述实验不能证明Fe2O3是该反应的催化剂,理由是 ____ ;A、只有二氧化锰能起催化作用 B、未验证回收的固体是否仍是Fe2O3 C、未验证回收的固体的物理性质 D、未验证Fe2O3是否改变反应速率(4)、Fe2O3催化分解双氧水的化学反应式为 ;(5)、步骤③中,试管中各物质质量随反应时间t变化曲线正确的是 20. 某化学实验兴趣小组的同学欲制取并探究氧气的化学性质,请你帮助他们完成下列任务。
20. 某化学实验兴趣小组的同学欲制取并探究氧气的化学性质,请你帮助他们完成下列任务。
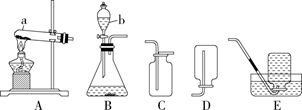 (1)、写出标号a、b仪器的名称:a , b。(2)、现有如下几种物质:A.氯化钠(NaCl);B.氯酸钾(KClO3);C.水(H2O);D.过氧化氢(H2O2);E.甲烷(CH4)。从元素组成角度推测,上述物质中能制得氧气的是(填字母)。(3)、写出用过氧化氢溶液和二氧化锰制取氧气的符号表达式: , 其中,二氧化锰起作用。(4)、若用氯酸钾和二氧化锰的固体混合物制取并收集一瓶纯净的氧气,所选择的装置为(填字母)。(5)、该小组同学利用制得的氧气,进行了如图三个实验。
(1)、写出标号a、b仪器的名称:a , b。(2)、现有如下几种物质:A.氯化钠(NaCl);B.氯酸钾(KClO3);C.水(H2O);D.过氧化氢(H2O2);E.甲烷(CH4)。从元素组成角度推测,上述物质中能制得氧气的是(填字母)。(3)、写出用过氧化氢溶液和二氧化锰制取氧气的符号表达式: , 其中,二氧化锰起作用。(4)、若用氯酸钾和二氧化锰的固体混合物制取并收集一瓶纯净的氧气,所选择的装置为(填字母)。(5)、该小组同学利用制得的氧气,进行了如图三个实验。①实验二中,铁丝在氧气中燃烧的现象为。
②通过上述实验探究,发现可燃物在氧气中燃烧比在空气中燃烧更剧烈。请从微观角度进行解释:。
 (6)、实验结束后,同学们进行了以下反思,你认为正确的观点有____(填字母)。A、可根据反应物的状态和反应条件,选择适当的发生装置 B、可根据气体的密度(与空气密度相比较)和在水中的溶解性,选择气体的收集方法 C、氧气是一种化学性质比较活泼的气体,能与很多物质发生氧化反应
(6)、实验结束后,同学们进行了以下反思,你认为正确的观点有____(填字母)。A、可根据反应物的状态和反应条件,选择适当的发生装置 B、可根据气体的密度(与空气密度相比较)和在水中的溶解性,选择气体的收集方法 C、氧气是一种化学性质比较活泼的气体,能与很多物质发生氧化反应
-