福建省福州市鼓楼区重点中学2023年中考化学模拟试卷
试卷更新日期:2023-10-23 类型:中考模拟
一、选择题
-
1. 化学使世界变得绚丽多彩。生活中的下列变化没有化学变化发生的是( )A、节日燃放焰火 B、木炭烤熟食物 C、西瓜榨成西瓜汁 D、檀树皮制成宣纸2. 材料在人类生产、生活中有着重要的作用。下列对材料的分类判断正确的是( )A、陶瓷属于合成材料 B、棉线、蚕丝属于天然纤维 C、塑料属于无机非金属材料 D、玻璃钢属于金属材料3. 下列实验操作正确的是( )A、
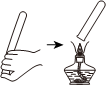 氢气验纯
B、
氢气验纯
B、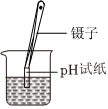 测溶液的
C、
测溶液的
C、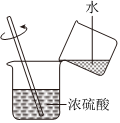 浓硫酸稀释
D、
浓硫酸稀释
D、 滴加液体
4. 对下列事实或做法的解释中,正确的是( )A、氧气能被液化贮存于钢瓶中-----分子间有间隔且间隔能改变 B、用嘴吹灭燃着的蜡烛----降低蜡烛的着火点 C、用明矾净化天然水----降低水中的钙、镁离子含量 D、将食品放入冰箱里防止变质----分子运动速率随温度降低而减慢5. 如图表示、、三种物质的溶解度曲线,下列说法错误的是( )
滴加液体
4. 对下列事实或做法的解释中,正确的是( )A、氧气能被液化贮存于钢瓶中-----分子间有间隔且间隔能改变 B、用嘴吹灭燃着的蜡烛----降低蜡烛的着火点 C、用明矾净化天然水----降低水中的钙、镁离子含量 D、将食品放入冰箱里防止变质----分子运动速率随温度降低而减慢5. 如图表示、、三种物质的溶解度曲线,下列说法错误的是( ) A、中含有少量 , 用海水晒盐的原理提纯 B、时,三种物质的饱和溶液升温到 , 溶液中溶质质量分数的大小关系是 C、时,、的饱和溶液降温到 , 析出晶体较多的是 D、时,等质量的、分别配成该温度下的饱和溶液,所得溶液质量6. 剧烈运动会感到肌肉酸痛,是因为体内产生大量乳酸化学式为的缘故。下列关于的叙述错误的是( )A、是一种有机物 B、由三种元素组成 C、一个分子中共有个原子 D、中、、的质量比为::7. 归纳法是一种重要的学习方法,可以将零散知识结构化、系统化,下列知识归纳都正确的一组是 ( )
A、中含有少量 , 用海水晒盐的原理提纯 B、时,三种物质的饱和溶液升温到 , 溶液中溶质质量分数的大小关系是 C、时,、的饱和溶液降温到 , 析出晶体较多的是 D、时,等质量的、分别配成该温度下的饱和溶液,所得溶液质量6. 剧烈运动会感到肌肉酸痛,是因为体内产生大量乳酸化学式为的缘故。下列关于的叙述错误的是( )A、是一种有机物 B、由三种元素组成 C、一个分子中共有个原子 D、中、、的质量比为::7. 归纳法是一种重要的学习方法,可以将零散知识结构化、系统化,下列知识归纳都正确的一组是 ( )A、物质类型与组成
B、化学与生活
纯碱、烧碱都是碱
煤、石油、天然气都含有碳元素
冰箱中放入活性炭可消除异味
洗涤剂具有乳化作用可清洗餐具油污
C、物质与使用
D、化学与健康
生活中常用肥皂水软化硬水
铵态氮肥不能与草木灰碱性混用
人体缺维生素易患坏血病
儿童缺锌引起食欲不振发育不良
A、 B、 C、 D、8. 关于下列实验的说法正确的是 ( )



A、图中可依据产生大量白烟这一现象,可得出氧气约占空气总体积的五分之一
B、向图中加硝酸铵固体,型管液面左低右高,说明硝酸铵溶于水放热
C、对比图中铜片上红磷和白磷,可得出燃烧需要温度达到着火点的结论
D、探究溶解度的影响因素
A、 B、 C、 D、9. 日常生活或化学实验中,鉴别以下物质的方法不正确的是 ( )选项
待鉴别的物质
鉴别方法
硬水与软水
加肥皂水,搅拌,观察产生泡沫的多少
黄铜与黄金
灼烧,观察颜色是否变黑
一氧化碳与二氧化碳
通入澄清石灰水中,观察澄清石灰水是否变浑浊
碳粉与铁粉
加水,观察是否溶解于水
A、 B、 C、 D、10. 小明同学利用进行了一系列实验并绘制了如下坐标图像,其图像的变化趋势与对操作不相符的是( )A、 向一定量水中加入一定量的固体
B、
向一定量水中加入一定量的固体
B、 将硫酸铜溶液逐滴加入一定量溶液中
C、
将硫酸铜溶液逐滴加入一定量溶液中
C、 将稀盐酸逐滴加入一定量溶液中
D、
将稀盐酸逐滴加入一定量溶液中
D、 向一定量溶液中通入
向一定量溶液中通入
二、非选择题
-
11. 金属的广泛使用,与我们生活息息相关。(1)、在空气中 制品填“铝”或“铁”更耐腐蚀。(2)、人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度 填“大”或“小”。(3)、生铁和钢都是铁的合金,二者性能不同的原因是 。(4)、重铬酸钾可用于测试酒驾,重铬酸钾中铬元素的化合价为 。(5)、仅用下列试剂验证铝、铁、铜这三种金属的活动性顺序,能达到目的的是 ____ 填序号。A、硫酸铝溶液 B、硫酸亚铁溶液 C、硫酸铜溶液12. 研究“水”可从多角度展开。(1)、水的电解

宏观现象:按图所示装置,通电一段时间后,试管、中产生气体的体积比约为 。
微观分析:该反应中发生分解的微粒名称是 。
结论:水由 组成。
(2)、水的性质将黄豆粒大小的金属钾放入盛有水的烧杯中,生成;在反应后的溶液中滴入酚酞试液,溶液变红。写出该反应的化学方程式 。(3)、水的用途碘与锌在常温下反应速度很慢,若滴入几滴水则反应剧烈,水在此的作用是 。
下列实验中,对水的主要作用分析不全面的是 填字母。

A.图中的水便于观察烧瓶内气压变化
B.图中的水提供热量
C.图集气瓶中的水排尽空气且便于观察何时集满
D.图中的水可防止熔融物炸裂集气瓶
13. 新华网年月日报道,我国学者研发出一种新型铂单原子催化剂,可将高效转化为纯度以上的甲醇化学式为。如图为转化成甲醇的微观示意图: (1)、Ⅰ“宏观辨识与微观探析”是化学核心素养之一。
(1)、Ⅰ“宏观辨识与微观探析”是化学核心素养之一。
甲物质属于 选填“混合物”、“氧化物”或“单质”。(2)、表示丁物质的方框内粒子图示应为图中的 填序号。 (3)、从图中可知,化学变化中不变的微粒是 填“分子”或“原子”。(4)、写出表示该反应的化学方程式为 。(5)、该方法的现实意义在于 写出一点即可。(6)、Ⅱ科学家研制出一种以元素锶的原子做钟摆的钟,是世界上最精确的钟。图是锶元素在元素周期表中的相关信息。图是锶元素形成的一种粒子的结构示意图。
(3)、从图中可知,化学变化中不变的微粒是 填“分子”或“原子”。(4)、写出表示该反应的化学方程式为 。(5)、该方法的现实意义在于 写出一点即可。(6)、Ⅱ科学家研制出一种以元素锶的原子做钟摆的钟,是世界上最精确的钟。图是锶元素在元素周期表中的相关信息。图是锶元素形成的一种粒子的结构示意图。
锶元素的相对原子质量为 。(7)、图中的 ,该粒子的符号是 。14. 酸、碱、盐是几类重要化合物,它们与人类日常生活和工农业生产关系十分密切。(1)、盐酸和硫酸具有相似的性质,是因为它们在溶液中都能电离出 填符号。(2)、由熟石灰和硫酸铜配制的波尔多液不能用铁桶来装的原因是 用化学方程式解释。(3)、如图是氢氧化钠溶液与盐酸反应的微观粒子示意图,由示意图可知,参加反应的微粒是 。(4)、敞口放置的氢氧化钠溶液变质后,生成纯碱。纯碱的化学式为 ;纯碱的一种用途是 。若将部分变质的氢氧化钠溶液的杂质去除,你选择的试剂是 。 15.(1)、Ⅰ实验一:如图是配制溶质质量分数为的溶液的操作示意图。
15.(1)、Ⅰ实验一:如图是配制溶质质量分数为的溶液的操作示意图。
配制一定质量分数溶液的步骤为:计算 量取 装瓶;填空主要步骤 (2)、A处有一个明显的错误是 ;(3)、D处量筒的规格应选用 选或;(4)、实验反思:下列情况会导致所配溶液中溶质的质量分数偏高的是 填字母。
(2)、A处有一个明显的错误是 ;(3)、D处量筒的规格应选用 选或;(4)、实验反思:下列情况会导致所配溶液中溶质的质量分数偏高的是 填字母。A.氯化钠中混有少量杂质
B.称量时氯化钠和砝码位置放反了使用了游码
C.用于溶解氯化钠的烧杯洗净后残留有少量的水
D.用量筒取水时,俯视读数
(5)、实验二:配制一定溶质质量分数的盐酸:
根据浓盐酸试剂瓶上标签的部分内容,现要配制的稀盐酸 , 需要这种浓盐酸的质量是 , 需加水的质量是 。 (6)、Ⅱ氧化锌可作为紫外线吸收剂应用于化妆品中,其一种生产工艺如图所示:
(6)、Ⅱ氧化锌可作为紫外线吸收剂应用于化妆品中,其一种生产工艺如图所示:
据图分析并回答下列问题:推测草酸的化学式是 。(7)、“沉锌”过程中发生复分解反应,反应的化学方程式为 。(8)、“操作”的名称是 。16. 实验室制取气体时需要的一些装置如图所示,请回答下列问题。 (1)、写出标有序号的仪器名称: 。(2)、实验室制取氧气和二氧化碳的发生装置都可选用 ,装置中使用分液漏斗的优点是 ,写出实验室制取二氧化碳的化学方程式 。(3)、若要得到干燥的氧气,所选择装置的连接顺序为: 填字母序号。(4)、某兴趣小组的同学连接、、装置进行实验。若实验时装置中蜡烛燃烧更剧烈,装置中溶液变浑浊,则装置中反应的化学方程式为 。17. 叠氮化钠被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究。
(1)、写出标有序号的仪器名称: 。(2)、实验室制取氧气和二氧化碳的发生装置都可选用 ,装置中使用分液漏斗的优点是 ,写出实验室制取二氧化碳的化学方程式 。(3)、若要得到干燥的氧气,所选择装置的连接顺序为: 填字母序号。(4)、某兴趣小组的同学连接、、装置进行实验。若实验时装置中蜡烛燃烧更剧烈,装置中溶液变浑浊,则装置中反应的化学方程式为 。17. 叠氮化钠被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究。【查阅资料】
受撞击会生成、。
遇盐酸、溶液没有气体生成。
碱石灰是和 的混合物。
的制备方法是:将金属钠与液态氨反应制得 , 再将与反应可生成、和。
【问题探究】
(1)、汽车经撞击后,毫秒内引发迅速分解,写出该反应的化学方程式 。(2)、工业级中常含有少量的 , 写出生成的化学方程式 。(3)、为测定某工业级样品中含有的质量分数,小组同学设计了如图实验装置。
小明同学认为通过测定装置Ⅰ中反应前后的质量差,再通过相应计算,就可测定的纯度,小组同学通过讨论装置Ⅰ认为很多因素会导致测定数据不准确,误差太大。
小明同学在大家讨论的基础上,又设计了装置Ⅱ。
请分析:装置Ⅱ中的作用是 ;若无装置 , 对测定结果造成的影响是 填“偏大”、“偏小”或“无影响”;装置的作用是 。
18. “十四五”期间,我国将独立完成“天宫二号”空间实验室建造。建造舱段使用的新型铝基碳化硅复合材料是由颗粒状的铝和碳化硅(SiC)复合而成的。一位科技爱好者自研了一种铝基碳化硅复合材料,为了分析其中铝的质量分数,该科技爱好者取了10g样品溶于足量稀硫酸,所得实验数据如图所示。已知:碳化硅既不溶于水和酸,也不与二者反应。请回答下列问题:
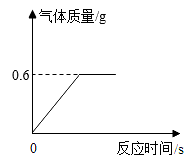 (1)、当样品中的铝完全反应时,生成的气体质量为g。(2)、样品中铝的质量分数为多少?(写出完整解题过程)。
(1)、当样品中的铝完全反应时,生成的气体质量为g。(2)、样品中铝的质量分数为多少?(写出完整解题过程)。