福建省福州市2023年中考化学质检试卷
试卷更新日期:2023-10-23 类型:中考模拟
一、选择题
-
1. 近年来我国科学进展的项目中,属于化学研究范畴的是( )A、全新原理电解海水制氢 B、珠穆朗玛峰新高程测定 C、嫦娥五号月面自动采样 D、雷达探测火星浅表结构2. 人体运动出汗后饮用淡盐水,补充的营养素除水外还有( )A、油脂 B、无机盐 C、蛋白质 D、维生素3. 我国自主研发产品中,采用的材料属于合成材料的是( )A、“福建舰”舰体合金钢 B、“极目一号”浮空艇艇体复合材料 C、舱外航天服合成橡胶 D、“祝融号”火星车热控器二氧化硅4. 实验室制取氧气的部分操作中,正确的是( )A、
 连接
B、
连接
B、 加热
C、
加热
C、 收集
D、
收集
D、 验满
5. 下列有关燃烧和灭火的说法错误的是( )A、油锅起火用水浇灭 B、星火燎原使温度达到可燃物的着火点 C、釜底抽薪移走可燃物 D、架空篝火增大可燃物与氧气接触面积6. 空间站处理的一种原理为 , 的化学式为( )A、 B、 C、 D、7. 稳定碘碘可用于阻止或减少甲状腺对放射性碘的吸收。如图为碘在元素周期表中的相关信息及其原子结构示意图,下列说法正确的是( )
验满
5. 下列有关燃烧和灭火的说法错误的是( )A、油锅起火用水浇灭 B、星火燎原使温度达到可燃物的着火点 C、釜底抽薪移走可燃物 D、架空篝火增大可燃物与氧气接触面积6. 空间站处理的一种原理为 , 的化学式为( )A、 B、 C、 D、7. 稳定碘碘可用于阻止或减少甲状腺对放射性碘的吸收。如图为碘在元素周期表中的相关信息及其原子结构示意图,下列说法正确的是( ) A、的数值为 B、碘原子的质子数为 C、个碘原子质量为 D、碘原子在化学反应中易失去电子8. 甲、乙两种固体物质均不含结晶水的溶解度曲线如图。下列说法正确的是( )
A、的数值为 B、碘原子的质子数为 C、个碘原子质量为 D、碘原子在化学反应中易失去电子8. 甲、乙两种固体物质均不含结晶水的溶解度曲线如图。下列说法正确的是( )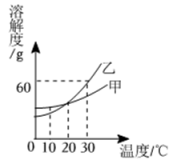 A、时,甲的溶解度小于乙 B、若乙中含少量甲,可用蒸发结晶法提纯乙 C、时,甲、乙饱和溶液溶质的质量相等 D、时,将乙充分溶解于水中,得到溶液9. 下列实验能达到目的的是( )A、
A、时,甲的溶解度小于乙 B、若乙中含少量甲,可用蒸发结晶法提纯乙 C、时,甲、乙饱和溶液溶质的质量相等 D、时,将乙充分溶解于水中,得到溶液9. 下列实验能达到目的的是( )A、 软化硬水
B、
软化硬水
B、 分离酒精和水
C、
分离酒精和水
C、 比较三种金属活动性
D、
比较三种金属活动性
D、 检验碳酸盐
10. 二氧化锰因应用广泛而备受关注。某研究小组采用图装置制取 , 反应原理为 , 石英管内剩余固体的质量和成分随温度的变化如图。据图分析,下列说法正确的是 ( )
检验碳酸盐
10. 二氧化锰因应用广泛而备受关注。某研究小组采用图装置制取 , 反应原理为 , 石英管内剩余固体的质量和成分随温度的变化如图。据图分析,下列说法正确的是 ( ) A、实验结束时先停止通入空气再停止加热 B、温度越高剩余固体中锰元素质量分数越高 C、制备二氧化锰须控制反应温度高于 D、时,固体减少的质量即为生成二氧化碳的质量
A、实验结束时先停止通入空气再停止加热 B、温度越高剩余固体中锰元素质量分数越高 C、制备二氧化锰须控制反应温度高于 D、时,固体减少的质量即为生成二氧化碳的质量二、非选择题
-
11. 文化传承,“化”说非遗。(1)、传统技艺榕城三绝即寿山石雕、脱胎漆器和软木画。
寿山石的主要成分是 , 该物质由 种元素组成。
脱胎漆器的修饰过程中,需要往大漆中添加银粉。银在自然界中能以单质形式存在的原因是 。
软木画以栓皮栎树的木栓层作主要原料。栓皮栎是喜光树种,进行光合作用时能量转化形式为:太阳能 。
(2)、传统民俗正月廿九日是福州传统的“拗九节”。熬煮“拗九粥”的食材有:糯米、花生、桂圆、红枣、蔗糖、芝麻等。花生根瘤菌繁育的范围为至 , 则花生适宜在 填“酸性”或“碱性”土壤中生长。
红糖与白糖的主要成分均为蔗糖。利用活性炭的 性,可将红糖脱色为白糖。蔗糖在氧气中燃烧生成二氧化碳和水,则蔗糖中一定含有的元素是 。
黑芝麻富含钙、铁等元素。适量食用黑芝麻可预防缺 填“钙”或“铁”引发的贫血。
12. 磷元素是人类发现的第一种元素。(1)、德国炼金术师布兰德最先从尿液含等中炼出白磷,该过程发生 填“物理变化”或“化学变化”。(2)、白磷隔绝空气加热到时变为红磷。白磷在隔绝空气高压加热后急速冷却,可得到有金属光泽的黑磷,黑磷的结构、性质与石墨相似。下列叙述正确的是 ____ 填标号。A、黑磷能导电 B、黑磷能在空气中自燃 C、红磷、白磷和黑磷均为单质(3)、中国科学家首次在月球上发现新矿物“嫦娥石”,它是一种新的磷酸盐矿物,主要成分为 , 其中磷、氧的原子数目比为 填最简比。(4)、发令枪的火药由氯酸钾和红磷混合制成,撞击后发生剧烈反应,发出响声并产生白烟成分为氯化钾和五氧化二磷 , 该反应的化学方程式为 。(5)、磷酸二氢钙是一种高效肥料,属于 填“磷肥”或“复合肥”。13. 铁是人类广泛使用的金属。(1)、识铁人类最早发现铁源自陨石。某铁陨石中含铁以及镍、钴等,则铁陨石属于 填“纯净物”或“混合物”。
(2)、炼铁古代中国冶铁的原理;高温熔化铁矿如赤铁矿主要含氧化铁过程中,不断加入木炭粉,可炼得生铁,同时生成二氧化碳,则该反应属于 填基本反应类型。
(3)、锈蚀利用如图装置探究铁锈蚀条件:实验开始,同时将装置、和中的液体分别注入容器内,一段时间后,仅瓶中铁粉不变色。瓶中反应的化学方程式为 。

、瓶中铁粉更快锈蚀的是 填标号,下同。比较装置 中出现的现象,可推知水是铁锈蚀的条件之一。
欲证明铁生锈需同时与水和氧气同时接触,还需增加一个实验是 。
(4)、用铁新型纳米级铁粉能用作高效催化剂,反应前后其 和化学性质不变。
辩证看待铁锈蚀:锈蚀原理的有益应用是 写一点。
14. 某学习团队围绕“中和反应”开展以下活动:(1)、甲同学往稀硫酸中加入适量氢氧化铜,反应的化学方程式是 。(2)、乙同学进行改良酸性土壤的实验:可向土壤中加入适量 填化学式 , 来中和土壤中的酸。(3)、丙同学往装有氢氧化钠溶液与无色酚酞溶液的试管中,逐滴滴加稀盐酸至恰好完全反应。该实验的现象是 。
如图为该反应的微观过程,将反应后的微粒补充完整 。
往反应后溶液中加入溶液有白色沉淀产生,产生该现象的化学方程式是 。
 15. 国以农为本,农以种为先。跨学科实践活动“选好种”开展如下:(1)、盐水选种是古人智慧结晶:将鸡蛋放入盐水中,蛋壳只露出一个硬币大小的盐水适合选种。
15. 国以农为本,农以种为先。跨学科实践活动“选好种”开展如下:(1)、盐水选种是古人智慧结晶:将鸡蛋放入盐水中,蛋壳只露出一个硬币大小的盐水适合选种。时盐水浓度与密度对照如下表。用密度计测定此时盐水的密度为 , 则该盐水中氯化钠的质量分数为 。
浓度溶质的质量分数
溶液的密度
同一鸡蛋在三种盐水中的浮沉状态如图。下列说法正确的是 填标号。

A.三种盐水中溶质的质量分数相等
B.乙杯中鸡蛋的密度比盐水密度小
C.若丙中继续加盐溶解后,鸡蛋露出液面的体积会增大
(2)、实验室拟配制的氯化钠溶液。提供药品:氯化钠固体、氯化钠溶液密度约为、蒸馏水密度约为;
仪器:托盘天平、滴管、烧杯、玻璃棒、量筒规格有、和。
配制方法
所需药品及用量
所需仪器
方法一
氯化钠固体 , 水
托盘天平、滴管、烧杯、玻璃棒和
方法二
将 的氯化钠溶液稀释
烧杯、 、滴管、量筒和量筒
16. 利用注射器完成下列实验。 (1)、用装置电解水,该反应的化学方程式为 ;实验结束,将形管两侧气体抽出,若注射器Ⅰ收集到气体,则注射器Ⅱ收到 气体。(2)、实验室制备二氧化碳反应的化学方程式为 。
(1)、用装置电解水,该反应的化学方程式为 ;实验结束,将形管两侧气体抽出,若注射器Ⅰ收集到气体,则注射器Ⅱ收到 气体。(2)、实验室制备二氧化碳反应的化学方程式为 。检查装置气密性的方法:关闭止水夹,将注射器的活塞向上拉,松手后若 ,说明气密性良好。
若将装置与注射器内液体全部注入,装置 填标号可随时控制反应结束。停止反应的操作是 。
17. 某化学小组探究与碱溶液的反应。(1)、【实验Ⅰ】探究与三种碱溶液的反应如图
瓶和中均出现浑浊,中不浑浊。写出中反应的化学方程式: 。 (2)、三个软矿泉水瓶变瘪程度从左至右依次明显,据此推测,常温下三种碱的 填物理性质不同。(3)、【实验Ⅱ】利用实验室制取的 , 探究与溶液反应如图和图
(2)、三个软矿泉水瓶变瘪程度从左至右依次明显,据此推测,常温下三种碱的 填物理性质不同。(3)、【实验Ⅱ】利用实验室制取的 , 探究与溶液反应如图和图
设计图实验与图进行对照,目的是 。(4)、两天后观察到现象;图试管内液面上升得与图一样高,分析其原因是 。一周后发现:两试管中均始终无法充满液体,产生该现象的原因可能是 写一点。(5)、【实验Ⅲ】数字化探究 CO2 与 NaOH 溶液反应
在老师指导下,该小组同学将 CO2 持续通入一定量的 NaOH 溶液中,利用传感器测定反应过程中溶液的 pH 和温度变化,结果如图 4 与图 5 。
【资料在线】
① 向 NaOH 溶液中持续通入 CO2 ,先后发生两步化学反应。
第一步, CO2 与 NaOH 溶液反应生成 Na2CO3 和 H2O ;
第二步, CO2 与 Na2CO3 溶液继续反应生成 NaHCO3 。
② 本实验条件下, Na2CO3 溶液和 NaHCO3 溶液的 pH 分别约为 11.0 和 8.0 。
图中段发生的是第 填“一”或“二”步反应。图显示与溶液的反应属于 填“吸热”或“放热”反应。18. 某天然气含质量分数为的甲烷制氢的原理为。根据化学方程式计算:用该方法制得氢气,需消耗天然气的质量为多少?写出计算过程。