江苏省无锡市2023年中考化学真题
试卷更新日期:2023-10-20 类型:中考真卷
一、单选题
-
1. “天工开物”是指人利用自然规律开创物质财富。下列过程中的变化属于物理变化的是( )A、海水晒盐 B、粮食酿酒 C、烧石成灰 D、烧窑制砖2. 金属材料使用的历程体现着人类文明的演变。下列金属最先被大规模使用的是( )A、铝 B、锌 C、铁 D、铜3. 白鱼、白虾和银鱼被称为“太湖三白”。“太湖三白”富含的营养素为( )A、蛋白质 B、糖类 C、油脂 D、维生素4. 下列物质属于纯净物的是( )A、自来水 B、石灰水 C、矿泉水 D、蒸馏水5. 下列图标表示“禁止带火种”的是( )A、
 B、
B、 C、
C、 D、
D、 6. 配制50 g溶质的质量分数为6%的氯化钠溶液,不需要的仪器是( )
6. 配制50 g溶质的质量分数为6%的氯化钠溶液,不需要的仪器是( )
A、酒精灯 B、玻璃棒 C、烧杯 D、量筒7. 下列化肥不能配成绿植“水培溶液”的是( )A、氯化钾 B、氯化铵 C、硝酸钠 D、磷矿粉8. 市售饼干、海苔等食品包装中常用的干燥剂是( )A、生石灰 B、氯化钠 C、浓硫酸 D、氢氧化钠9. 下列化学用语所表达的意义正确的是( )A、—3个氧原子 B、—1个钠离子 C、Al—氯元素 D、2N—2个氮分子10. 铕是一种稀土元素,铕在元素周期表中的信息如图所示。下列叙述错误的是( ) A、铕是一种金属元素 B、铕原子中的质子数为63 C、铕的相对原子质量为152.0g D、稀土资源应合理利用和保护11. 在给定条件下,下列物质间的转化不能一步实现的是( )A、 B、溶液 C、 D、12. 下列趣味实验的目的无法达成的是( )A、用紫甘蓝自制酸碱指示剂 B、用灼烧法鉴别棉线和羊毛线 C、用铅笔芯做导电实验 D、用蔗糖水鉴别硬水和软水13. 下列概念之间存在图所示关系的是( )
A、铕是一种金属元素 B、铕原子中的质子数为63 C、铕的相对原子质量为152.0g D、稀土资源应合理利用和保护11. 在给定条件下,下列物质间的转化不能一步实现的是( )A、 B、溶液 C、 D、12. 下列趣味实验的目的无法达成的是( )A、用紫甘蓝自制酸碱指示剂 B、用灼烧法鉴别棉线和羊毛线 C、用铅笔芯做导电实验 D、用蔗糖水鉴别硬水和软水13. 下列概念之间存在图所示关系的是( )选项
A
B
C
D
概念
X
单质
氧化反应
碱溶液
中和反应
Y
化合物
化合反应
碱性溶液
分解反应
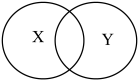 A、A B、B C、C D、D14. 艾草中富含的黄酮素()有极高的药用价值。下列叙述正确的是( )A、黄酮素属于有机高分子化合物 B、黄酮素中氧元素的质量分数最小 C、黄酮素的相对分子质量为222 D、黄酮素中含有1个氧分子15. 如图是“光催化固氮合成氨”反应前后分子种类变化的示意图。下列叙述正确的是( )
A、A B、B C、C D、D14. 艾草中富含的黄酮素()有极高的药用价值。下列叙述正确的是( )A、黄酮素属于有机高分子化合物 B、黄酮素中氧元素的质量分数最小 C、黄酮素的相对分子质量为222 D、黄酮素中含有1个氧分子15. 如图是“光催化固氮合成氨”反应前后分子种类变化的示意图。下列叙述正确的是( )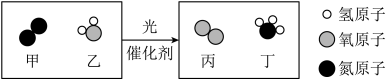 A、乙和丙都是氧化物 B、参加反应的甲和乙的分子个数比为 C、反应后原子数目增加 D、反应生成的丙和丁的质量比为16. 下列除杂方法能达到实验目的的是(括号中的物质为杂质)( )
A、乙和丙都是氧化物 B、参加反应的甲和乙的分子个数比为 C、反应后原子数目增加 D、反应生成的丙和丁的质量比为16. 下列除杂方法能达到实验目的的是(括号中的物质为杂质)( )选项
物质
除杂方法
A
在空气中点燃
B
加入过量稀盐酸
C
加足量水溶解、过滤
D
KCl溶液()
加入适量溶液,过滤
A、A B、B C、C D、D17. 用如图所示装置探究铜生锈的条件,一个月后发现铜丝未生锈。下列叙述错误的是( )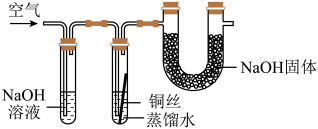 A、金属的腐蚀是金属从单质变成化合物的过程 B、在潮湿的空气中,铝比铁耐锈蚀 C、在有氧气和水的条件下,铜比铁易生锈 D、铜生锈可能与空气中的O2、H2O和CO2有关18. 某固体粉末可能由氢氧化钠、氢氧化钙、碳酸钠和碳酸钙中的一种或几种组成,进行如下实验:①取少量固体加入足量的水,搅拌,有白色沉淀;②过滤,向滤液中加入盐酸,有气泡产生。下列对固体粉末成分的判断中正确的是( )A、一定有碳酸钙 B、一定有氢氧化钠 C、一定有碳酸钠 D、一定有氢氧化钙19. “化学链燃烧”是指燃料不直接与空气接触,而是以载氧体在两个反应器之间的循环来实现燃料较低温度下燃烧的过程。某“化学链燃烧”的过程如下:
A、金属的腐蚀是金属从单质变成化合物的过程 B、在潮湿的空气中,铝比铁耐锈蚀 C、在有氧气和水的条件下,铜比铁易生锈 D、铜生锈可能与空气中的O2、H2O和CO2有关18. 某固体粉末可能由氢氧化钠、氢氧化钙、碳酸钠和碳酸钙中的一种或几种组成,进行如下实验:①取少量固体加入足量的水,搅拌,有白色沉淀;②过滤,向滤液中加入盐酸,有气泡产生。下列对固体粉末成分的判断中正确的是( )A、一定有碳酸钙 B、一定有氢氧化钠 C、一定有碳酸钠 D、一定有氢氧化钙19. “化学链燃烧”是指燃料不直接与空气接触,而是以载氧体在两个反应器之间的循环来实现燃料较低温度下燃烧的过程。某“化学链燃烧”的过程如下:
下列叙述错误的是( )
A、空气反应器中发生的反应为: B、X中氮气的含量比空气中高 C、与直接燃烧相比,“化学链燃烧”有利于二氧化碳的捕集 D、等质量的甲烷直接燃烧比“化学链燃烧”消耗氧气多20. 柠檬酸()能与碳酸氢钠反应生成二氧化碳。向4份等质量、等浓度的柠檬酸溶液中分别加入一定质量的碳酸氢钠,充分反应,4次实验数据记录见下表。实验序号
①
②
③
④
柠檬酸质量/g
0.96
0.96
0.96
0.96
加入的碳酸氢钠质量/g
0.42
二氧化碳体积/mL(标准状况下)
112
224
336
336
则实验④中参加反应的碳酸氢钠的质量为( )
A、0.84g B、1.26g C、1.68g D、2.10g二、填空题
-
21. 2008年北京奥运会“祥云”火炬(见图1)使用的燃料是丙烷(),2022年北京冬奥会“飞扬”火炬(见图2)使用的燃料是氢气。
 (1)、丙烷属于(选填“有机物”或“无机物”)。(2)、氢气属于(填序号)。
(1)、丙烷属于(选填“有机物”或“无机物”)。(2)、氢气属于(填序号)。a.化石能源 b.清洁能源 c.不可再生能源
(3)、氢气和丙烷都可压缩储存的原因是(填序号)。a.分子的质量很小 b.分子在不断运动 c.分子之间有间隔
(4)、“飞扬”火炬使用氢气替代丙烷作为燃料的原因是(写出一点即可)。22. 北京冬奥会利用“二氧化碳跨临界直冷制冰技术”将水快速制成冰。 (1)、液态二氧化碳汽化的过程(选填“放出”或“吸收”)热量。(2)、干冰和氟利昂都可作制冷剂。化学式为的氟利昂中含有种元素。(3)、在海底低温高压的条件下,甲烷水合物呈固态,被称为可燃冰(见图)。冰、干冰与可燃冰三种“冰”的化学性质不同,其原因是。23. 北京冬奥会使用了多种新型材料。(1)、铝合金属于(填序号)。
(1)、液态二氧化碳汽化的过程(选填“放出”或“吸收”)热量。(2)、干冰和氟利昂都可作制冷剂。化学式为的氟利昂中含有种元素。(3)、在海底低温高压的条件下,甲烷水合物呈固态,被称为可燃冰(见图)。冰、干冰与可燃冰三种“冰”的化学性质不同,其原因是。23. 北京冬奥会使用了多种新型材料。(1)、铝合金属于(填序号)。a.金属材料 b.合成材料 c.复合材料
(2)、“飞扬”火炬的外壳使用碳纤维树脂。碳纤维的硬度是钢的7倍,密度只有钢的1/4,能承受1200℃的高温;树脂选用高温阻燃型。你认为作为火炬外壳的材料应具备的性能是(写出一点即可),其理由是。三、科普阅读题
-
24. 阅读下列短文,回答相关问题。
科技助力人工碳循环
中国的经济发展离不开大量的能源,目前我国的能源结构中以煤(高碳)、石油(中碳)、天然气(低碳)为代表的化石燃料仍占主导地位,化石燃料的燃烧在释放热量的同时产生 , 是最主要的温室气体。低碳、零碳、负碳技术的开发是我国科学家正致力研发的项目。
也是巨大的碳资源。目前,的低能耗捕集、转化和利用正受到世界各国的广泛关注。根据与其他能源的耦合方式不同,的转化利用技术可分为以下三条途径。
途径1:耦合化石能源的转化利用技术。如与催化重整为与CO。
途径2:耦合零碳能源的转化利用技术。如图所示是我国科研团队利用催化剂实现低温、高效、长寿命催化加氢制甲醇()的工艺。
途径3:直接转化利用技术。如以太阳能或其他可再生能源发电为驱动力,在温和条件下将直接转化为化学原料或燃料。
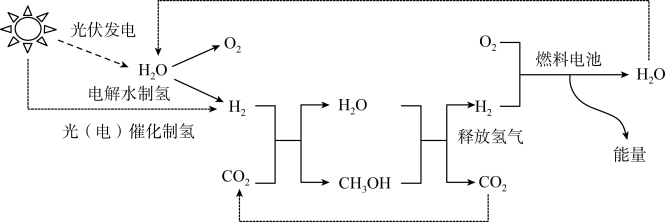
科学技术的研发和应用将促进自然界碳循环回归平衡。如何摆脱对含碳化石能源的依赖,转化利用丰富的资源,跨越低碳及创新新能源,拥抱新式零碳能源,期待同学们学好和利用化学开创未来。
(1)、写出自然界中吸收的一条途径:。(2)、氢氧燃料电池的能量转化形式是将化学能转化为。(3)、我国科学家将直接转化成葡萄糖的过程中,第一阶段的反应可表示为: , R的化学式是。(4)、写出和在催化剂和加热条件下转化为甲醇()的化学方程式:。(5)、下列叙述正确的是(填序号)。a.、与在一定条件下可相互转化
b.途径2解决了氢气低成本制取和有效储存的难题
c.能源的开发与利用向“减碳趋氢”的方向发展
四、流程题
-
25. 由菱铁矿(主要成分为 , 含少量等杂质)制备铁粉的一种流程如下:
 (1)、碳酸亚铁()中铁元素的化合价为。(2)、“酸浸”时,为使反应充分,可采取的一种措施是。“酸浸”后所得溶液中含有的溶质有:和。(3)、“沉铁”时,转化为沉淀,该反应的基本类型是。“焙烧”时,在高温条件下,与反应生成与的化学方程式为。(4)、“还原”时,在高温条件下,利用炭粉可将铁从氧化铁中还原出来;若向氧化铁与炭粉的混合物中添加适量的 , 更利于还原氧化铁,其原因是。
(1)、碳酸亚铁()中铁元素的化合价为。(2)、“酸浸”时,为使反应充分,可采取的一种措施是。“酸浸”后所得溶液中含有的溶质有:和。(3)、“沉铁”时,转化为沉淀,该反应的基本类型是。“焙烧”时,在高温条件下,与反应生成与的化学方程式为。(4)、“还原”时,在高温条件下,利用炭粉可将铁从氧化铁中还原出来;若向氧化铁与炭粉的混合物中添加适量的 , 更利于还原氧化铁,其原因是。五、实验题
-
26. 兴趣小组对燃烧的条件进行探究。(1)、利用如图所示装置进行实验,观察到的现象有:

Ⅰ.试管中白磷燃烧;
Ⅱ.水中白磷未燃烧;
Ⅲ.试管中红磷未燃烧;
Ⅳ.气球a先变大后变小。
①由现象Ⅰ、Ⅱ可推知的结论是。
②由现象Ⅰ、Ⅲ可推知的结论是。
③从现象Ⅳ分析:气球a先变大的原因是。
(2)、利用图1所示装置进行燃烧条件的进一步探究。实验测得集气瓶中氧气的体积分数随时间的变化曲线如图2所示。
①写出红磷燃烧的化学方程式:。
②红磷熄灭后,集气瓶内的氧气并未耗尽,氧气的含量约为10%。你对燃烧条件的新认识是。
六、综合应用题
-
27. 侯德榜先生为制取纯碱作出了杰出贡献。(1)、实验室模拟制取碳酸氢钠。
“侯氏制碱法”生产纯碱的过程中,碳酸氢钠的生成是至关重要的一环,其原理是: , 。兴趣小组在常温(20℃)下设计并完成了如图所示实验。
[已知20℃时NaCl、、、的溶解度为36.0g、21.0g、9.6g、37.2g。]

①实验1、2所得溶液处于饱和状态的是(填实验序号)。
②实验3的锥形瓶中出现白色浑浊,经检验为。写出用稀盐酸检验的化学方程式:。
(2)、侯氏制碱法的生产流程如下:
①实际生产中沉淀池内的温度不能太高,原因是。
②如图是四种物质的溶解度曲线。母液中含有较高浓度的和少量NaCl,利用降温结晶的方法可提纯 , 理由是。

③上述流程中可循环利用的物质有:NaCl和。
(3)、测定纯碱样品中碳酸钠的质量分数。纯碱产品中常混有少量氯化钠,兴趣小组设计以下两种方案测定某纯碱样品中碳酸钠的质量分数:

根据方案1,实验测得的质量为0.88g。根据方案2,实验测得的质量为3.94g。请任选其中一种方案与相关数据,计算该纯碱样品中碳酸钠的质量分数 (写出计算过程,结果精确到0.1%)。
28. 2023年5月30日,神舟十六号载人飞船发射成功,航天员将在中国空间站完成各项任务,因此,保障航天员的氧气需求至关重要。那么,空间站的氧气从哪里来?(1)、Ⅰ.从地球带上去实验室用高锰酸钾等原料制氧,写出高锰酸钾分解的化学方程式:;航天工业以空气为原料制氧,工业上选择空气的主要原因是。
(2)、工业上采用分离液态空气法获得氧气,其过程可用如图所示实验模拟。
①浸入液氮3min后,试管内产生约占其容积1/3的液态空气。取出试管,液态空气沸腾,伸入燃着的木条,木条熄灭;1min后伸入带火星的木条,观察到木条复燃。导致木条熄灭的原因是。
②上述实验利用氮气与氧气的沸点不同实现分离,由实验现象可知,两种气体中沸点比较高的气体是。
(3)、利用分子筛可将氧分子从空气中“筛”出去,从而获得高浓度的氧气。其原理示意图如下:
由此可知两种分子的大小:(填“>”或“<”)。
(4)、Ⅱ.在天宫制出来早期空间站利用过氧化钠()、超氧化钾()等物质制氧,其原理表示如下:空间站内二氧化碳的主要来源是。
(5)、目前空间站已实现电解水制氧,写出反应的化学方程式:。(6)、空间站是一个相对封闭的场所,解决“气体从哪里来”的问题必然伴生着“气体往哪里去”的问题。为此,科学家设计了生物再生生命保障系统,实现了“水-氧-碳”的循环转化。下列叙述正确的是(填序号)。a.“水-氧-碳”的循环转化,减少了氧气的携带量,减轻了火箭和飞船的载重
b.电解水在产生氧气的同时产生氢气,系统需要对氢气进行转化
c.人体代谢产物中的水既有气态又有液态,设计系统时应考虑水的冷凝与净化
-
-
-