广东省东莞市2023年化学中考一模试题
试卷更新日期:2023-10-16 类型:中考模拟
一、单选题
-
1. 在大型活动开幕式上会有精彩的表演,下列发生化学变化的是( )A、音乐喷泉 B、气球升空 C、焰火表演 D、霓虹灯走秀2. 回收废弃矿泉水瓶的垃圾桶上应贴的标记是( )A、
 B、
B、 C、
C、 D、
D、 3. 下列食品中富含蛋白质的是( )A、鱼肉 B、蔬菜 C、稻米 D、芝麻油4. 持续改善生态环境,推动绿色低碳发展是一项重要国策。下列做法不利于改善生态环境的是( )A、提倡生活垃圾分类回收并利用 B、加快轻轨电车建设,减少机动车尾气排放 C、改造或淘汰高能耗、高污染企业 D、用生活污水直接灌溉农田5. 下列选项中物质的化学式、俗名、类别完全对应的是( )A、NaOH 烧碱 碱 B、CaO 熟石灰 氧化物 C、Ag 水银 单质 D、Na2CO3 纯碱 碱6. 把凹陷的乒乓球放在热水中一段时间,会恢复原来的球状,从分子的角度解释原因是( )A、分子的体积变大 B、分子间的间隔变大 C、分子分成了原子 D、分子在不断运动7. 下列物品所使用的材料中,不属于有机合成材料的是( )A、尼龙绳子 B、汽车轮胎 C、铁钉 D、塑料盆8. “生活离不开化学”,下列叙述合理的是( )A、天然气泄漏时,立即打开排气扇电源开关 B、用甲醛溶液浸泡鱿鱼,以保质保鲜 C、食用加碘盐,可预防大脖子病 D、煤、石油都是可再生的能源9. 我国自主研发出超流氦大型低温制冷装备,打破了发达国家的技术垄断。液氦是制造超低温的“神器”。根据图中信息分析,下列关于氦的说法中正确的是( )
3. 下列食品中富含蛋白质的是( )A、鱼肉 B、蔬菜 C、稻米 D、芝麻油4. 持续改善生态环境,推动绿色低碳发展是一项重要国策。下列做法不利于改善生态环境的是( )A、提倡生活垃圾分类回收并利用 B、加快轻轨电车建设,减少机动车尾气排放 C、改造或淘汰高能耗、高污染企业 D、用生活污水直接灌溉农田5. 下列选项中物质的化学式、俗名、类别完全对应的是( )A、NaOH 烧碱 碱 B、CaO 熟石灰 氧化物 C、Ag 水银 单质 D、Na2CO3 纯碱 碱6. 把凹陷的乒乓球放在热水中一段时间,会恢复原来的球状,从分子的角度解释原因是( )A、分子的体积变大 B、分子间的间隔变大 C、分子分成了原子 D、分子在不断运动7. 下列物品所使用的材料中,不属于有机合成材料的是( )A、尼龙绳子 B、汽车轮胎 C、铁钉 D、塑料盆8. “生活离不开化学”,下列叙述合理的是( )A、天然气泄漏时,立即打开排气扇电源开关 B、用甲醛溶液浸泡鱿鱼,以保质保鲜 C、食用加碘盐,可预防大脖子病 D、煤、石油都是可再生的能源9. 我国自主研发出超流氦大型低温制冷装备,打破了发达国家的技术垄断。液氦是制造超低温的“神器”。根据图中信息分析,下列关于氦的说法中正确的是( ) A、氦原子核外电子数为4 B、氦元素形成的单质的化学式为He2 C、氦原子在化学反应中易失去电子,形成阳离子 D、氦的相对原子质量是4.00310. 目前,“新冠肺炎”与人类共生。加强个人卫生,注重防护是有效减少感染的有效途径。次氯酸钠(NaClO)和二氧化氯(ClO2)是两种常用的消毒剂。下列有关说法中正确的是( )A、次氯酸钠属于氧化物 B、二氧化氯由1个氯原子和2个氧原子构成 C、次氯酸钠中钠元素、氯元素和氧元素的质量比为1:1:1 D、次氯酸钠中氯元素的质量分数比二氧化氯中氯元素的质量分数小11. 除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是( )
A、氦原子核外电子数为4 B、氦元素形成的单质的化学式为He2 C、氦原子在化学反应中易失去电子,形成阳离子 D、氦的相对原子质量是4.00310. 目前,“新冠肺炎”与人类共生。加强个人卫生,注重防护是有效减少感染的有效途径。次氯酸钠(NaClO)和二氧化氯(ClO2)是两种常用的消毒剂。下列有关说法中正确的是( )A、次氯酸钠属于氧化物 B、二氧化氯由1个氯原子和2个氧原子构成 C、次氯酸钠中钠元素、氯元素和氧元素的质量比为1:1:1 D、次氯酸钠中氯元素的质量分数比二氧化氯中氯元素的质量分数小11. 除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是( )选项
物质(括号内为杂质)
选用试剂
操作方法
A
FeCl2溶液(CuCl2溶液)
足量铁粉
过滤
B
CaO(CaCO3)
足量蒸馏水
过滤、蒸发
C
NaCl溶液(Mg(OH)2溶液)
过量稀盐酸
过滤
D
CO2(CO)
过量O2
点燃
A、A B、B C、C D、D12. 甲、乙、丙三种固体物质的溶解度曲线如图所示。下列有关说法正确的是( ) A、t1℃时甲、乙、丙三种物质的溶解度大小关系是甲>乙>丙 B、乙中含有少量甲时,可用冷却热饱和溶液的方法提纯乙 C、t2℃时,将55g乙加入100g水中充分溶解,所得溶液的质量为150g D、将t3℃时甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液中溶质质量分数由大到小的顺序是:乙>甲=丙13. 某小组利用如图装置进行创新实验,向右缓慢推动注射器活塞后发现白碳燃烧。下列有关该实验的说法错误的是( )
A、t1℃时甲、乙、丙三种物质的溶解度大小关系是甲>乙>丙 B、乙中含有少量甲时,可用冷却热饱和溶液的方法提纯乙 C、t2℃时,将55g乙加入100g水中充分溶解,所得溶液的质量为150g D、将t3℃时甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液中溶质质量分数由大到小的顺序是:乙>甲=丙13. 某小组利用如图装置进行创新实验,向右缓慢推动注射器活塞后发现白碳燃烧。下列有关该实验的说法错误的是( ) A、证明燃烧需要温度达到着火点 B、注射器中氧气可以换成空气 C、细沙和纸棒可以阻止白磷随水流动 D、气球可以缓冲气压减少污染14. 如图表示稀盐酸和氢氧化钠溶液发生反应时,烧杯中溶液的pH随滴入液体体积的变化曲线及相关的实验操作,下列说法正确的是( )
A、证明燃烧需要温度达到着火点 B、注射器中氧气可以换成空气 C、细沙和纸棒可以阻止白磷随水流动 D、气球可以缓冲气压减少污染14. 如图表示稀盐酸和氢氧化钠溶液发生反应时,烧杯中溶液的pH随滴入液体体积的变化曲线及相关的实验操作,下列说法正确的是( ) A、该实验是将氢氧化钠溶液滴入盛有稀盐酸的烧杯中 B、当滴入液体体积为5mL时,烧杯内溶液呈酸性 C、当滴入液体体积为7mL时,盐酸和氢氧化钠恰好完全反应 D、当滴入液体体积为9mL时,烧杯内溶液中的微粒有2种15. 下列图像关系合理的是( )
A、该实验是将氢氧化钠溶液滴入盛有稀盐酸的烧杯中 B、当滴入液体体积为5mL时,烧杯内溶液呈酸性 C、当滴入液体体积为7mL时,盐酸和氢氧化钠恰好完全反应 D、当滴入液体体积为9mL时,烧杯内溶液中的微粒有2种15. 下列图像关系合理的是( ) A、图①:向一定质量的石灰石中加入过量的稀盐酸 B、图②:常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应 C、图③:在饱和的KNO3溶液中加入KNO3晶体 D、图④:电解水生成氢气和氧气的质量
A、图①:向一定质量的石灰石中加入过量的稀盐酸 B、图②:常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应 C、图③:在饱和的KNO3溶液中加入KNO3晶体 D、图④:电解水生成氢气和氧气的质量二、填空题
-
16. 无人机的用途越来越广泛,可以用于航拍、喷洒农药、巡查、空投等。无人机的最基本组件有框架、发动机和螺旋桨、电池、传感器几个部分。
 (1)、高性能无人机框架最适合选用密度小、强度高、耐热、硬度较大、化学稳定性好的____(填字母)。A、生铁 B、纯铝 C、黄铜 D、铝合金(2)、无人机的动力来源是锂离子电池,电池在工作过程中实现的能量转化是能转化为电能。锂系电池分为锂电池和锂离子电池,锂电池在工作时是与二氧化锰反应生成亚锰酸锂(LiMnO2),该反应的化学方程式为。(3)、锂原子结构示意图如图所示,在反应中该原子容易(填“得到”或“失去”)1个电子形成离子,写出锂离子的符号。
(1)、高性能无人机框架最适合选用密度小、强度高、耐热、硬度较大、化学稳定性好的____(填字母)。A、生铁 B、纯铝 C、黄铜 D、铝合金(2)、无人机的动力来源是锂离子电池,电池在工作过程中实现的能量转化是能转化为电能。锂系电池分为锂电池和锂离子电池,锂电池在工作时是与二氧化锰反应生成亚锰酸锂(LiMnO2),该反应的化学方程式为。(3)、锂原子结构示意图如图所示,在反应中该原子容易(填“得到”或“失去”)1个电子形成离子,写出锂离子的符号。
三、科普阅读题
-
17. 阅读科普短文,回答问题。
“碳中和”是指通过各种捕捉技术使排放到大气中的温室气体净增量为零。目前,CO2捕捉技术有①物理吸收法—用活性炭、沸石等或用甲醇作溶剂对CO2进行吸收;②化学吸收法——主要利用氨水吸收剂(主要成分为NH3•H2O,受热易分解)、钙基吸收剂(主要成分为CaO)等。用氨水吸收剂时,控制温度在30℃左右采用喷氨技术吸收CO2 , 生成碳酸氢铵。
(1)、活性炭、沸石等可作吸附剂,则其可能具备的结构特点是。(2)、用甲醇作溶剂吸收CO2时为提高吸收率应采用的温度和压强条件是(选序号)。a.高温、高压 b.高温、低压 c.低温、高压 d.低温、低压
(3)、采用喷氨技术吸收CO2时,发生的反应方程式为。(4)、碳基吸收剂中的生石灰在生活中可做食品干燥剂,其干燥原理用化学方程式表示为;钙基吸收剂长期露置在空气中,最终得到的固体成分主要为(填化学式)。(5)、二氧化碳的用处很多,其中干冰能用于人工降雨,是因为干冰升华(填“吸热”或“放热”),使水蒸气凝结成小水滴。(6)、下列措施利于实现“碳中和”目标的为____(填序号)。A、电脑长时间待机 B、研发新能源汽车 C、鼓励乘坐公交车出行 D、多植树造林四、实验题
-
18. 下图为实验室制取气体时常用的仪器,请结合你所学的化学知识回答下列问题。
 (1)、写出实验室用KClO3与MnO2的混合固体制取O2的化学方程式:;若选A为发生装置,还缺少(填仪器名称)。(2)、实验室制取CO2的药品是和稀盐酸,不能使用浓盐酸的原因是。为了可以随时控制反应的发生和停止,应选择为发生装置(选序号,下同),为收集装置;为获得干燥的二氧化碳气体,可将气体先通入装置F再收集,则装置F中盛放的是。(3)、实验室常用B装置制取乙炔(C2H2)气体,该反应很剧烈,可通过调节B装置中的(填仪器名称)的活塞控制反应速率。通常情况下乙炔是一种无色、无味、密度比空气小的气体,若用G装置采用“排空气法”收集乙炔气体,请在图中将导管补画完整。
(1)、写出实验室用KClO3与MnO2的混合固体制取O2的化学方程式:;若选A为发生装置,还缺少(填仪器名称)。(2)、实验室制取CO2的药品是和稀盐酸,不能使用浓盐酸的原因是。为了可以随时控制反应的发生和停止,应选择为发生装置(选序号,下同),为收集装置;为获得干燥的二氧化碳气体,可将气体先通入装置F再收集,则装置F中盛放的是。(3)、实验室常用B装置制取乙炔(C2H2)气体,该反应很剧烈,可通过调节B装置中的(填仪器名称)的活塞控制反应速率。通常情况下乙炔是一种无色、无味、密度比空气小的气体,若用G装置采用“排空气法”收集乙炔气体,请在图中将导管补画完整。五、科学探究题
-
19. 某兴趣小组同学探究了酸、碱的部分性质。(1)、【实验一】探究酸碱中和反应。
图1将注射器内的液体逐滴注入烧瓶内,烧瓶中反应的化学方程式为。实验测得烧瓶中溶液的pH随时间的变化关系如图2所示,c点所示溶液加热蒸干所得固体是。(填化学式) (2)、该反应是放热反应,对应图2中点温度最高。(3)、图1能说明盐酸和氢氧化钠恰好完全反应的现象是:此时溶液的颜色恰好变化为 , pH传感器测得溶液的pH7(填“>”、“<”或“=”)。(4)、【实验二】探究NaOH和CO2的反应。
(2)、该反应是放热反应,对应图2中点温度最高。(3)、图1能说明盐酸和氢氧化钠恰好完全反应的现象是:此时溶液的颜色恰好变化为 , pH传感器测得溶液的pH7(填“>”、“<”或“=”)。(4)、【实验二】探究NaOH和CO2的反应。从压强变化的角度探究。
①利用如图装置进行实验,先挤压胶头滴管,再打开止水夹,观察到烧瓶内形成红色“喷泉”,原因是烧瓶内压强(填“大于”或“小于”)外界大气压,烧瓶内发生的主要反应化学方程式。

②利用如图装置进行实验,分别将等体积的NaOH溶液和水同时注入盛有等体积CO2的玻璃容器中,证明CO2与NaOH溶液发生反应的实验现象是。

六、流程题
-
20. 某化学兴趣小组同学在实验室中模拟从电镀厂排放的污水中回收固体硫酸锌、金属镍和铜,操作流程如图所示:【已知金属活动性:Cu<(H)<Ni<Zn】
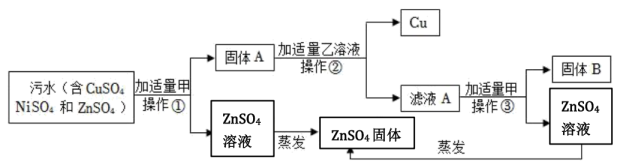 (1)、上述①②③的操作名称是 , 所使用的玻璃仪器有玻璃棒、烧杯、 , 其中玻璃棒的作用是。(2)、操作①中,加适量甲单质的化学式是 , 加入适量甲的目的是 , 请写出该过程中发生反应的化学方程式(任选一个即可)。(3)、写出操作②中发生反应的化学方程式。(4)、若忽略实验过程中的物质损失,最终回收的硫酸锌固体的质量(填“大于”“等于”或“小于”)原污水中该物质的质量。
(1)、上述①②③的操作名称是 , 所使用的玻璃仪器有玻璃棒、烧杯、 , 其中玻璃棒的作用是。(2)、操作①中,加适量甲单质的化学式是 , 加入适量甲的目的是 , 请写出该过程中发生反应的化学方程式(任选一个即可)。(3)、写出操作②中发生反应的化学方程式。(4)、若忽略实验过程中的物质损失,最终回收的硫酸锌固体的质量(填“大于”“等于”或“小于”)原污水中该物质的质量。七、计算题
-
21. 已知水垢的主要成分为碳酸钙,某同学取12g的水垢放入烧杯中,逐滴加入120g的稀盐酸进行反应(水垢中的其他杂质不与盐酸反应,也不溶于稀盐酸),反应关系如下图所示。请回答下列问题:
 (1)、碳酸钙中钙元素和氧元素的质量比为(最简比)。(2)、产生的二氧化碳的质量为g。(3)、计算水垢中碳酸钙的质量分数(精确到0.1%,写出计算过程)。(4)、所用稀盐酸的溶质质量分数为。
(1)、碳酸钙中钙元素和氧元素的质量比为(最简比)。(2)、产生的二氧化碳的质量为g。(3)、计算水垢中碳酸钙的质量分数(精确到0.1%,写出计算过程)。(4)、所用稀盐酸的溶质质量分数为。
-
-
-
-
-