广东省东莞市2023年化学中考三模试题
试卷更新日期:2023-10-16 类型:中考模拟
一、单选题
-
1. 世界是物质的,物质是变化的。下列变化不属于化学变化的是( )A、火药使用 B、酒精洗掉沾在试管壁上的碘 C、植物光合作用 D、鸡蛋变臭2. 我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。下列措施对实现”碳中和”不具有直接贡献的是( )A、推行生活垃圾分类 B、植树造林增加绿色植被 C、采取节能低碳生活方式 D、创新CO2转化为碳燃料的技术3. 下列物质可看作纯净物的是( )A、食盐水 B、稀有气体 C、液氧 D、生铁4. 2022北京冬奥会吉祥物“冰墩墩”(如图),一款冰墩墩制作的外部材料为纯羊毛绒,内充无毒的合成纤维。下列说法正确的是( )
 A、制作冰墩墩的合成纤维是引起“白色污染”的主要物质之一 B、纯羊毛和合成纤维可用燃烧法区别 C、制作冰墩墩的外部材料属于有机合成材料 D、合成纤维的吸水性和透气性比纯羊毛好5. 下列物质中氯元素的化合价最高的是( )A、HCl B、Cl2 C、NaClO3 D、NaClO46. 为检测白醋的酸碱性,将白醋滴到紫色石蕊试纸上,试纸显示的颜色为( )A、红色 B、蓝色 C、紫色 D、黄色7. 2022年12月4日,神舟十四号安全返回地面,并带回了“世界上第一粒在太空中培育出的水稻种子”。种植水稻,要施加复合肥。下列属于复合肥的是( )A、K2CO3 B、NH4HCO3 C、Ca(H2PO4)2 D、KNO38. “劳动创造幸福,实干成就伟业”,下列劳动所涉及的化学知识正确的是( )
A、制作冰墩墩的合成纤维是引起“白色污染”的主要物质之一 B、纯羊毛和合成纤维可用燃烧法区别 C、制作冰墩墩的外部材料属于有机合成材料 D、合成纤维的吸水性和透气性比纯羊毛好5. 下列物质中氯元素的化合价最高的是( )A、HCl B、Cl2 C、NaClO3 D、NaClO46. 为检测白醋的酸碱性,将白醋滴到紫色石蕊试纸上,试纸显示的颜色为( )A、红色 B、蓝色 C、紫色 D、黄色7. 2022年12月4日,神舟十四号安全返回地面,并带回了“世界上第一粒在太空中培育出的水稻种子”。种植水稻,要施加复合肥。下列属于复合肥的是( )A、K2CO3 B、NH4HCO3 C、Ca(H2PO4)2 D、KNO38. “劳动创造幸福,实干成就伟业”,下列劳动所涉及的化学知识正确的是( )选项
劳动项目
化学知识
A
煮水时,若水的硬度大,易结垢
硬水中含有较多可溶性钙、镁化合物
B
用明矾处理较浑浊的天然水
明矾主要起杀菌消毒作用
C
在盐田中晾晒海水,得到粗盐
粗盐除去泥沙即可得到纯净的氯化钠
D
用洗涤剂清洗污渍
洗涤剂可以溶解油污
A、A B、B C、C D、D9. 微信表情包“苯宝宝装纯”,是根据化合物“苯酚”的结构设计的,其化学式为C6H6O,下列有关“苯酚”说法正确的是( )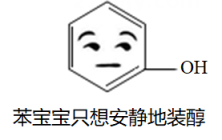 A、由13个原子构成 B、含有水分子 C、氢元素的质量分数最小 D、碳、氢两种元素的质量比为1:110. 甲和乙在一定条件下反应生成丙和丁,微观示意图如下。有关说法正确的是( )
A、由13个原子构成 B、含有水分子 C、氢元素的质量分数最小 D、碳、氢两种元素的质量比为1:110. 甲和乙在一定条件下反应生成丙和丁,微观示意图如下。有关说法正确的是( )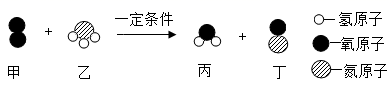 A、反应前后分子的种类、数目均不变 B、反应前后各元素的化合价均不变 C、该反应属于置换反应 D、参加反应的甲和乙分子个数比为5:411. 小陈用稀盐酸和NaOH溶液进行中和反应的有关探究如图甲所示,用pH传感器测得烧杯内溶液pH变化图像如图乙所示,同时用温度传感器测得烧杯内溶液温度变化图像如图丙所示,实验过程中保温良好,忽略热量散失。下列说法错误的是( )
A、反应前后分子的种类、数目均不变 B、反应前后各元素的化合价均不变 C、该反应属于置换反应 D、参加反应的甲和乙分子个数比为5:411. 小陈用稀盐酸和NaOH溶液进行中和反应的有关探究如图甲所示,用pH传感器测得烧杯内溶液pH变化图像如图乙所示,同时用温度传感器测得烧杯内溶液温度变化图像如图丙所示,实验过程中保温良好,忽略热量散失。下列说法错误的是( )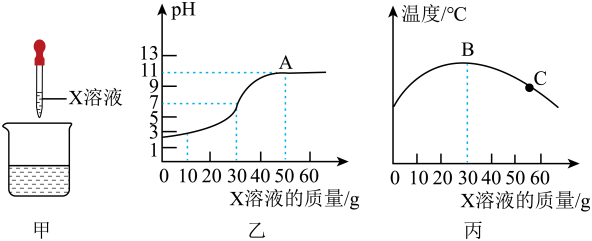 A、X溶液为NaOH溶液 B、图丙说明中和反应是放热反应 C、B点对应溶液中的溶质是NaCl D、图乙中A点与图丙中的C点对应,都属于恰好完全反应12. 中和反应在生产、生活中应用广泛。下列应用的主要原理不涉及中和反应的是( )A、用硫酸处理印染厂含碱的废水 B、氢氧化铝用于治疗胃酸过多 C、碳酸氢钠溶液用于处理皮肤上沾有的酸 D、硼酸用于处理皮肤上沾有的碱13. 除去下列物质中的少量杂质,所用试剂及方法正确的是( )
A、X溶液为NaOH溶液 B、图丙说明中和反应是放热反应 C、B点对应溶液中的溶质是NaCl D、图乙中A点与图丙中的C点对应,都属于恰好完全反应12. 中和反应在生产、生活中应用广泛。下列应用的主要原理不涉及中和反应的是( )A、用硫酸处理印染厂含碱的废水 B、氢氧化铝用于治疗胃酸过多 C、碳酸氢钠溶液用于处理皮肤上沾有的酸 D、硼酸用于处理皮肤上沾有的碱13. 除去下列物质中的少量杂质,所用试剂及方法正确的是( )选项
混合物(括号内为杂质)
试剂及方法
A
KCl溶液(K2CO3)
滴加过量稀硫酸
B
HCl溶液(H2SO4)
滴加适量氯化钡溶液,过滤
C
FeCl2溶液(CuCl2)
加过量锌粉,过滤
D
N2(O2)
通过灼热的氧化铜
A、A B、B C、C D、D14. 王亚平用过饱和醋酸钠溶液演示“冰雪”实验。如图是醋酸钠的溶解度曲线,下列说法正确的是( )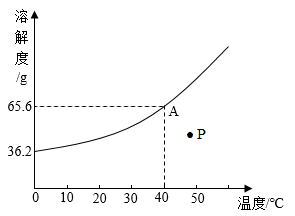 A、降温能使P点醋酸钠溶液变为饱和溶液 B、40℃时,50g水中加入40g醋酸钠,可得90g溶液 C、40℃时,饱和醋酸钠溶液的溶质质量分数是65.6% D、将A点的饱和溶液升温至50℃,溶质质量分数增大15. 下列图像能正确反映对应变化过程的是( )A、
A、降温能使P点醋酸钠溶液变为饱和溶液 B、40℃时,50g水中加入40g醋酸钠,可得90g溶液 C、40℃时,饱和醋酸钠溶液的溶质质量分数是65.6% D、将A点的饱和溶液升温至50℃,溶质质量分数增大15. 下列图像能正确反映对应变化过程的是( )A、 加热高锰酸钾制取氧气
B、
加热高锰酸钾制取氧气
B、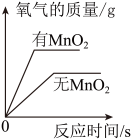 分解等质量等浓度的过氧化氢溶液
C、
分解等质量等浓度的过氧化氢溶液
C、 将等质量的镁片、铁片加入足量稀硫酸中
D、
将等质量的镁片、铁片加入足量稀硫酸中
D、 用燃烧红磷的方法测定空气中氧气含量
用燃烧红磷的方法测定空气中氧气含量
二、填空题
-
16. 古代典籍《梦溪笔谈》中记载了用“苦泉水”制取铜的方法:“挹其水熬之,则成胆矾(化学式为CuSO4·5H2O)。烹胆矾则成铜;熬胆矾铁釜,久之亦化为铜”。请回答下列问题:(1)、CuSO4属于(填“纯净物”或“混合物”)。(2)、CuSO4·5H2O由种元素组成,其中氢、氧原子个数比为 , 质量分数最大的元素是。(填元素名称)(3)、“熬胆矾铁釜,久之亦化为铜”涉及反应的化学方程式是。(4)、“烹胆矾则成铜”的化学原理是CuSO4·5H2O在加热的条件下逐渐失水,最后分解并转化为氧化亚铜(Cu2O),标出氧化亚铜中铜元素的化合价:。17. 近期,广东疾控中心发布提醒,注意诺如病毒。据悉,该病毒十分狡猾,下手不挑人,环境抵抗力极强,认识病毒的传播与防治十分重要。(1)、出门或在社交场所尽量戴口罩,口罩防护相当于化学实验操作中的 , 可以有效地防止病毒在人与人之间传播。(2)、发现体温异常可以用水银温度计测量体温,从微观角度解释水银可以用来测量体温的原因:。(3)、对场所进行消毒可以使用的ClO2消毒液,该物质名称是 , 也可以用其他消毒剂,下列不属于含氯消毒剂的是(填标号)。
A.84消毒剂(主要成分是NaClO) B.过氧化氢 C.氯气 D.过氧乙酸(C2H4O3)
(4)、利用75%的酒精进行消毒时一定要注意安全,防止酒精燃烧造成危险,写出酒精燃烧的化学方程式:。(5)、“石灰淹苗足”指用熟石灰来改良酸性土壤。①酸雨是导致土壤呈酸性的原因之一,酸雨的pH<。
②下列空气污染物会导致酸雨的是(多选,填字母序号)。
a.CO2 b.SO2 c.NO2 d.CO
三、实验题
-
18. 具备基本化学实验技能是学习化学的基础和保证。(1)、Ⅰ.根据下列装置图,回答有关问题:
写出装置图中标号仪器的名称:a。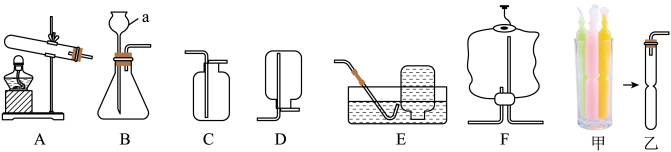 (2)、用高锰酸钾制取O2 , 装置A还需做的一点改动是 , 发生反应的化学方程式为。若用如图F所示塑料袋排空气法收集O2 , 则O2导入端为(填“长”或“短”)管。(3)、如图中,甲是某品牌可吸棒棒冰。某兴趣小组利用其塑料包装设计了如乙所示装置来制取CO2 , 该装置的优点主要为 , 实验中大理石应放置在软管的(选填“上部”或“下部”)。(4)、Ⅱ.实验室欲配制50g溶质质量分数为20%的氯化钠溶液。
(2)、用高锰酸钾制取O2 , 装置A还需做的一点改动是 , 发生反应的化学方程式为。若用如图F所示塑料袋排空气法收集O2 , 则O2导入端为(填“长”或“短”)管。(3)、如图中,甲是某品牌可吸棒棒冰。某兴趣小组利用其塑料包装设计了如乙所示装置来制取CO2 , 该装置的优点主要为 , 实验中大理石应放置在软管的(选填“上部”或“下部”)。(4)、Ⅱ.实验室欲配制50g溶质质量分数为20%的氯化钠溶液。实验步骤:①计算,需要氯化钠的质量为g,②称量,③量取,④溶解,⑤转移,⑥贴标签备用。
(5)、应用:农业上常用氯化钠溶液来选种,若要用16%的氯化钠溶液来选种,则应在上述配好的氯化钠溶液中加入水的质量为g。(6)、若将上述配置好的溶质质量分数为20%的氯化钠溶液倒出一半,则剩余溶液的溶质质量分数为。四、科学探究题
-
19. 咸宁市某校2022年实验操作模拟考试的一个考题是:用碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水。(1)、【进行实验】
实验步骤
实验现象
实验结论
分别用a,b,c三支试管取样,各加入一定量碳酸钠溶液
a中有气泡产生
b中无明显现象
c中
a中物质是稀盐酸
b中物质是食盐水
c中物质是澄清石灰水
写出a试管中发生反应的化学方程式:。
把c试管反应后的物质进行过滤,得到滤液。
【提出问题】滤液中溶质的成分是什么?
猜想一:Na2CO3和NaOH;
猜想二:NaOH;
猜想三:。
【实验过程】为证明猜想一是否正确,进行了如下实验
实验步骤
实验现象
实验结论
取一定量滤液于试管中,加入一种盐溶液(写化学式)
有白色沉淀
猜想一正确
写出上述有白色沉淀生成的化学方程式:。
同学们还对a试管反应后废液的酸碱性感兴趣,决定用pH试纸测定其pH值。
用pH试纸测定a试管反应后废液酸碱性的过程
测定结果
在白瓷板上放一小片pH试纸,用玻璃棒蘸取。(写操作过程)
pH<7(废液显酸性)
(2)、【反思与交流】a试管中的废液显酸性,从环保、经济、操作简便等方面考虑,应向废液加入一种碱(写俗名)后再排放。20. 在初中化学“金属的性质”中有如下实验:将无锈铁钉浸入CuSO4溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。(1)、【提出问题】Al和CuSO4溶液也能发生化学反应吗?
预测Al和CuSO4溶液反应,理由是。(2)、【进行实验】将一端缠绕的铝丝浸入CuSO4溶液(如下图),观察现象。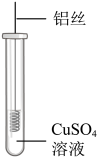
铝丝表面未出现红色物质,原因是。
(3)、【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。填写实验报告单:
序号
实验现象
结论与解释
①
铝丝表面有少量气泡;铝丝周围出现蓝绿色物质
CuSO4溶液呈弱酸性,与Al反应产生的气体是;蓝绿色物质成分待探究
②
24h后,铝丝仍光亮;48h后,铝丝表面出现少量红色物质
红色物质是 , 说明Al能和CuSO4溶液反应,但反应较慢
③
铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色;两层溶液界面清晰
反应生成的Al2(SO4)3为无色;Al2(SO4)3溶液的密度(填“>”或“<”)CuSO4溶液的密度
(4)、【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为。
(5)、欲加快Al和CuSO4溶液的反应,可加入的物质是(填一种即可)。(6)、【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。铝制品有较好的抗腐蚀性,其原因是。(用化学方程式表示)
五、计算题
-
21. 某项目学习小组对实验室制取二氧化碳后过滤所得的废液进行探究。取100g该废液,逐滴加入碳酸钠溶液,充分反应后测得产生沉淀的质量如图所示,请回答下列问题。
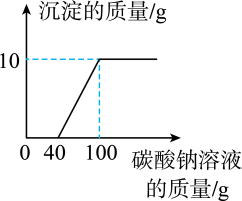 (1)、分析题图可知,废液中的溶质为(填化学式)。(2)、充分反应生成碳酸钙的质量为g。(3)、计算该废液中氯化钙的质量分数(写出计算过程)。(4)、用氧化钙、氢氧化钙和碳酸钙都可将该废液中的盐酸除去,获得氯化钙溶液,处理等质量的该废液,需这三种物质的质量由小到大的顺序为(用化学式填空)。
(1)、分析题图可知,废液中的溶质为(填化学式)。(2)、充分反应生成碳酸钙的质量为g。(3)、计算该废液中氯化钙的质量分数(写出计算过程)。(4)、用氧化钙、氢氧化钙和碳酸钙都可将该废液中的盐酸除去,获得氯化钙溶液,处理等质量的该废液,需这三种物质的质量由小到大的顺序为(用化学式填空)。
-