广东省广州市增城区2023年中考化学二模试卷
试卷更新日期:2023-10-13 类型:中考模拟
一、选择题
-
1. 用紫甘蓝自制酸碱指示剂,并检验溶液的酸碱性。有关步骤涉及化学变化的是( )A、在研钵中捣烂紫甘蓝 B、加入酒精浸泡紫甘蓝 C、用纱布过滤浸泡出的汁液 D、用紫甘蓝汁液检验苹果醋2. 关于空气成分的性质与用途的说法均正确且对应的是 ( )
选项
物质
性质
用途
氮气
化学性质不活泼
保护气
氧气
支持燃烧
作燃料
二氧化碳
还原性
冶炼金属
稀有气体
导电性
制作霓虹灯
A、 B、 C、 D、3. 下列有关水的说法正确的是( )A、通过过滤从海水中获取淡水 B、六大基本营养素不包括水 C、农业上采用滴灌节约用水 D、工业废水可直接排入河道4. 钙是一种活泼金属,在空气中氧化生成氧化钙。钙原子的原子结构示意图如图所示。有关说法正确的是( ) A、钙元素是人体中含量最高的元素 B、 C、钙在化学反应中容易得到电子 D、氧化钙的化学式为5. 古籍辍耕录记载:“杭人削松木为小片,其薄为纸,镕硫磺涂木片顶端分许,名曰发烛”下列说法错误的是( )A、削松木为小片可使燃烧更充分 B、镕硫磺涂木片说明松木不可燃烧 C、“发烛”发火会放出热量 D、“发烛”发火产物会污染空气6. 幸福需要辛勤的劳动来创造。下列劳动项目与所涉及的化学知识不相符的是 ( )
A、钙元素是人体中含量最高的元素 B、 C、钙在化学反应中容易得到电子 D、氧化钙的化学式为5. 古籍辍耕录记载:“杭人削松木为小片,其薄为纸,镕硫磺涂木片顶端分许,名曰发烛”下列说法错误的是( )A、削松木为小片可使燃烧更充分 B、镕硫磺涂木片说明松木不可燃烧 C、“发烛”发火会放出热量 D、“发烛”发火产物会污染空气6. 幸福需要辛勤的劳动来创造。下列劳动项目与所涉及的化学知识不相符的是 ( )用发酵粉焙制糕点
能产生
用布擦干淋湿的自行车
铁部件潮湿易生锈
用洗洁精清洗有油污的碗筷
洗洁精能溶解油污
施用碳酸氢铵化肥后,应及时盖土
碳酸氢铵不稳定
A、 B、 C、 D、7. 实验室用固体氢氧化钠配制质量分数为的氢氧化钠溶液。下列说法错误的是( )A、计算:所需固体氢氧化钠的质量是 B、称量:将固体氢氧化钠直接放在托盘上 C、量取:用的量筒和滴管量取所需的水 D、溶解:用玻璃棒搅拌加快氢氧化钠溶解8. 某品牌的泡腾片说明书如图所示。有关说法错误的是 ( )配料:每片含维生素
辅料:柠檬酸、碳酸氢钠等
用法:用冷水或温水溶解后服用
A、维生素和柠檬酸的组成元素相同 B、氧元素的质量分数:维生素柠檬酸 C、泡腾片放入水中可观察到气泡 D、柠檬酸在水中可解离出9. 下列说法中错误的是( )A、煤炭脱硫能减少酸雨的产生 B、回收利用废旧电池能保护水源 C、用天然气作燃料可消除温室效应 D、使用可降解塑料可减少“白色污染”10. 通过“人造树叶”模拟光合作用,和在光照的条件下转化成其他物质的反应微观示意图如图,下列说法错误的是( ) A、物质不含有碳元素 B、该反应将太阳能转化为化学能 C、利用该反应开发新能源 D、在工业生产中应严禁烟火11. 时,在装有氯化钠饱和溶液的甲烧杯中加入水,后变为乙烧杯,有关描述正确的是 ( )
A、物质不含有碳元素 B、该反应将太阳能转化为化学能 C、利用该反应开发新能源 D、在工业生产中应严禁烟火11. 时,在装有氯化钠饱和溶液的甲烧杯中加入水,后变为乙烧杯,有关描述正确的是 ( )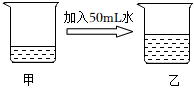
已知时,氯化钠饱和溶液的密度是
A、甲、乙溶液中存在的微粒只有和 B、甲、乙溶液中氯化钠的溶解度:甲乙 C、甲、乙溶液中溶质的质量相等 D、甲、乙溶液中溶质的质量分数:12. 和在催化剂的作用下发生反应的微观示意图如图,下列说法正确的是 ( ) A、反应前后分子和原子的种类保持不变 B、参加反应物质分子个数之比为: C、该反应涉及种氧化物 D、反应前后氮元素化合价发生变化13. 下列实验方案中,能达到实验目的的是 ( )
A、反应前后分子和原子的种类保持不变 B、参加反应物质分子个数之比为: C、该反应涉及种氧化物 D、反应前后氮元素化合价发生变化13. 下列实验方案中,能达到实验目的的是 ( )选项
实验目的
实验方案
区分羊毛纤维和合成纤维
取样,灼烧,闻气味
除去氯化钾中的氯酸钾
加入适量二氧化锰后,加热
除去气体中的气体
将气体通入足量的溶液中
鉴别和固体
将固体溶于水,观察固体是否溶解
A、 B、 C、 D、14. 由下列实验操作及现象所得到的结论错误的是 ( )选项
实验操作及现象
结论
将黄铜片铜锌合金与铜片相互刻画,铜片上有刻痕
黄铜片的硬度比铜片大
往放有少量锌片、铜片的两支试管中加入稀盐酸,观察到锌片上有气泡产生,铜片上没有气泡产生
锌的金属活动性比铜强
向稀硫酸中加入氧化铜,溶液的变大
硫酸和氧化铜发生反应
取硝酸钾固体少量,加入少量熟石灰粉末,混合、研磨,未能闻到刺激性气味
氮肥与碱作用都无刺激性气体产生
A、 B、 C、 D、二、非选择题
-
15. 我国科技成果斩获重大创新和突破,在世界科技舞台留下了浓墨重彩的印记。(1)、研究发明了海水无淡化原位直接电解制氢技术,该技术的关键是利用海水和电解池内压力差使水蒸馏到电解池内,再加入溶液作为电解液进行电解。
电解液因含有 填离子符号而增强水的导电性。
电解水的化学方程式为 。
(2)、研究创建了一种将二氧化碳转化为葡萄糖的新工艺:
气体能使带火星的木条复燃,该气体是 写化学式。
写出装置中反应的化学方程式为 。
为保证醋酸转化成葡萄糖的高效性,反应的温度应控制为 填“高温”或“低温”。
该新工艺给人类带来的重大意义是 写一点。
16. 利用手持技术探究一定体积的空气与过量铜片的反应如图 , 利用数据采集器绘得装置内的“氧气含量时间”曲线如图。 (1)、加入铜片前要对装置进行 检查。(2)、根据图可以判断反应发生的曲线是 填标号。
(1)、加入铜片前要对装置进行 检查。(2)、根据图可以判断反应发生的曲线是 填标号。段
②BC段
段
(3)、加热时,铜与氧气反应的化学方程式为 。(4)、反应后恢复到室温,玻璃管内的气体压强 填“增大”、“不变”或“减小”。(5)、该实验能证明铜与氧气发生了化学变化的证据有 、 。17. 碳酸锂是制备锂电池的重要原料。工业上以锂辉石精矿主要成分是和 , 和其他杂质既不溶于水也不溶于酸为原料制取碳酸锂的工艺流程如下:
查阅资料:与在不同温度下的溶解度如下表:
温度
的溶解度
的溶解度
(1)、“酸浸”发生反应的化学方程式为 。(2)、滤渣的主要成分是 写化学式。“沉锂”过程中发生的基本反应类型是 。(3)、从滤液中回收适宜采用的操作是蒸发浓缩、 、过滤。(4)、用热水洗滤渣的原因是 。(5)、若固体中含有少量杂质 , 请简述提纯的实验操作: 。18. 盐酸是重要的化工产品,用途广泛。 (1)、工业上,氯化氢由氯气和氢气在点燃条件下化合得到,该反应的化学方程式为 ,将生成的产物溶于水得到盐酸。(2)、实验室用盐酸制取二氧化碳,装置如图所示,仪器的名称是 ,该反应的化学方程式为 。
(1)、工业上,氯化氢由氯气和氢气在点燃条件下化合得到,该反应的化学方程式为 ,将生成的产物溶于水得到盐酸。(2)、实验室用盐酸制取二氧化碳,装置如图所示,仪器的名称是 ,该反应的化学方程式为 。 (3)、兴趣小组进一步探究浓盐酸的性质,开展了如下实验:
(3)、兴趣小组进一步探究浓盐酸的性质,开展了如下实验:先同时打开、止水夹,观察到段玻璃管内紫色石蕊试纸 。
再同时打开、止水夹,可观察到段玻璃管处出现白烟,该白烟是与化合生成的产物 写化学式。
通过以上实验得出浓盐酸具有的物理性质是 。
(4)、人体胃液中含有盐酸,胃酸过多会造成胃不舒服,需要服用胃药缓解,下列物质可作胃药成分的是 ____ 。填标号A、氢氧化钠 B、氢氧化镁 C、碳酸氢钠 D、氯化镁19. 硫酸亚铁铵【】是一种重要的化工原料,可作净水剂,作木材防腐剂,医药中用于治疗缺铁性贫血等。(1)、具有两种盐的性质,一种是 , 另一种是 写化学式。(2)、是可溶性盐,从微粒组成分析,推测其具有的化学性质有 ____ 填标号。A、能与反应 B、能与稀盐酸反应 C、能与溶液反应 D、能与溶液反应(3)、产品以废铁屑、硫酸、硫酸铵饱和溶液为原料制取。首先,将洗净后的铁屑用过量稀硫酸溶解,该反应的化学方程式为 。
接着,加入一定量的硫酸铵饱和溶液,缓缓加热,浓缩至表面出现结晶薄膜为止。过滤后用无水乙醇洗涤。由此说明产品在无水乙醇中的溶解度 填“大”或“小”。
(4)、另外设计三种制取硫酸亚铁的方案要求含铁原料分别属于不同的物质类别。方案
预期反应的化学方程式
依据的反应规律
金属单质与盐溶液反应
金属氧化物与酸反应
20. 某融雪剂可能由、、和中的一种或两种物质组成。为了探究融雪剂的物质组成,兴趣小组进行了实验:取少量的融雪剂于试管中,加足量水,振荡,观察到固体溶解得到无色澄清的溶液,然后向溶液中滴加溶液,有白色沉淀产生。(1)、根据上述实验分析写出产生白色沉淀的化学方程式 。
推测融雪剂的组成
推测一:和
推测二:
(2)、为了进一步确定融雪剂的组成,设计了如下实验方案:方案一:通过测定物质溶解时温度的变化来确定。
设计如下对比实验,的最大数值是 ,数据现象记录如下表。已知时,的溶解度是 , 的溶解度是74.5g)

实验序号
加入溶质前的水温
溶解现象
全部溶解
全部溶解
溶解后溶液的温度
根据实验,不能确定融雪剂的组成。
方案二:通过测定融雪剂中的含量来确定。
取的融雪剂于试管中,加足量水溶解,再加入过量溶液,充分反应, 、干燥、称量得到沉淀。由此可证明融雪剂是由和组成的,理由是 。