广东省深圳市宝安区2023年中考化学二模试卷
试卷更新日期:2023-10-13 类型:中考模拟
一、选择题
-
1. 2023年深圳宝安马拉松于3月19日举行。有关说法不正确的是( )A、发令枪内含有红磷,鸣枪时产生白烟的过程是物理变化 B、赛道补给的云片糕、花生糖等可提供能量 C、跑步后的急促呼吸,属于缓慢氧化 D、赛后将废弃物回收再利用,体现可持续发展理念2. 下列化学用语表述正确的是 ( )A、2个氯分子:2Cl B、铵根离子: C、氧化钙中钙元素的化合价: D、铝片在空气中被氧化:3. 如图是元素周期表的一部分。相关说法不正确的是( )
 A、磷元素的相对原子质量为30.97 B、①处的数字应为16,可推知硫原子的质子数为16 C、硒元素属于金属元素 D、硒原子核外有34个电子4. 2023年“世界水日”“中国水周”的主题为“强化依法治水、携手共护母亲河”。有关水的说法正确的是( )A、水分子由氢元素和氧元素构成 B、工业废水应处理达标后再排放 C、使用活性炭对河水进行杀菌消毒 D、禁止化肥和农药的使用,以免污染水资源5. 剧烈运动后肌肉酸痛是部分葡萄糖(C6H12O6)转化成乳酸(C3H6O3)引起的,有关说法正确的是( )A、葡萄糖(C6H12O6)中含有6个氧原子 B、葡萄糖(C6H12O6)中碳、氢、氧元素的质量比为1:2:1 C、乳酸(C3H6O3)在体内完全氧化的产物是CO和H2O D、葡萄糖(C6H12O6)和乳酸(C3H6O3)中,氢元素的质量分数相等6. 高压臭氧除甲醛反应的微观图示如下。有关说法正确的是( )
A、磷元素的相对原子质量为30.97 B、①处的数字应为16,可推知硫原子的质子数为16 C、硒元素属于金属元素 D、硒原子核外有34个电子4. 2023年“世界水日”“中国水周”的主题为“强化依法治水、携手共护母亲河”。有关水的说法正确的是( )A、水分子由氢元素和氧元素构成 B、工业废水应处理达标后再排放 C、使用活性炭对河水进行杀菌消毒 D、禁止化肥和农药的使用,以免污染水资源5. 剧烈运动后肌肉酸痛是部分葡萄糖(C6H12O6)转化成乳酸(C3H6O3)引起的,有关说法正确的是( )A、葡萄糖(C6H12O6)中含有6个氧原子 B、葡萄糖(C6H12O6)中碳、氢、氧元素的质量比为1:2:1 C、乳酸(C3H6O3)在体内完全氧化的产物是CO和H2O D、葡萄糖(C6H12O6)和乳酸(C3H6O3)中,氢元素的质量分数相等6. 高压臭氧除甲醛反应的微观图示如下。有关说法正确的是( ) A、
A、 属于氧化物
B、反应Ⅰ中,反应前后氧原子个数增加
C、反应Ⅱ中,参加反应的反应物分子的个数比为1:2
D、整个过程中,可循环使用
7. 下列陈述Ⅰ与陈述Ⅱ均正确,且具备因果关系的是( )
属于氧化物
B、反应Ⅰ中,反应前后氧原子个数增加
C、反应Ⅱ中,参加反应的反应物分子的个数比为1:2
D、整个过程中,可循环使用
7. 下列陈述Ⅰ与陈述Ⅱ均正确,且具备因果关系的是( )选项
陈述Ⅰ
陈述Ⅱ
A
石墨具有导电性
石墨常用作铅笔芯
B
厨余垃圾含N、P、K等元素
厨余垃圾制花肥
C
铝的化学性质比铁活泼
铝比铁更耐腐蚀
D
氢氧化钠能与酸反应
氢氧化钠常用于改良酸性土壤
A、A B、B C、C D、D8. 下列设计能达到实验目的的是( )A、探究铁生锈是否需要水 B、探究可燃物燃烧是否需要氧气
B、探究可燃物燃烧是否需要氧气 C、测定空气中氧气含量
C、测定空气中氧气含量 D、验证质量守恒定律
D、验证质量守恒定律 9. 铁是使用最广泛的金属。(图中“——”表示物质可以反应,“→”表示物质转化方向)下列说法正确的是( )
9. 铁是使用最广泛的金属。(图中“——”表示物质可以反应,“→”表示物质转化方向)下列说法正确的是( ) A、赤铁矿炼铁的原理是CO+Fe2O3=2Fe+3CO2 B、反应①是一个吸热反应 C、反应②的现象为出现气泡,溶液变浅绿色 D、反应③的盐溶液可以为溶液10. 小明在“海洋资源的综合利用与制盐”的实践活动中制得的盐中除NaCl外,还含有、 , 它们的溶解度曲线如图。下列说法正确的是( )
A、赤铁矿炼铁的原理是CO+Fe2O3=2Fe+3CO2 B、反应①是一个吸热反应 C、反应②的现象为出现气泡,溶液变浅绿色 D、反应③的盐溶液可以为溶液10. 小明在“海洋资源的综合利用与制盐”的实践活动中制得的盐中除NaCl外,还含有、 , 它们的溶解度曲线如图。下列说法正确的是( ) A、溶解度最小的是NaCl B、40℃时,MgCl2溶液中溶质的质量分数为57.5% C、70℃时,MgSO4饱和溶液升高温度或降低温度都可能析出晶体 D、从含有NaCl、MgCl2、MgSO4的溶液中提取NaCl可采用降温结晶的方法11. 下列实验方法能达到实验目的的是( )
A、溶解度最小的是NaCl B、40℃时,MgCl2溶液中溶质的质量分数为57.5% C、70℃时,MgSO4饱和溶液升高温度或降低温度都可能析出晶体 D、从含有NaCl、MgCl2、MgSO4的溶液中提取NaCl可采用降温结晶的方法11. 下列实验方法能达到实验目的的是( )选项
实验目的
实验方法
A
鉴别NaOH和NH4NO3
取样,加水溶解,测温度
B
检验工业废水中是否含有硫酸
取样,滴加无色酚酞溶液,观察颜色
C
除去O2中的水蒸气
通过足量的稀硫酸
D
分离Na2CO3和NaCl的混合物
溶解后过滤,洗涤滤渣,蒸发滤液
A、A B、B C、C D、D12. 如图1所示,分别将等体积H2O、NaOH溶液注入充满CO2的锥形瓶,测得气压变化如图2。有关说法不正确的是( ) A、曲线①表示的是将H2O注入充满CO2的锥形瓶后的气压变化 B、由曲线②可知,反应后锥形瓶内的CO2仍有剩余 C、对比曲线①和②可知,CO2能与NaOH溶液反应 D、A点表示CO2与锥形瓶内的溶液恰好完全反应,则此时溶液pH=7
A、曲线①表示的是将H2O注入充满CO2的锥形瓶后的气压变化 B、由曲线②可知,反应后锥形瓶内的CO2仍有剩余 C、对比曲线①和②可知,CO2能与NaOH溶液反应 D、A点表示CO2与锥形瓶内的溶液恰好完全反应,则此时溶液pH=7二、非选择题
-
13. 根据如图回答:
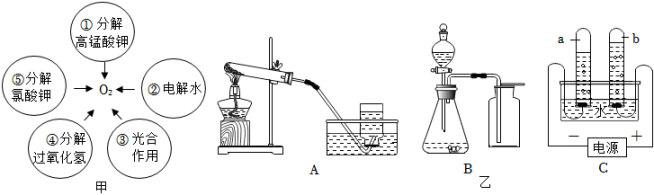 (1)、图甲中,可用于实验室制取氧气的途径有 用①⑤填写 , 其中,从环保和节约资源的角度分析,实验室制取的最佳途径的反应原理 写化学方程式。(2)、在图乙的装置中,装置 填“A”“B”“C”既可以用来制取 , 又可用于制取。选用该装置制取的化学方程式为 。(3)、查阅资料可知:①浓氨水受热易分解产生;②密度比空气小。
(1)、图甲中,可用于实验室制取氧气的途径有 用①⑤填写 , 其中,从环保和节约资源的角度分析,实验室制取的最佳途径的反应原理 写化学方程式。(2)、在图乙的装置中,装置 填“A”“B”“C”既可以用来制取 , 又可用于制取。选用该装置制取的化学方程式为 。(3)、查阅资料可知:①浓氨水受热易分解产生;②密度比空气小。实验室常用CaO和浓氨水可快速制取的原因是 ,但利用该方法不能用装置B制取 , 理由是 。
14. 化学小组对过氧碳酸钠的性质进行探究。(1)、【查阅资料】与反应可生成和。该反应的化学方程式为① 。
与酸反应产生气体。
的产品优劣可用“活性氧”衡量,活性氧含量越高,产品越优。
(2)、【提出问题】与稀硫酸反应的气体产物是什么?
【形成假设】猜想一:只有;猜想二:只有;猜想三:② 。(3)、【设计并进行实验】组装如图所示的装置进行实验。
实验前,先通一段时间 , 再点燃酒精灯。通的目的是③ 。
打开分液漏斗的活塞,将稀硫酸滴入锥形瓶中。装置B中的溶液为④ ,装置B中反应的化学方程式为⑤ 。
(4)、【现象与结论】装置B中溶液变浑浊,装置C中固体变成黑色,说明⑥ 填“猜想一”“猜想二”或“猜想三”成立。(5)、【思考与交流】可由和制得,反应温度对产率、活性氧含量的影响如图,由图可知最佳反应温度的范围是⑦ 。A.
B.
C.
D.
 15. 利用磷尾矿粉主要成分为、等制备的流程如下:
15. 利用磷尾矿粉主要成分为、等制备的流程如下:
查阅资料:的化学性质与类似;难溶于水。
(1)、过程Ⅰ中反应的化学方程式为 ,属于 反应填基本反应类型。(2)、过程分离出固体的操作是 。(3)、过程的化学方程式为 。(4)、该制备流程中最终产品除获得外,还可以获得一种物质 写物质名称用作肥料。(5)、如图表示碳元素的部分化合价与物质类别的关系。中碳元素的化合价可表示为点 填“”中的一个字母。 (6)、制取方法还有很多种,在下表中写出合适的反应物。
(6)、制取方法还有很多种,在下表中写出合适的反应物。反应物1
反应物2
NaOH
16. 铜及其化合物广泛应用于生活生产中。(1)、青铜属于 填“金属单质”或“合金”。(2)、 , CuO、三种物质的转化关系如图甲所示:①反应Ⅱ中,CuO与稀硫酸反应的现象是 。
②反应Ⅲ中, 填化学式可将CuO一步转化为Cu。
③图乙所示的实验中,将铜片浸入 填化学式溶液中,可根据现象证明Cu的金属活动性比Ag强。
(3)、往四个都装有15g样品只含Cu和的烧杯中,分别加入不同质量的稀硫酸,反应过程中的质量关系如下表所示,计算所用稀硫酸的溶质质量分数。烧杯序号
一
二
三
四
稀硫酸的质量
50
100
150
200
剩余固体质量
11
7
3
3
