2023-2024 学年 浙教版科学九年级上册 第2章 物质转化与材料利用 复习
试卷更新日期:2023-10-07 类型:同步测试
一、选择题
-
1. 下图表示的是气体分子的模型,图中
 和
和 分别表示不同元素的原子,其中表示混合物模型的是( ) A、
分别表示不同元素的原子,其中表示混合物模型的是( ) A、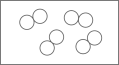 B、
B、 C、
C、 D、
D、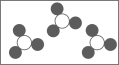 2. 向一定质量的AgNO3溶液中加入铜、锌的混合粉末,充分反应后过滤,得到溶液甲和固体乙,下列判断不正确的是( )A、若固体乙中含有铜、银、锌三种金属,则溶液甲中的溶质是AgNO3 B、若向溶液甲中滴加氯化钠溶液产生白色沉淀,则固体乙是Ag和Cu C、若溶液甲呈蓝色,则固体乙中一定含Ag,可能含有Cu D、若将固体乙加入到Cu(NO3)2溶液中,则有红色物质析出3. 据报道,杭州亚运会火炬“薪火”将以生物质燃气为燃料。生物质燃气是以农作物秸秆、禽畜粪便等含有生物质体的物质为原料,在一定条件下制成含有氢气、一氧化碳、甲烷等的生物质燃气。其中的一个反应是水气和碳在高温条件产生一氧化碳和氢气。下列有关叙述中,正确的是( )A、生物质燃气中只有无机物 B、生物质燃气中的物质都是化合物 C、产生一氧化碳的反应中,碳具有还原性 D、生物质燃气燃烧是吸热反应4. 有一包白色固体,可能由硫酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成。为探究该白色固体的组成,某小组取样溶于水,有白色沉淀产生,过滤后向该沉淀加适量稀盐酸,沉淀全部溶解;同时往滤液中通入CO2气体,滤液变浑浊。由此推断该白色固体中( )A、可能存在硫酸钾 B、一定存在氢氧化钾 C、可能存在氯化钡 D、有且仅有两种物质构成5. 2008年北京奥运会“祥云”火炬、2022年北京冬奥会“飞扬”火炬的外壳材料的主要成分和燃料如表所示。奥运火炬的迭代,体现了我国科技水平的提高。下列有关两火炬的说法错误的是( )
2. 向一定质量的AgNO3溶液中加入铜、锌的混合粉末,充分反应后过滤,得到溶液甲和固体乙,下列判断不正确的是( )A、若固体乙中含有铜、银、锌三种金属,则溶液甲中的溶质是AgNO3 B、若向溶液甲中滴加氯化钠溶液产生白色沉淀,则固体乙是Ag和Cu C、若溶液甲呈蓝色,则固体乙中一定含Ag,可能含有Cu D、若将固体乙加入到Cu(NO3)2溶液中,则有红色物质析出3. 据报道,杭州亚运会火炬“薪火”将以生物质燃气为燃料。生物质燃气是以农作物秸秆、禽畜粪便等含有生物质体的物质为原料,在一定条件下制成含有氢气、一氧化碳、甲烷等的生物质燃气。其中的一个反应是水气和碳在高温条件产生一氧化碳和氢气。下列有关叙述中,正确的是( )A、生物质燃气中只有无机物 B、生物质燃气中的物质都是化合物 C、产生一氧化碳的反应中,碳具有还原性 D、生物质燃气燃烧是吸热反应4. 有一包白色固体,可能由硫酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成。为探究该白色固体的组成,某小组取样溶于水,有白色沉淀产生,过滤后向该沉淀加适量稀盐酸,沉淀全部溶解;同时往滤液中通入CO2气体,滤液变浑浊。由此推断该白色固体中( )A、可能存在硫酸钾 B、一定存在氢氧化钾 C、可能存在氯化钡 D、有且仅有两种物质构成5. 2008年北京奥运会“祥云”火炬、2022年北京冬奥会“飞扬”火炬的外壳材料的主要成分和燃料如表所示。奥运火炬的迭代,体现了我国科技水平的提高。下列有关两火炬的说法错误的是( )“祥云”火炬
“飞扬”火炬
外壳材料的主要成分
铝合金
碳纤维复合材料
燃料
丙烷(C3H8)
氢气(H2)
A、铝合金属于金属 B、火炬熄灭,温度降低,着火点不变 C、燃料燃烧时,助燃剂都是氧气 D、“飞扬”火炬的燃烧产物更环保6. 青铜是冶铸史上最早出现的Cu、Sn(锡)合金,与纯铜相比,耐磨且耐腐蚀。下列描述中错误的是( )A、青铜是Cu和Sn(锡)发生化合反应生成的化合物 B、将青铜屑加入足量的稀盐酸中,会有气泡产生 C、用CuSO4溶液能验证Cu、Sn的金属活动性强弱 D、青铜是铜的合金,因此青铜属于金属材料7. 哈佛大学科学家将固态氢置于488万个标准大气压下,氢分子破裂为氢原子,由氢原子直接构成金属氢。金属氢具有金属的性质,还具有超导性。用它输电,其输电效率可以提高几十倍。以下说法合理的是( )A、金属氢属于无机化合物 B、形成金属氢的过程中氢原子核发生改变 C、金属氢和氢气互为同位素 D、用金属氢输电可减少导线发热造成的能量损失8. 向一定质量的Na2CO3溶液中滴加一定质量的Ba(OH)2溶液,反应一段时间后改为滴加Ca(OH)2溶液,当恰好不再产生沉淀时,再滴加稀盐酸至沉淀消失。反应过程中产生沉淀的质量与加入物质的质量关系如图所示。下列说法错误的是( ) A、a点溶液中溶质只有NaOH B、c﹣d段发生反应的化学方程式为NaOH+HCl═NaCl+H2O C、整个过程溶液中的溶质种类最多含有3种 D、d﹣e段有气泡产生9. 《天工开物》中记载烧制青砖时”火候足,止薪之候,泥固塞其孔,然后使水转釉”。该过程的主要化学反应为:Fe2O3+CO2FeO+CO2。下列说法正确的是( )
A、a点溶液中溶质只有NaOH B、c﹣d段发生反应的化学方程式为NaOH+HCl═NaCl+H2O C、整个过程溶液中的溶质种类最多含有3种 D、d﹣e段有气泡产生9. 《天工开物》中记载烧制青砖时”火候足,止薪之候,泥固塞其孔,然后使水转釉”。该过程的主要化学反应为:Fe2O3+CO2FeO+CO2。下列说法正确的是( ) A、该反应属于置换反应 B、CO的相对分子质量为28克 C、FeO中铁元素的化合价为+2价 D、塞住砖窑的通气孔,窑内柴火会较快熄灭,是由于缺少可燃物10. 小敏在鉴别氢气、氮气、氧气、二氧化碳四瓶无色气体时,对它们的部分性质进行归纳梳理并编制了检索表(如图)。检索表中S代表的是( )
A、该反应属于置换反应 B、CO的相对分子质量为28克 C、FeO中铁元素的化合价为+2价 D、塞住砖窑的通气孔,窑内柴火会较快熄灭,是由于缺少可燃物10. 小敏在鉴别氢气、氮气、氧气、二氧化碳四瓶无色气体时,对它们的部分性质进行归纳梳理并编制了检索表(如图)。检索表中S代表的是( )检索表
1a具有可燃性...............P
1b不具有可燃性...............2
2a能使澄清石灰水变浑........Q
2b不能使澄清石灰水变浑.......3
3a能使带火星的木条复......R
3b不能使带火星的木条复..... S
A、氢气 B、氮气 C、氧气 D、二氧化碳11. 物质的鉴别是重要的实验技能。鉴别下列各组物质所用试剂或方法选择错误的是( )选项
需鉴别物质
试剂或方法
A
铁粉、木炭粉
磁铁吸引
B
盐酸、氯化钠溶液
硝酸银溶液
C
氧气、二氧化碳气体
用燃着的木条
D
氢氧化钠固体、氯化钠固体
水
A、A B、B C、C D、D12. “灰汁团”是宁波传统小吃,制作过程中要用到大米和“灰汁”。“灰汁”制取方法如资料卡所示,下列说法错误的是( ) A、大米中含有的淀粉属于有机物 B、稻草燃烧属于物理变化 C、传统方法制得的“灰汁”是混合物 D、现代方法制得的“灰汁”能使酚酞试液变红色13. 有一包固体样品,可能含氯化铁、硫酸钠、氢氧化钡、氢氧化钠中的一种或几种。小宁进行了如下实验.根据实验现象,下列判断错误的是( )
A、大米中含有的淀粉属于有机物 B、稻草燃烧属于物理变化 C、传统方法制得的“灰汁”是混合物 D、现代方法制得的“灰汁”能使酚酞试液变红色13. 有一包固体样品,可能含氯化铁、硫酸钠、氢氧化钡、氢氧化钠中的一种或几种。小宁进行了如下实验.根据实验现象,下列判断错误的是( )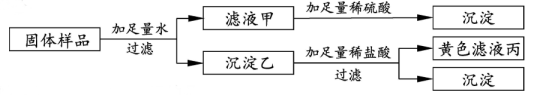 A、滤液丙中含有氯化铁 B、沉淀乙为氢氧化铁、硫酸钡 C、滤液甲中一定不存在氢氧化钠 D、样品中一定有氯化铁、硫酸钠、氢氧化钡14. 小明将甲、乙、丙三种金属与两种溶液反应,并根据实验现象编制了如图的检索表,根据检索表可知甲、乙、丙三种金属的活动性顺序为( )
A、滤液丙中含有氯化铁 B、沉淀乙为氢氧化铁、硫酸钡 C、滤液甲中一定不存在氢氧化钠 D、样品中一定有氯化铁、硫酸钠、氢氧化钡14. 小明将甲、乙、丙三种金属与两种溶液反应,并根据实验现象编制了如图的检索表,根据检索表可知甲、乙、丙三种金属的活动性顺序为( ) A、甲>乙>丙 B、乙>丙>甲 C、丙>甲>乙 D、甲>丙>乙15. 长征七号火箭采用无毒无污染的液氧、煤油作为推进剂,煤油的成分之一可用CH3(CH2)10CH3表示。下列说法正确的是( )A、液氧属于混合物 B、CH3(CH2)10CH3 属于无机物 C、保持液氧化学性质的最小微粒是氧分子 D、CH3(CH2)10CH3 可以燃烧,具有助燃性
A、甲>乙>丙 B、乙>丙>甲 C、丙>甲>乙 D、甲>丙>乙15. 长征七号火箭采用无毒无污染的液氧、煤油作为推进剂,煤油的成分之一可用CH3(CH2)10CH3表示。下列说法正确的是( )A、液氧属于混合物 B、CH3(CH2)10CH3 属于无机物 C、保持液氧化学性质的最小微粒是氧分子 D、CH3(CH2)10CH3 可以燃烧,具有助燃性二、实验探究题
-
16. 探究盐酸的化学性质,某化学小组做了如下实验:

将反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质成分进行探究:(提出问题)滤液中溶质的成分是什么?(作出猜想)
猜想一:NaCl
猜想二:NaCl和CaCl2
猜想三:
猜想四:NaCl、Ca(OH)2和HCl
同学们马上否定了猜想四,请问他们否定的理由是什么?
(设计实验)请完成实验报告。
实验步骤
实验现象
实验结论
取少量滤液于试管中,滴加适量的碳酸钠溶液。
①
猜想二不成立
取少量滤液于试管中,滴加②_(填名称)。
产生气泡
猜想三成立
17. 如图所示是木炭还原氧化铜的实验,小科对碳与氧化铜反应生成的气体成分进行探究。[提出问题]碳燃烧时可能生成CO2 , 也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
[作出猜想]
猜想①:CO;猜想②:CO2;
猜想③:CO和CO2。
[设计方案]打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气。
方案一:从定性观察角度判断
(1)、若观察到B中澄清石灰水变浑浊,则可排除猜想。(2)、实验结束后,需要先熄灭(选填“A”或“D”)酒精灯。(3)、方案二:从定量计算角度判断取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:反应前的质量
反应后的质量
A(玻璃管+固)
m1
m2
B+C+(广口瓶+混合液)
m3
m4
若猜想②成立,则理论上(m4-m3)(m1-m2)(填“>”“=”或“<”)。
(4)、若猜想③成立且CuO全部转化成Cu,则参加反应碳的质量m的取值范围是。18. 研究小组同学在完成”酸的性质”实验①②后,将①②实验后试管中的物质全部倒入各自废液缸③中(如图甲),结果出现了不同现象,部分小组同学的实验现象记录如下表。
组别
废液缸中现象
现象解释
第1小组
无沉淀、有气泡产生
第2小组
无沉淀、无气泡产生
第3小组
……
……
……
[原理分析]小组同学在老师指导下讨论后认为:任何一个化学反应,反应物的用量不同,反应后物质的组成成分就会不同,这是最终导致各组废液缸中出现不同现象的原因。
[交流讨论]
(1)、为分析第1小组废液缸中溶液的溶质成分,用玻璃棒蘸取溶液测得pH=3,则该小组废液中的溶质组成成分为 (写化学式);(2)、第2小组废液缸中无沉淀、无气泡产生,从反应物用量的角度分析实验①②,可以得出该小组的实验②中反应物盐酸的用量应该是;(3)、如果其他小组实验所用反应物的用量都不一样,除了上面第1、2小组出现的现象外,还会出现的现象是。(4)、 [实验拓展]取第1小组废液缸中的溶液于试管中,逐滴溶加入碳酸钠溶液,并振荡,产生的气体全部逸出。图乙表示”溶液质量”随加入”碳酸钠溶液质量”的变化情况。
解释图中AB段和BC段溶液质量呈现不同增重趋势的原因。
19. 某科学兴趣小组的同学对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。他们称取了13.6g固体样品,用图甲所示的装置继续实验,测定的部分数据如图乙所示。 (1)、请写出玻璃管内发生的化学方程式 。(2)、固体样品中氧化铁的质量是 克。
(1)、请写出玻璃管内发生的化学方程式 。(2)、固体样品中氧化铁的质量是 克。三、填空题
-
20. 整理和归纳是有效的学习方法。下面是某学习小组的同学对Mg、Fe、Cu、Hg、Ag五种金属相关知识的归纳复习,请你参与并回答问题:(1)、从物理性质上看,每种金属都有自己的特性。你认为Hg与其他金属的不同之处是。(2)、从化学性质上看,与盐酸反应最剧烈的是 , 这五种金属中,有一种金属的化合物溶液能与其他四种金属发生反应,请写出铁与该盐溶液反应得方程式。(3)、性质决定用途,用途反映性质是重要的化学学科思想。用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的性。21. 无土栽培是利用营养液栽培作物的一种方法。现有一种无色营养液,可能由KNO3、K2CO3、Ca(NO3)2和KCl中的一种或几种物质组成,为探究其成分,小宁设计并完成了如上图所示的实验。根据以上实验,请你进行有关推断。
 (1)、由实验1可确定原营养液中一定没有的物质是。(2)、由实验1和实验2可推测原营养液(填“一定有”或“可能有”)KCl。(3)、若测得原营养液中K+和Cl﹣的数目之比为3:2,则原营养液的组成中的溶质是。22. 钐在元素周期表中的信息如图所示。钐的应用较为广泛,钐钴磁体是现今第二强磁性的磁铁。钐-153同位素是治疗癌症的重要药物。
(1)、由实验1可确定原营养液中一定没有的物质是。(2)、由实验1和实验2可推测原营养液(填“一定有”或“可能有”)KCl。(3)、若测得原营养液中K+和Cl﹣的数目之比为3:2,则原营养液的组成中的溶质是。22. 钐在元素周期表中的信息如图所示。钐的应用较为广泛,钐钴磁体是现今第二强磁性的磁铁。钐-153同位素是治疗癌症的重要药物。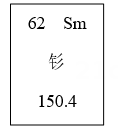 (1)、下列材料中,能被钐钴磁体吸引的是______。A、铁 B、钴 C、铜(2)、钐-153放射性同位素原子的中子数为。(3)、请写出+3价钐的氧化物化学式。23. 袋装食品中一般会放置一包干燥剂,干燥剂种类各不相同,氧化钙是比较常见的一种。(1)、氧化钙吸水的过程会 (选填“吸收”或 者“释放")热量。(2)、取少量氧化钙放入水中,所得溶液呈 (选填“酸性”、“碱性"或者“中性")。(3)、暴露在空气中的氧化钙,可能会转变成。24. 实验室处理含铜废液的过程中,部分流程如下图:
(1)、下列材料中,能被钐钴磁体吸引的是______。A、铁 B、钴 C、铜(2)、钐-153放射性同位素原子的中子数为。(3)、请写出+3价钐的氧化物化学式。23. 袋装食品中一般会放置一包干燥剂,干燥剂种类各不相同,氧化钙是比较常见的一种。(1)、氧化钙吸水的过程会 (选填“吸收”或 者“释放")热量。(2)、取少量氧化钙放入水中,所得溶液呈 (选填“酸性”、“碱性"或者“中性")。(3)、暴露在空气中的氧化钙,可能会转变成。24. 实验室处理含铜废液的过程中,部分流程如下图: (1)、操作A的名称是。(2)、沉淀物中一定含有。25. 室外的铁制栏杆在多雨季节易生锈,小宁对铁生锈的条件进行了探索,实验装置如图。3天后,发现只有装置C中的铁丝生锈了。
(1)、操作A的名称是。(2)、沉淀物中一定含有。25. 室外的铁制栏杆在多雨季节易生锈,小宁对铁生锈的条件进行了探索,实验装置如图。3天后,发现只有装置C中的铁丝生锈了。 (1)、装置A中生石灰的作用是。(2)、装置B、C中的实验现象说明与接触是铁生锈的条件之一。26. 如图是“铁粉和硫黄反应”的改进实验,将铁粉和硫黄混合物置于两块石英玻璃片之间,并铁粉与硫黄固定。在酒精灯上加热,产生红色火星,固体由棕灰色变为黑色。
(1)、装置A中生石灰的作用是。(2)、装置B、C中的实验现象说明与接触是铁生锈的条件之一。26. 如图是“铁粉和硫黄反应”的改进实验,将铁粉和硫黄混合物置于两块石英玻璃片之间,并铁粉与硫黄固定。在酒精灯上加热,产生红色火星,固体由棕灰色变为黑色。 (1)、铁粉和硫黄在两块玻璃片之间,反应时几乎接触不到氧气,减少了(填化学式)气体的生成,更加环保。(2)、向反应后的黑色固体滴入稀硫酸,有臭鸡蛋气味的硫化氢(H2S)气体产生,说明铁粉和硫黄发生反应。H2S中硫元素的化合价为。(3)、反应后的黑色固体加入CuSO4溶液中,生成红色物质,说明黑色固体中有剩余。27. 从盐湖中提取的某种矿物主要含有KCl,还有少量MgSO4、CaCl2及不溶性杂质SiO2.从该矿物中提取KCl的流程如图:回答下列问题:
(1)、铁粉和硫黄在两块玻璃片之间,反应时几乎接触不到氧气,减少了(填化学式)气体的生成,更加环保。(2)、向反应后的黑色固体滴入稀硫酸,有臭鸡蛋气味的硫化氢(H2S)气体产生,说明铁粉和硫黄发生反应。H2S中硫元素的化合价为。(3)、反应后的黑色固体加入CuSO4溶液中,生成红色物质,说明黑色固体中有剩余。27. 从盐湖中提取的某种矿物主要含有KCl,还有少量MgSO4、CaCl2及不溶性杂质SiO2.从该矿物中提取KCl的流程如图:回答下列问题: (1)、滤渣Ⅰ的主要成分是。(2)、Y溶液中溶质的化学式为。(3)、向滤液Ⅱ中加入过量盐酸的目的是。28. 下列两种方案体现了物质除杂的不同思路:思路一:将杂质直接转化为所需物质;
(1)、滤渣Ⅰ的主要成分是。(2)、Y溶液中溶质的化学式为。(3)、向滤液Ⅱ中加入过量盐酸的目的是。28. 下列两种方案体现了物质除杂的不同思路:思路一:将杂质直接转化为所需物质;思路二:将所需物质转化为中间物质,再将中间物质转化为所需物质。
 (1)、运用思路一:除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶解,再向溶液中加入适量的溶液,过滤、蒸发,即得氯化镁固体。(2)、运用思路二:除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾。根据流程回答以下问题。步骤②中加入的甲溶液是(填化学式)溶液。29. 为除去铜和氧化铜混合物中的氧化铜,达到回收金属铜的目的,小科向混合固体中逐滴加入过量的稀盐酸。
(1)、运用思路一:除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶解,再向溶液中加入适量的溶液,过滤、蒸发,即得氯化镁固体。(2)、运用思路二:除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾。根据流程回答以下问题。步骤②中加入的甲溶液是(填化学式)溶液。29. 为除去铜和氧化铜混合物中的氧化铜,达到回收金属铜的目的,小科向混合固体中逐滴加入过量的稀盐酸。 (1)、实验中稀盐酸需加过量的目的是。(2)、逐滴加入稀盐酸时,可观察到的现象是。(3)、实验后得到金属铜与剩余溶液,小科结合建立模型的方法对反应前后的溶液成分进行分析。图甲为所加稀盐酸中各微粒数量的百分含量,请在图乙中完成反应后溶液中各微粒数量百分含量的模型图。
(1)、实验中稀盐酸需加过量的目的是。(2)、逐滴加入稀盐酸时,可观察到的现象是。(3)、实验后得到金属铜与剩余溶液,小科结合建立模型的方法对反应前后的溶液成分进行分析。图甲为所加稀盐酸中各微粒数量的百分含量,请在图乙中完成反应后溶液中各微粒数量百分含量的模型图。四、解答题
-
30. 在学习“金属的冶炼”时,某学习小组用如图所示的装置测量氧化铜样品中氧化铜的质量分数,实验所取氧化铜样品质量为10克。(所含杂质不参加反应)
 (1)、该实验利用了一氧化碳的性。(2)、甲同学的方法:先称量出玻璃管及样品的总质量为m1 , 待反应完全后再次称量,质量为m2 , 利用m1−m2的值,求出样品中氧化铜的质量分数。其中m1−m2的值是指的质量。(3)、乙同学的方法:先测出氢氧化钠浓溶液的质量为50克,待反应完全后再次称量,质量为54.4克。请你计算样品中氧化铜的质量分数。31. 二氧化氯(ClO2)消毒剂是新一代安全、高效的消毒剂,对新型冠状病毒也具有很强的杀灭作用。如表是某品牌二氧化氯消毒液的部分标签信息,图甲是一种稀释瓶,用户可以根据需求用它以一定体积比对原液进行稀释,图乙是它的7种不同比例的稀释方式。现取原液10mL用该稀释瓶按1:3的比例稀释原液,稀释过程中不考虑温度变化和混合前后的体积变化。求:
(1)、该实验利用了一氧化碳的性。(2)、甲同学的方法:先称量出玻璃管及样品的总质量为m1 , 待反应完全后再次称量,质量为m2 , 利用m1−m2的值,求出样品中氧化铜的质量分数。其中m1−m2的值是指的质量。(3)、乙同学的方法:先测出氢氧化钠浓溶液的质量为50克,待反应完全后再次称量,质量为54.4克。请你计算样品中氧化铜的质量分数。31. 二氧化氯(ClO2)消毒剂是新一代安全、高效的消毒剂,对新型冠状病毒也具有很强的杀灭作用。如表是某品牌二氧化氯消毒液的部分标签信息,图甲是一种稀释瓶,用户可以根据需求用它以一定体积比对原液进行稀释,图乙是它的7种不同比例的稀释方式。现取原液10mL用该稀释瓶按1:3的比例稀释原液,稀释过程中不考虑温度变化和混合前后的体积变化。求:
二氧化氯消毒液
溶质的质量分数
80%
体积
5000mL
密度
1.2g/cm3
强腐蚀性,阴冷,密封储藏
(1)、二氧化氯是(填“无机化合物”或“有机化合物”);二氧化氯中氧、氯元素最根本的区别是不同。(2)、稀释得到的二氧化氯消毒液的密度为g/cm3 , 溶质质量分数为。(计算结果精确到0.1g/cm3和0.1%)32. 某混合溶液由硫酸和硫酸铜溶液组成。小宁进行了如下实验;取200克该混合溶液于烧杯中,然后将240克20%的NaOH溶液分6次加入其中,每次充分反应后称量所得溶液的质量,所测数据如表所示。
第1次
第2次
第3次
第4次
第5次
第6次
加入NaOH溶液的质量/g
40
40
40
40
40
40
反应后溶液的质量/g
240
280
315.1
345.3
375.5
415.5
每次产生沉淀的质量/g
0
0
4.9
m
9.8
0
(1)、上述表格中m=;第二次混合液中的硫酸(填“被”或“未被”)反应完。(2)、求混合溶液中硫酸的质量。(3)、第5次加入NaOH溶液充分反应后所得溶液中溶质的质量分数。(计算结果精确到0.1%)
(4)、画出上述过程中产生沉淀的质量与加入NaOH溶液质量的关系图。33. 用石灰石和砂岩粘土高温煅烧可得一种新型水泥熟料,主要反应为:CaCO3+SiO2 CaSiO3+CO2↑(1)、从物质分类的角度看,CaCO3属于无机化合物中的。(2)、用含CaCO390%的石灰石1000吨生产新型水泥熟料,理论上会排放CO2多少吨?(写出计算过程)(3)、在实验室,用如图所示方法粗略测定石灰石中CaCO3的质量分数,可不用测定的数据是 (填序号) 。 A、取用石灰石样品的质量 B、倒入的过量稀盐酸的质量 C、盐酸接触样品前电子称的读数 D、反应停止后电子秤的读数34. 在某次科学实验创新比赛中,小缙利用生活废品做了一个实验来模拟蒸汽机的工作原理。
A、取用石灰石样品的质量 B、倒入的过量稀盐酸的质量 C、盐酸接触样品前电子称的读数 D、反应停止后电子秤的读数34. 在某次科学实验创新比赛中,小缙利用生活废品做了一个实验来模拟蒸汽机的工作原理。先在油漆桶(如图甲)筒壁上沿同一倾斜方向均匀地戳了三个小孔,然后将90克发热包(如图乙)置于桶内,倒入200mL的冷水后迅速盖紧盖子,用绳子提起油桶,大约20s后,观察到静止的油漆桶小孔冒出大量“白汽”(模型如图丙),并开始快速的旋转,再过10s,油漆桶旋转速度越来越慢直至停止。请用所学知识解释以上现象。【发热包主要成分:氧化钙、铝粉、碳酸钠;铝粉作用:在碱性热水中产生氢气,缓慢放热。】
 35. 如图是小科探究铁生锈条件的装置,a、b两支具支试管中加入形状和大小完全相同的铁片,再向a中加入植物油,U形玻璃管内为红墨水,塞上橡皮塞后U形玻璃管内两端液面相平,整个装置气密性良好,放置一段时间。请写出该实验会出现的现象并解释原因。
35. 如图是小科探究铁生锈条件的装置,a、b两支具支试管中加入形状和大小完全相同的铁片,再向a中加入植物油,U形玻璃管内为红墨水,塞上橡皮塞后U形玻璃管内两端液面相平,整个装置气密性良好,放置一段时间。请写出该实验会出现的现象并解释原因。