沪教版初中化学2023-2024学年九年级上学期第4章 认识化学变化素养检测
试卷更新日期:2023-10-07 类型:单元试卷
一、选择题(每小题4分,共40分)
-
1. 下列图标中属于消防安全标志的是( )
 A、①③ B、①②⑤ C、③ D、②④2. 树立安全意识,掌握科学知识,做到“加强防范,守护生命”。下列做法符合安全要求的是( )A、加油站、面粉加工厂严禁烟火 B、室内起火,迅速打开门窗通风 C、更换灯泡时,不必断开电源开关 D、在高速公路上,汽车超速行驶3. 硝酸铵是一种烈性炸药,当温度达到400 ℃以上时,硝酸铵即可发生爆炸,化学方程式是4NH4NO33N2↑+2X↑+8H2O,其中X的化学式是( )A、NO2 B、O2 C、N2O D、N2O44. 下列化学方程式中书写完全正确的是( )A、铝与稀硫酸反应生成硫酸铝和氢气:Al+H2SO4= AlSO4+H2↑ B、甲烷(CH4)燃烧生成二氧化碳和水:CH4+2O2 CO2+2H2O C、红磷燃烧:2P+O5 P2O5 D、电解水:2H2O 2H2↑+O2↑5. 在一次家庭小实验中,当点燃装有半杯水的纸杯时,发现水面以下部分没有燃烧,其主要原因是( )
A、①③ B、①②⑤ C、③ D、②④2. 树立安全意识,掌握科学知识,做到“加强防范,守护生命”。下列做法符合安全要求的是( )A、加油站、面粉加工厂严禁烟火 B、室内起火,迅速打开门窗通风 C、更换灯泡时,不必断开电源开关 D、在高速公路上,汽车超速行驶3. 硝酸铵是一种烈性炸药,当温度达到400 ℃以上时,硝酸铵即可发生爆炸,化学方程式是4NH4NO33N2↑+2X↑+8H2O,其中X的化学式是( )A、NO2 B、O2 C、N2O D、N2O44. 下列化学方程式中书写完全正确的是( )A、铝与稀硫酸反应生成硫酸铝和氢气:Al+H2SO4= AlSO4+H2↑ B、甲烷(CH4)燃烧生成二氧化碳和水:CH4+2O2 CO2+2H2O C、红磷燃烧:2P+O5 P2O5 D、电解水:2H2O 2H2↑+O2↑5. 在一次家庭小实验中,当点燃装有半杯水的纸杯时,发现水面以下部分没有燃烧,其主要原因是( ) A、纸杯着火点变低 B、温度低于着火点 C、与氧气接触面太小 D、纸杯不是可燃物6. 2023年9月23日在杭州将举办第19届亚洲运动会。运动员在剧烈运动之后,血液中会产生较多的乳酸(C3H6O3),使肌肉酸痛,放松一段时间之后,由于发生如下反应:C3H6O3+3O2= 3CO2+3H2O,而使肌肉的酸痛感消失。从该化学方程式中获取的信息错误的是( )A、反应物是乳酸和氧气 B、生成物是二氧化碳和水 C、参加反应的乳酸与氧气的质量比为45∶16 D、生成的二氧化碳与水的分子个数比为1∶17. 在催化剂作用下,N2和H2反应生成NH3的微观过程示意如下:
A、纸杯着火点变低 B、温度低于着火点 C、与氧气接触面太小 D、纸杯不是可燃物6. 2023年9月23日在杭州将举办第19届亚洲运动会。运动员在剧烈运动之后,血液中会产生较多的乳酸(C3H6O3),使肌肉酸痛,放松一段时间之后,由于发生如下反应:C3H6O3+3O2= 3CO2+3H2O,而使肌肉的酸痛感消失。从该化学方程式中获取的信息错误的是( )A、反应物是乳酸和氧气 B、生成物是二氧化碳和水 C、参加反应的乳酸与氧气的质量比为45∶16 D、生成的二氧化碳与水的分子个数比为1∶17. 在催化剂作用下,N2和H2反应生成NH3的微观过程示意如下: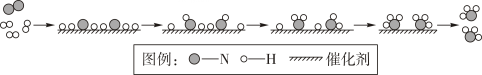
下列说法正确的是( )
A、过程中原子种类不断发生变化 B、过程中H原子数不断减少 C、反应前后分子数未改变 D、NH3不具有N2和H2的化学性质8. 已知白磷的着火点是40 ℃,红磷的着火点是240 ℃。如图实验,三支试管里面充满氮气,初始温度25 ℃,升温至60 ℃后,用注射器同时向②③试管中迅速注入足量氧气。下列说法有误的是( ) A、只有②中有燃烧现象 B、由①②现象说明可燃物达到着火点未必燃烧 C、若继续水浴升温,则③中一定会燃烧 D、该实验能总结出燃烧的条件9. 在一定条件下,把乙炔(C2H2)和氧气放在密闭容器中反应,测得数据如下表,下列说法中正确的是( )
A、只有②中有燃烧现象 B、由①②现象说明可燃物达到着火点未必燃烧 C、若继续水浴升温,则③中一定会燃烧 D、该实验能总结出燃烧的条件9. 在一定条件下,把乙炔(C2H2)和氧气放在密闭容器中反应,测得数据如下表,下列说法中正确的是( )物质(纯净物)
乙炔

二氧
化碳

 氧原子
氧原子 氢原子
氢原子反应前质量/g
26
80
0
0
t1时刻的质量/g
19.5
a
22
4.5
t2时刻的质量/g
0
0
88
b
A、该反应中,乙炔与二氧化碳的化学计量数之比为1∶3 B、b=10 C、t1时刻, 和
和 的质量比为40∶3
D、反应前后,分子和原子的种类均不变
10. 已知:2Na2O2+2CO2= 2Na2CO3+O2。在真空密闭容器中,将13.2 g CO2与一定质量的Na2O2固体充分反应后,收集到气体M为x g。下列说法正确的是( )A、若x=4.8,气体M中含有CO2 B、若x=4.8,生成的Na2CO3的质量为15.9 g C、若x=7.6,Na2O2反应后可能有剩余 D、若x=7.6,气体M中CO2与O2的质量比为11∶8
的质量比为40∶3
D、反应前后,分子和原子的种类均不变
10. 已知:2Na2O2+2CO2= 2Na2CO3+O2。在真空密闭容器中,将13.2 g CO2与一定质量的Na2O2固体充分反应后,收集到气体M为x g。下列说法正确的是( )A、若x=4.8,气体M中含有CO2 B、若x=4.8,生成的Na2CO3的质量为15.9 g C、若x=7.6,Na2O2反应后可能有剩余 D、若x=7.6,气体M中CO2与O2的质量比为11∶8二、填空题(共18分)
-
11. 质量守恒定律对社会发展具有重大意义。请根据质量守恒定律回答下列问题:(1)、H2O、H2O2、KMnO4、KClO3在一定条件下都能反应制得氧气的原因是;研究人员将“铜绿”隔绝空气加热,发现它分解生成了氧化铜、水和二氧化碳,由此得出组成“铜绿”的元素有(填元素符号)。(2)、明代宋应星所著的《天工开物》里记载了我国古代冶金工艺。在炼铁反应3CO+Fe2O3 2Fe+3CO2中,反应前后化合价升高的元素是;铁丝在空气中不能燃烧,在氧气中剧烈燃烧,由此得出的结论是。(3)、科研人员利用催化剂,将两种温室气体进行转化,为“碳中和”提供了一种新的途径,其反应原理如图所示。该反应的化学方程式为。
 12. 书写下列化学方程式。(1)、在氧气中剧烈燃烧,火星四射,生成黑色物质:。(2)、汽车尾气中含有一氧化氮和一氧化碳,会污染空气。有人设计在尾气处加装催化剂,将其转化成无污染的空气中占比最多的一种单质和一种可以灭火的化合物:。(3)、气体打火机用的燃料是丁烷(C4H10),丁烷完全燃烧生成二氧化碳和水,写出其化学方程式:。(4)、写出实验室用双氧水制取氧气的化学方程式:。(5)、金属镁着火不能用二氧化碳扑救,因为镁可以在二氧化碳中继续燃烧生成氧化镁和碳单质,写出其化学方程式:。13. “灭火弹”是一种常见的灭火器材,主要分为沙石灭火弹和干粉灭火弹。目前市场上的灭火弹主要以干粉为主。超细干粉灭火剂是目前国内外已查明的灭火剂中,灭火浓度最低,灭火效能最高,灭火速度最快的一种,且灭火时不会造成火场中人员中毒或窒息死亡。在扑灭森林大火时,可以选用引燃式超细干粉灭火弹。
12. 书写下列化学方程式。(1)、在氧气中剧烈燃烧,火星四射,生成黑色物质:。(2)、汽车尾气中含有一氧化氮和一氧化碳,会污染空气。有人设计在尾气处加装催化剂,将其转化成无污染的空气中占比最多的一种单质和一种可以灭火的化合物:。(3)、气体打火机用的燃料是丁烷(C4H10),丁烷完全燃烧生成二氧化碳和水,写出其化学方程式:。(4)、写出实验室用双氧水制取氧气的化学方程式:。(5)、金属镁着火不能用二氧化碳扑救,因为镁可以在二氧化碳中继续燃烧生成氧化镁和碳单质,写出其化学方程式:。13. “灭火弹”是一种常见的灭火器材,主要分为沙石灭火弹和干粉灭火弹。目前市场上的灭火弹主要以干粉为主。超细干粉灭火剂是目前国内外已查明的灭火剂中,灭火浓度最低,灭火效能最高,灭火速度最快的一种,且灭火时不会造成火场中人员中毒或窒息死亡。在扑灭森林大火时,可以选用引燃式超细干粉灭火弹。根据内容回答下列问题:
(1)、常见灭火弹主要分为沙石灭火弹和。(2)、超细干粉灭火剂的特点有____(填字母)。A、灭火浓度最低 B、灭火效能最高 C、灭火速度最快 D、会造成人员伤亡(3)、某种干粉灭火剂的主要成分是NaHCO3 , 遇热时NaHCO3会分解生成Na2CO3、H2O和CO2气体,写出该反应的化学方程式:。(4)、“森林防火,人人有责”。请你对预防森林火灾提一条建设性意见:。三、实验探究题(共30分)
-
14. 兴趣小组的同学在实验室用“红磷燃烧前后质量的测定实验”对质量守恒定律进行验证,并展开了项目化学习的探究。
任务一:测定红磷燃烧前后的质量
小组同学利用如图所示实验装置测定红磷燃烧前后的质量关系。
 (1)、【小组讨论】
(1)、【小组讨论】红磷燃烧装置的总质量是g。
(2)、红磷燃烧的现象是 , 反应的化学方程式为。(3)、装置中小气球的作用是 , 整个实验过程中小气球的变化情况是。(4)、任务二:讨论上述实验与质量守恒定律的关系通过上述实验发现,红磷燃烧前后,天平始终平衡,同学们认为该实验验证了质量守恒定律。但是同学们进一步观察发现,锥形瓶底部仍有红磷剩余,于是小林同学提出了自己的观点:“红磷没有充分燃烧,所以不能验证质量守恒定律。”【小组交流】你同意小林的观点吗?(填“同意”或“不同意”),理由是。(5)、任务三:探究上述实验结束后的锥形瓶内氧气是否有剩余小组同学将实验结束后的锥形瓶取下,用凸透镜聚光照射剩余红磷,观察到红磷不燃烧。
【反思评价】该实验(填“能”或“不能”)说明锥形瓶内氧气没有剩余。15. 化学兴趣小组利用传感器和数据采集器测量模拟建筑火灾现场中氧气含量、二氧化碳浓度和温度的变化,研究火场逃生策略的合理性。如图1所示,在圆筒形透明塑料实验容器中底部三个点(K1、K2、K3)分别放置甲、乙、丙3根高低不同的蜡烛,如图2所示,在3根烛芯一定距离都依次放置氧气传感器(al、a2、a3)、温度传感器(b1、b2、b3)和二氧化碳传感器(c1、c2、c3)。点燃蜡烛后,盖上实验容器顶盖后,采集3根蜡烛火焰附近相关数据。
 (1)、实验获取3根蜡烛从开始燃烧到熄灭的时间如表1所示,并提取每根蜡烛熄灭时不同高度的含氧量如表2所示。
(1)、实验获取3根蜡烛从开始燃烧到熄灭的时间如表1所示,并提取每根蜡烛熄灭时不同高度的含氧量如表2所示。表1 3根蜡烛从开始燃烧到熄灭的时间
蜡烛
甲
乙
丙
时间/s
106
164
199
表2 熄灭时不同高度所测的含氧量
熄灭
时间/s
低处
(a3)/%
中处
(a2)/%
高处
(a1)/%
106
19.8
19.1
18.5
164
18.9
17.7
x
199
18.6
17.1
16.5
①三支蜡烛熄灭的先后顺序是。
②表2中,x可能是(填字母)。
A.18.6 B.17.9 C.17.2 D.16.1
③蜡烛熄灭时,含氧量均不为零。请据此对燃烧条件的表述做进一步的完善:。
④纵看表2数据,(填“低”“中”或“高”)处氧气含量下降最慢。
(2)、实验获取温度和二氧化碳浓度随时间变化曲线依次如图3和图4所示。

由此可知,点燃蜡烛后二氧化碳浓度由低处到高处逐渐变 , 原因是。
(3)、根据以上分析,发生建筑火灾时,人员应低下身子沿墙壁或贴近地面逃生,原因是。四、计算题(共12分)
-
16. 我国核工业技术世界领先,现已出口到西方发达国家。极硬的陶瓷材料碳化硼(B4C)可用作核反应堆的中子吸收剂,还可用于制造坦克装甲、防弹背心等。在电弧炉中用C与B2O3反应制得B4C,反应的化学方程式为2B2O3+7CB4C+6CO↑。按此反应,当消耗70千克B2O3时,可制得B4C多少千克?