天津市滨海新区2022-2023学年高一下学期期末检测化学试题
试卷更新日期:2023-09-27 类型:期末考试
一、单选题
-
1. 有利于实现“碳达峰、碳中和”的是( )A、粮食酿酒 B、石油裂化 C、燃煤脱硫 D、风能发电2. 下列有关化学品的说法正确的是( )A、阿司匹林有解热镇痛作用,是非处方药,可以长期服用 B、维生素C性质稳定不易被氧化,是水果罐头中常用的抗氧化剂 C、亚硝酸钠是一种常见防腐剂和护色剂,无毒性,对人体无害 D、硝酸铵是一种高效氮肥,但受热或经撞击易发生爆炸,必须作改性处理后施用3. 下列有关化学反应与能量的说法错误的是( )A、与的反应是吸热反应 B、镁条、碳酸氢钠与盐酸的反应都是放热反应 C、化学键的断裂与形成是化学反应中能量变化的主要原因 D、如果反应物的总能量高于生成物的总能量,发生反应时会向环境释放能量4. 利用金属的活泼性不同,冶炼铝、铁、银分别应采用的方法是( )A、电解法、热还原法、热分解法 B、热还原法、热分解法、电解法 C、热分解法、热还原法、电解法 D、电解法、热分解法、热还原法5. 下列有关化学电池的说法正确的是( )A、化学电池的反应基础是氧化还原反应 B、锌锰干电池工作时,锌筒作负极,发生还原反应 C、铅酸蓄电池属于二次电池,可以无限次的反复放电、充电 D、燃料电池是一种清洁、高效的新型电池,但是不安全6. 下列措施中,不能增大化学反应速率的是( )A、过氧化氢分解制取氧气时,添加少量氯化铁 B、碳与水蒸气反应生成水煤气时,用粉末状的碳代替块状的碳 C、钠与乙醇反应置换氢气时,增大乙醇的量 D、工业上合成氨时,将温度升高到500℃7. 下列有关煤、石油和天然气的说法错误的是( )A、煤的干馏为化学变化,石油的分馏为物理变化 B、“可燃冰”是天然气与水在高压、低温条件下形成的类冰状结晶物质 C、以煤或天然气为主要原料,均可以生产甲醇 D、通过石油裂化和裂解可以得到苯或甲苯等环状烃8. 下列有关氮的说法错误的是( )A、自然界中既有游离态的氮又有化合态的氮 B、氮的氧化物只有和 , 且均有毒 C、氮的固定是将氮气转化成含氮的化合物 D、含氮无机物和含氮有机物之间可相互转化9. 下列有关的说法正确的是( )A、有毒,不能用作食品添加剂 B、能使石蕊试液先变红后褪色 C、能使品红溶液褪色,加热后溶液又恢复红色 D、能使酸性溶液褪色,体现了的漂白性10. 下列有关无机非金属材料的说法正确的是( )A、石墨烯、碳化硅陶瓷等属于新型无机非金属材料 B、二氧化硅广泛用于制备芯片和太阳能电池 C、水泥、玻璃和水晶都是硅酸盐材料 D、现代信息社会用于传递信号的光纤的主要成分为硅11. 下列各组物质中属于同分异构体的是( )A、淀粉和纤维素 B、和 C、
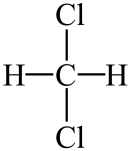 和
和 D、
D、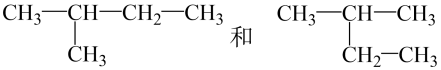 12. 下列事实可以用同一原理解释的是( )A、、均能使品红溶液褪色的实质 B、晶体、固体碘受热均能变成气体 C、S与铁、铜反应均生成低价硫化物 D、与、均不能在溶液中大量共存13. 一定温度下,可逆反应在体积固定的密闭容器中达到平衡状态的标志是( )A、单位时间内生成n mol的同时消耗2n mol B、用、表示的反应速率的比为的状态 C、混合气体的密度不再改变的状态 D、混合气体的压强不再改变的状态14. 在一定条件下,下列物质间的直接转化均能实现的是( )A、 B、 C、 D、15. 下列有关营养物质的说法正确的是( )A、葡萄糖能发生氧化反应和水解反应 B、油脂在碱性条件下水解生成甘油和高级脂肪酸 C、向盛有鸡蛋清溶液的试管中加入几滴醋酸铅溶液,无现象 D、淀粉和纤维素都能发生水解反应,最终生成葡萄糖16. 下列最符合绿色化学原子经济性反应要求的是( )A、乙烯与氯化氢反应制备一氯乙烷 B、甲烷与氯气反应制备一氯甲烷 C、将葡萄糖在酶的催化下转变为乙醇 D、氧化铜与稀硝酸反应制备硝酸铜17. 下列有关有机高分子材料的说法错误的是( )A、棉花、羊毛、蚕丝、麻和天然橡胶等属于天然有机高分子材料 B、聚乙烯塑料和聚氯乙烯塑料都可制成薄膜,用于食品、药物的内包装材料 C、线型结构的橡胶与硫作用可得到网状结构的硫化橡胶,该橡胶适合制造轮胎 D、合成纤维具有强度高、弹性好、耐磨、耐化学腐蚀、不易虫蛀等优良性能18. 既可以用来鉴别乙烷与乙烯,又可以用来除去乙烷中的乙烯以得到纯净乙烷的方法是( )A、通过足量的NaOH溶液 B、通过足量的溴水 C、在Ni催化、加热条件下通入H2 D、通过足量的酸性KMnO4溶液19. 下列有关硫酸和硝酸的说法正确的是( )A、浓硫酸和浓硝酸的混合物(体积比为)叫做王水 B、稀硫酸和稀硝酸均能与铁反应生成有毒气体 C、浓硫酸和浓硝酸均能与炽热的木炭反应 D、常温下浓硫酸和浓硝酸都不能用铝制容器盛放20. 实验室制取NH3时,下列装置能达到相应实验目的的是( )
12. 下列事实可以用同一原理解释的是( )A、、均能使品红溶液褪色的实质 B、晶体、固体碘受热均能变成气体 C、S与铁、铜反应均生成低价硫化物 D、与、均不能在溶液中大量共存13. 一定温度下,可逆反应在体积固定的密闭容器中达到平衡状态的标志是( )A、单位时间内生成n mol的同时消耗2n mol B、用、表示的反应速率的比为的状态 C、混合气体的密度不再改变的状态 D、混合气体的压强不再改变的状态14. 在一定条件下,下列物质间的直接转化均能实现的是( )A、 B、 C、 D、15. 下列有关营养物质的说法正确的是( )A、葡萄糖能发生氧化反应和水解反应 B、油脂在碱性条件下水解生成甘油和高级脂肪酸 C、向盛有鸡蛋清溶液的试管中加入几滴醋酸铅溶液,无现象 D、淀粉和纤维素都能发生水解反应,最终生成葡萄糖16. 下列最符合绿色化学原子经济性反应要求的是( )A、乙烯与氯化氢反应制备一氯乙烷 B、甲烷与氯气反应制备一氯甲烷 C、将葡萄糖在酶的催化下转变为乙醇 D、氧化铜与稀硝酸反应制备硝酸铜17. 下列有关有机高分子材料的说法错误的是( )A、棉花、羊毛、蚕丝、麻和天然橡胶等属于天然有机高分子材料 B、聚乙烯塑料和聚氯乙烯塑料都可制成薄膜,用于食品、药物的内包装材料 C、线型结构的橡胶与硫作用可得到网状结构的硫化橡胶,该橡胶适合制造轮胎 D、合成纤维具有强度高、弹性好、耐磨、耐化学腐蚀、不易虫蛀等优良性能18. 既可以用来鉴别乙烷与乙烯,又可以用来除去乙烷中的乙烯以得到纯净乙烷的方法是( )A、通过足量的NaOH溶液 B、通过足量的溴水 C、在Ni催化、加热条件下通入H2 D、通过足量的酸性KMnO4溶液19. 下列有关硫酸和硝酸的说法正确的是( )A、浓硫酸和浓硝酸的混合物(体积比为)叫做王水 B、稀硫酸和稀硝酸均能与铁反应生成有毒气体 C、浓硫酸和浓硝酸均能与炽热的木炭反应 D、常温下浓硫酸和浓硝酸都不能用铝制容器盛放20. 实验室制取NH3时,下列装置能达到相应实验目的的是( )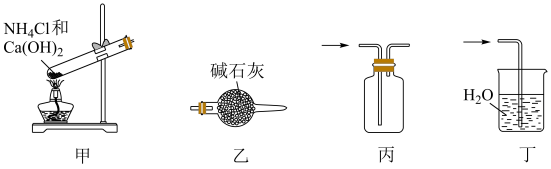 A、装置甲生成NH3 B、装置乙干燥NH3 C、装置丙收集NH3 D、装置丁吸收多余NH321. 下列方程式与所给事实不相符的是( )A、使溴水褪色: B、将分别蘸有浓盐酸和浓氨水的玻璃棒靠近时产生白烟: C、与反应,体现了的氧化性: D、工业上用焦炭还原石英砂可制的粗硅:22. 某有机物的结构简式为
A、装置甲生成NH3 B、装置乙干燥NH3 C、装置丙收集NH3 D、装置丁吸收多余NH321. 下列方程式与所给事实不相符的是( )A、使溴水褪色: B、将分别蘸有浓盐酸和浓氨水的玻璃棒靠近时产生白烟: C、与反应,体现了的氧化性: D、工业上用焦炭还原石英砂可制的粗硅:22. 某有机物的结构简式为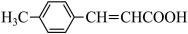 ,下列说法正确的是( ) A、该有机物的分子式为 B、该有机物属于不饱和烃 C、该有机物分子中有三种官能团 D、该有机物分子中所有原子不可能共面23. 下列有关环境保护的说法错误的是( )A、化石燃料燃烧产生的CO、、等属于次生污染物 B、污水的一级处理通常采用物理方法,除去污水中不溶解的污染物 C、含氮、磷化合物的生活污水大量排放可使水体富营养化 D、废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染24. 为精制食盐,需除去粗盐水中的、和 , 下列说法错误的是( )
,下列说法正确的是( ) A、该有机物的分子式为 B、该有机物属于不饱和烃 C、该有机物分子中有三种官能团 D、该有机物分子中所有原子不可能共面23. 下列有关环境保护的说法错误的是( )A、化石燃料燃烧产生的CO、、等属于次生污染物 B、污水的一级处理通常采用物理方法,除去污水中不溶解的污染物 C、含氮、磷化合物的生活污水大量排放可使水体富营养化 D、废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染24. 为精制食盐,需除去粗盐水中的、和 , 下列说法错误的是( ) A、①、②、③依次加入的试剂可以是过量的NaOH、、溶液 B、取滤液a,加入溶液,若有白色沉淀产生,则说明没有除尽 C、滤液a中加入稀盐酸初期,溶液中无明显现象,后期则会生成无色气体 D、用蒸发的方法从溶液中得到固体时,不能将溶液蒸干后再停止加热25. 根据下列实验操作和现象所得出的结论正确的是( )
A、①、②、③依次加入的试剂可以是过量的NaOH、、溶液 B、取滤液a,加入溶液,若有白色沉淀产生,则说明没有除尽 C、滤液a中加入稀盐酸初期,溶液中无明显现象,后期则会生成无色气体 D、用蒸发的方法从溶液中得到固体时,不能将溶液蒸干后再停止加热25. 根据下列实验操作和现象所得出的结论正确的是( )选项
实验操作和现象
结论
A
向某溶液中加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失。
原溶液中一定有
B
在试管中加入0.5g淀粉和4mL 2mol/L溶液,加热。待溶液冷却后,再加入少量碘水,溶液变蓝。
淀粉未发生水解
C
足量的铜片与一定量稀充分反应后,铜片剩余,再加入适量稀 , 铜片继续溶解。
Cu可以与稀反应
D
向某溶液中加入氢氧化钠溶液并加热,将湿润的红色石蕊试纸置于试管口,试纸变蓝。
原溶液中一定有
A、A B、B C、C D、D26. 乙醇、乙酸分子中的各种化学键如图所示,下列反应中断键的位置正确的是( )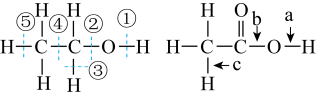 A、乙醇与金属钠发生置换反应,断裂①③⑤键 B、乙醇与乙酸发生酯化反应,断裂②键、a键 C、乙醇在铜催化共热下与反应,断裂①③键 D、乙酸与氢氧化钠溶液发生中和反应,断裂b键27. 把A、B、C、D四块金属片浸入稀硫酸中,分别用导线两两相连可以组成原电池。A、B相连时A为负极;C、D相连时,电流由D→C;A、C相连时,C极上产生大量气泡;B、D相连时,D极发生氧化反应。这四种金属的活动性顺序是( )A、A>B>C>D B、A>C>D>B C、C>A>B>D D、A>B>D>C28. 三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下列说法正确的是( )
A、乙醇与金属钠发生置换反应,断裂①③⑤键 B、乙醇与乙酸发生酯化反应,断裂②键、a键 C、乙醇在铜催化共热下与反应,断裂①③键 D、乙酸与氢氧化钠溶液发生中和反应,断裂b键27. 把A、B、C、D四块金属片浸入稀硫酸中,分别用导线两两相连可以组成原电池。A、B相连时A为负极;C、D相连时,电流由D→C;A、C相连时,C极上产生大量气泡;B、D相连时,D极发生氧化反应。这四种金属的活动性顺序是( )A、A>B>C>D B、A>C>D>B C、C>A>B>D D、A>B>D>C28. 三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下列说法正确的是( )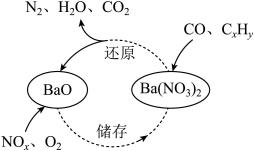 A、转化过程中,化合价发生变化的元素有C、N、O B、和是转化过程中的中间产物 C、还原过程中当生成0.1mol时,转移电子的物质的量为0.5mol D、汽车尾气中、被转化为排放到空气中会形成酸雨29. 一定温度下,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。下列说法正确的是( )
A、转化过程中,化合价发生变化的元素有C、N、O B、和是转化过程中的中间产物 C、还原过程中当生成0.1mol时,转移电子的物质的量为0.5mol D、汽车尾气中、被转化为排放到空气中会形成酸雨29. 一定温度下,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。下列说法正确的是( )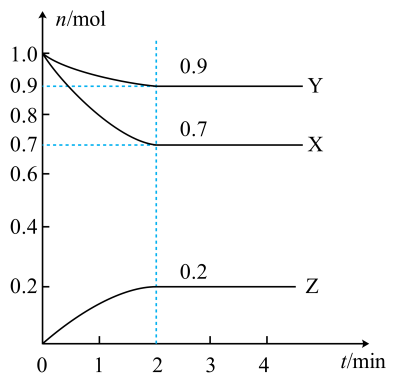 A、该反应的化学方程式为 B、0~2min时间段内,用物质X表示的反应速率为 C、反应物平衡时的转化率 D、恒温恒容下,充入Ar,能使反应速率增大30. 有一稀硫酸和稀硝酸的混合酸,其中和的物质的量浓度分别是4mol/L和2mol/L。取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,生成气体的总物质的量为(设反应中被还原成)( )A、0.045mol B、0.03mol C、0.02mol D、0.005mol
A、该反应的化学方程式为 B、0~2min时间段内,用物质X表示的反应速率为 C、反应物平衡时的转化率 D、恒温恒容下,充入Ar,能使反应速率增大30. 有一稀硫酸和稀硝酸的混合酸,其中和的物质的量浓度分别是4mol/L和2mol/L。取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,生成气体的总物质的量为(设反应中被还原成)( )A、0.045mol B、0.03mol C、0.02mol D、0.005mol二、有机推断题
-
31. 现有K、M、N三种烃,其球棍模型如图所示,请回答下列问题。
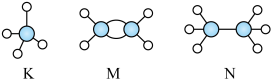 (1)、三种烃中互为同系物的是(填对应字母,下同)(2)、等质量的三种烃完全燃烧时消耗最多的是 , 生成最多的是。(3)、1mol K与发生取代反应,待反应完成后测得4种取代物物质的量相等,则消耗的物质的量为。(4)、以M为基本原料可以合成多种有机物,合成路线如下:
(1)、三种烃中互为同系物的是(填对应字母,下同)(2)、等质量的三种烃完全燃烧时消耗最多的是 , 生成最多的是。(3)、1mol K与发生取代反应,待反应完成后测得4种取代物物质的量相等,则消耗的物质的量为。(4)、以M为基本原料可以合成多种有机物,合成路线如下:
已知:(R代表烃基,X代表卤素原子)
①A与CuO在加热条件下反应的化学方程式为 , 反应类型为。
②B与D以物质的量之比生成E的化学方程式为 , 反应类型为。
三、填空题
-
32. 反应的能量变化趋势如图甲所示。
 (1)、该反应为(填“吸热”或“放热”)反应。(2)、若将上述反应设计成原电池,铜为原电池某一极材料,则铜为(填“正”或“负”)极。铜片上产生的现象为 , 该极的电极反应式为。(3)、某学生为了探究锌与硫酸反应过程中的速率变化,将表面被氧化的锌粒投入稀硫酸中,测得生成氢气的速率与反应时间t关系曲线如图乙所示。
(1)、该反应为(填“吸热”或“放热”)反应。(2)、若将上述反应设计成原电池,铜为原电池某一极材料,则铜为(填“正”或“负”)极。铜片上产生的现象为 , 该极的电极反应式为。(3)、某学生为了探究锌与硫酸反应过程中的速率变化,将表面被氧化的锌粒投入稀硫酸中,测得生成氢气的速率与反应时间t关系曲线如图乙所示。
①曲线0~a段,反应的离子方程是为。
②曲线b~c段,产生氢气的速率增加较快的主要原因是。
③曲线由c以后,产生氢气的速率逐渐下降的主要原因是。
四、实验题
-
33. 研究氮、硫及其化合物对工业生产、资源利用和环境保护都具有重要意义。(1)、实验室制备、收集干燥的 , 所需装置如图Ⅰ所示。

①装置A中反应的化学方程式为。
②请按气流方向连接各仪器接口,顺序为a→→→→→f。
③装置D的作用是 , 装置E中反应的离子方程式为。
(2)、为了有效实现和的相互转化,设计如下实验:按图Ⅱ组装好实验装置,并检查装置的气密性,实验前用排水法收集半瓶气体。
图II
①打开弹簧夹,推动针筒活塞,使进入烧瓶。关上弹簧夹,首先观察到烧瓶中的现象为 , 产生此现象的化学方程式为。
②轻轻摇动烧瓶,观察到烧瓶中的现象为 , 产生此现象的化学方程式为。
(3)、在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系:
当X是强酸时, A、B、C、D、E均含同种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。
①A是。(填化学式)
②当X是强碱时,B生成C的化学方程为。
-
-