山东省青岛市2022-2023学年高一下学期期末考试化学试题
试卷更新日期:2023-09-27 类型:期末考试
一、单选题
-
1. 党的二十大报告对“传承中华优秀传统文化”提出了明确要求。中华优秀传统文化中蕴藏着诸多化学知识,下列诗句相关说法错误的是( )A、“采桑作蚕丝”中的蚕丝属于蛋白质,可通过灼烧鉴别真伪 B、“杨花榆荚无才思”中的榆荚又称榆钱,主要有机成分是纤维素 C、“蜂蜜酿成花已飞”中的蜂蜜含有果糖和葡萄糖,二者互为同分异构体 D、“蜡炬成灰泪始干”中的蜡主要成分为高级脂肪酸酯,属于高分子化合物2. 蔡斯盐是最早发现的配合物,将乙烯气体通入溶液中,在氮化亚锡催化作用下即可制得。下列说法错误的是( )A、电负性: B、的电子式为
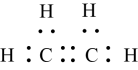 C、与互为同位素
D、蔡斯盐中化合价为+2
3. 下列关于烃及其衍生物的说法正确的是( )A、甲烷、苯、葡萄糖均不能使酸性高锰酸钾溶液褪色 B、与组成上相差1个 , 一定互为同系物 C、石油的裂化、石油的分馏与煤的干馏均属于化学变化 D、乙醇是优良的有机溶剂,可用于提取某些中药的有效成分4. 某学者绘制了一种八角星元素周期表,每个八角星代表一个周期(第1周期除外),八角星的每个顶角对应一种元素。为原子序数依次增大的五种短周期主族元素,基态原子核外电子占据3个能级且成对电子数是末成对电子数的3倍。下列说法错洖的是( )
C、与互为同位素
D、蔡斯盐中化合价为+2
3. 下列关于烃及其衍生物的说法正确的是( )A、甲烷、苯、葡萄糖均不能使酸性高锰酸钾溶液褪色 B、与组成上相差1个 , 一定互为同系物 C、石油的裂化、石油的分馏与煤的干馏均属于化学变化 D、乙醇是优良的有机溶剂,可用于提取某些中药的有效成分4. 某学者绘制了一种八角星元素周期表,每个八角星代表一个周期(第1周期除外),八角星的每个顶角对应一种元素。为原子序数依次增大的五种短周期主族元素,基态原子核外电子占据3个能级且成对电子数是末成对电子数的3倍。下列说法错洖的是( )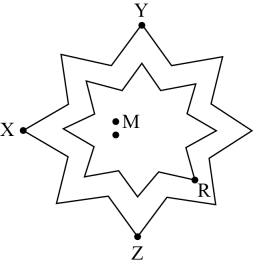 A、三种元素形成的化合物一定是离子化合物 B、分别与形成的最简单化合物的沸点: C、最高价氧化物的水化物之间均能两两反应 D、形成的两种常见化合物阴阳离子个数比均为5. 利用下列实验装置进行实验,能达到实验目的的是( )
A、三种元素形成的化合物一定是离子化合物 B、分别与形成的最简单化合物的沸点: C、最高价氧化物的水化物之间均能两两反应 D、形成的两种常见化合物阴阳离子个数比均为5. 利用下列实验装置进行实验,能达到实验目的的是( ) A、用装置①验证乙醇消去反应生成乙烯 B、用装置②制备少量乙酸乙酯 C、用装置③验证石蜡分解产生不饱和烃 D、用装畳④鉴别邻二甲苯与环己烯6. 富硒食品指富含饭量元素硒的食品,具有延缓衰老、抗癌、增强免疫力等作用。下列说法错误的是( )A、硒原子结构示意图为
A、用装置①验证乙醇消去反应生成乙烯 B、用装置②制备少量乙酸乙酯 C、用装置③验证石蜡分解产生不饱和烃 D、用装畳④鉴别邻二甲苯与环己烯6. 富硒食品指富含饭量元素硒的食品,具有延缓衰老、抗癌、增强免疫力等作用。下列说法错误的是( )A、硒原子结构示意图为 B、硒元素最高正价与最低负价代数和为4
C、依据元素周期律推测硒化氢的熔沸点及热稳定性均高于硫化氢
D、硒元素位于金属与非金属分界线附近推测硒可用作半导体材料
7. 乳酸亚铁是一种治疗贫血的药物,可由乳酸与铁粉制得,发生反应的化学方程式如下:2CH3CH(OH)COOH+Fe[CH3CH(OH)COO]2Fe+H2↑。下列说法错误的是( )A、乳酸在一定条件下可生成六元环酯 B、乳酸与乳酸亚铁均具有良好的水溶性 C、乳酸通过聚合反应生成的高分子化合物具有可降解性 D、乳酸与足量或反应均产生气体8. 氨硼烷()是一种高性能固体储氢材料,在催化剂作用下可发生如下反应:。已知结构如图所示,下列说法正确的是( )
B、硒元素最高正价与最低负价代数和为4
C、依据元素周期律推测硒化氢的熔沸点及热稳定性均高于硫化氢
D、硒元素位于金属与非金属分界线附近推测硒可用作半导体材料
7. 乳酸亚铁是一种治疗贫血的药物,可由乳酸与铁粉制得,发生反应的化学方程式如下:2CH3CH(OH)COOH+Fe[CH3CH(OH)COO]2Fe+H2↑。下列说法错误的是( )A、乳酸在一定条件下可生成六元环酯 B、乳酸与乳酸亚铁均具有良好的水溶性 C、乳酸通过聚合反应生成的高分子化合物具有可降解性 D、乳酸与足量或反应均产生气体8. 氨硼烷()是一种高性能固体储氢材料,在催化剂作用下可发生如下反应:。已知结构如图所示,下列说法正确的是( )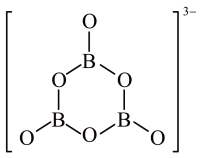 A、与具有相似的空间构型 B、中的“·”表示的作用力为氢键 C、中各原子均满足最外层稳定结构 D、反应前后,B原子的杂化方式未发生改变9. 实验室模拟工业海带提砷的流程如图。下列说法错误的是( )
A、与具有相似的空间构型 B、中的“·”表示的作用力为氢键 C、中各原子均满足最外层稳定结构 D、反应前后,B原子的杂化方式未发生改变9. 实验室模拟工业海带提砷的流程如图。下列说法错误的是( )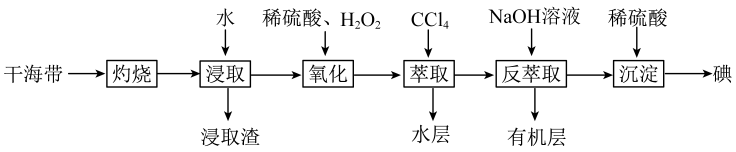 A、“灼烧”用到的硅酸盐仪器有坩埚、泥三角、玻璃棒、酒精灯 B、“氧化”时发生反应的离子方程式为 C、“反萃取”所得有机层经处理后可循环再利用 D、“沉淀”时每生成碘,理论上转移电子10. 在碱性溶液中,双缩脲能与作用形成紫红色配合物,配离子结构如图所示。下列说法错误的是( )
A、“灼烧”用到的硅酸盐仪器有坩埚、泥三角、玻璃棒、酒精灯 B、“氧化”时发生反应的离子方程式为 C、“反萃取”所得有机层经处理后可循环再利用 D、“沉淀”时每生成碘,理论上转移电子10. 在碱性溶液中,双缩脲能与作用形成紫红色配合物,配离子结构如图所示。下列说法错误的是( )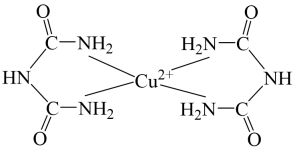 A、双缩脲分子中键与键个数比为 B、该配离子与水形成氢键的原子只有 C、该配离子中提供空轨道的微粒是 D、基态原子电子占据最高能级的电子云轮廓图为球形11. 邻苯二甲酸二甲酯可用于驱蚊剂,结构如图。下列说法错误的是( )
A、双缩脲分子中键与键个数比为 B、该配离子与水形成氢键的原子只有 C、该配离子中提供空轨道的微粒是 D、基态原子电子占据最高能级的电子云轮廓图为球形11. 邻苯二甲酸二甲酯可用于驱蚊剂,结构如图。下列说法错误的是( ) A、的分子式为 , B、能发生水解、加成和氧化反应 C、在一定条件下最多能与加成 D、中所有的原子可能处于同一平面内12. 下列实验操作能达到实验目的的是( )
A、的分子式为 , B、能发生水解、加成和氧化反应 C、在一定条件下最多能与加成 D、中所有的原子可能处于同一平面内12. 下列实验操作能达到实验目的的是( )选项
实验目的
实验操作
A
除去乙烷中的乙烯
将气体通过盛有酸性溶液的洗气瓶
B
证明能与形成配位键的是而不是
向盛有溶液的两支试管中,分别逐滴滴加氨水和溶液至过量
C
比较得电子能力:
将足量硝酸滴入到溶液中,产生的气体通入溶液中
D
探究乙醇在铜丝作用下发生催化氧化
取一根洁净、红亮的铜丝,前端绕成螺旋状,置于酒精灯外焰灼烧,然后慢慢移向内焰,迅速取出
A、A B、B C、C D、D13. 关于微粒间的相互作用的说法错误的是( )A、羊毛织品水洗变形与蛋白分子结构中的氢键有关 B、水的熔沸点高于甲烷是键能大于键能的缘故 C、金属的导电性和导热性都是通过自由电子的定向运动实现的 D、加热法分离和的过程中破坏了离子键和共价键14. 有学者提出,在铜基催化剂作用下,合成甲醇的转化过程如图所示。下列说法证确的是( )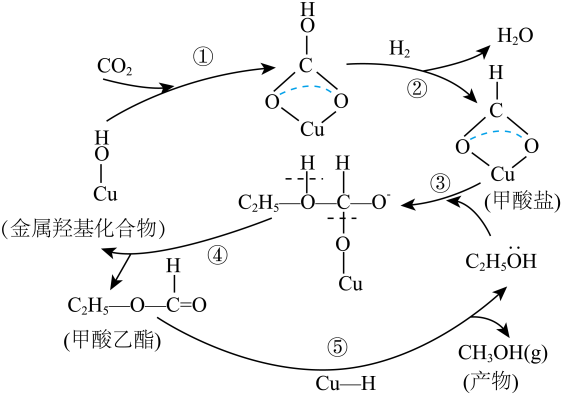 A、转化过程中碳原子有3种杂化方式 B、和均是由极性键构成的极性分子 C、能与溶液反应的甲酸乙酯的同分异构体分有1种 D、该过程的总反应方程式为15. 曲酸主要用作美白剂、食品添加剂等,其与脱氧曲酸的结构如图所示。下列说法正确的是( )
A、转化过程中碳原子有3种杂化方式 B、和均是由极性键构成的极性分子 C、能与溶液反应的甲酸乙酯的同分异构体分有1种 D、该过程的总反应方程式为15. 曲酸主要用作美白剂、食品添加剂等,其与脱氧曲酸的结构如图所示。下列说法正确的是( )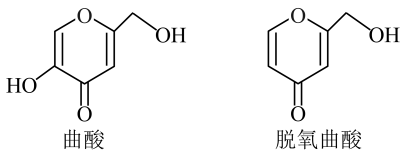 A、曲酸与脱氧曲酸均含有4种官能团 B、曲酸发生消去反应即可生成脱氧曲酸 C、与曲酸分子式相同且仅含羟基的芳香族化合物有3种 D、脱氧曲酸能与酸性溶液、溴水及溶液等反应
A、曲酸与脱氧曲酸均含有4种官能团 B、曲酸发生消去反应即可生成脱氧曲酸 C、与曲酸分子式相同且仅含羟基的芳香族化合物有3种 D、脱氧曲酸能与酸性溶液、溴水及溶液等反应二、元素或物质推断题
-
16. X、Y、Z、M、W是原子序数依次增大的前20号主族元素,且原子序数和为46。在周期表中原子半径最小;基态原子㤥外电子占据3个能级,且各能级电子数相同;第一电离能小于同周期相邻元素;焰色呈黄色。回答下列问题:(1)、化合物是一种无机盐,电子式为;已知MX遇水剧烈反应,所得溶液呈强碱性,则该反应的化学方程式为。(2)、Z、M、W简单离子半径由大到小的顺序为(用离子符号表示)。(3)、在相同温度与压强下,形成的某气态化合物与的密度之比为 , 则该化合物的分子式为 , 其结构有种。(4)、是一种白色晶体,难溶于水。该化合物受热分解过程中,热重分析测得剩余固体质量占初始固体质量的百分含量随温度变化的曲线如图所示。

①温度由升至过程中,发生反应的化学方程式为。
②点所得固体的化学式为。
三、实验题
-
17. 丁酸甲酯常用作香料,主要用于配制牛奶、干酪、苹果等型香精。实验室以丁酸和甲醇为原料制备丁酸甲酯的装置如图所示。
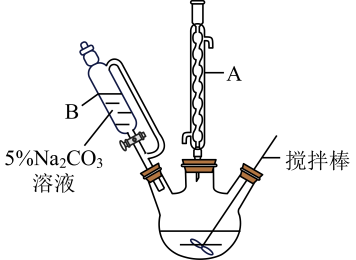
实验步骤:
Ⅰ.将丁酸和甲醇加入到三颈烧瓶中,再加入浓硫酸,混合均匀。
Ⅱ.加热三颈烧瓶,控制温度为 , 搅拌3—8h,充分反应。
Ⅲ.冷却,向混合液中加入溶液洗至中性。
Ⅳ.分液,取上层油状液体,加入无水固体,过滤后蒸馏,收集102~105℃馏分。
已知:几种物质的性质见下表
沸点
溶解性
性质
丁酸
163.5
与水互溶,易溶于有机溶剂
低毒
甲醇
64.7
与水互溶,易溶于有机溶剂
易挥发,有毒
丁酸甲酯
103
微溶于水,易溶于有机溶剂
易挥发
回答下列问题:
(1)、制备丁酸甲酯发生反应的化学方程式为;丁酸甲酯的同分异构体中属于酯类的还有种。(2)、仪器的作用是 , 仪器B的名称是(3)、步骤Ⅰ中加入浓硫酸的操作是;步骤Ⅱ中采用的加热方法是。(4)、步骤Ⅲ中混合液用溶液洗涤的目的是。(5)、步骤Ⅳ中加入无水固体的作用是;蒸馏用到的玻璃仪器主要有蒸馏烧瓶、酒棈灯、牛角管、锥形瓶、、。四、结构与性质
-
18. 过渡元素钒、锰、铁、镍等在生活、科研中应用广泛。回答下列问题:(1)、钒广泛应用于航天、化工及能源等行业,与钒同周期且基态原子未成对电子数相同的元素可能位于周期表区。(2)、与水杨醛缩邻氨基苯酚可形成黄色配合物,应用于科研光度法测定离子浓度。锰在元素周期表中的位置是。已知与其同分异构体的结构如图1所示,沸点较高的是(填标号),原因是。
 (3)、铁是构成血红蛋白的必要成分,血红蛋白携氧后的配合物结构如图2所示(部分氢末画出)。中心的配位数为 , 与血红蛋白中的配位能力(填“强于”或“弱于”) , 原因是。(4)、砷化镍激光在医学上用于治疗皮肤及黏膜创面的感染及溃疡等,人工合成的砷化镍常存在各种缺陷,已知某缺陷砷化镍的组成为 , 其中元数只有+2和+3两种价态,则为
(3)、铁是构成血红蛋白的必要成分,血红蛋白携氧后的配合物结构如图2所示(部分氢末画出)。中心的配位数为 , 与血红蛋白中的配位能力(填“强于”或“弱于”) , 原因是。(4)、砷化镍激光在医学上用于治疗皮肤及黏膜创面的感染及溃疡等,人工合成的砷化镍常存在各种缺陷,已知某缺陷砷化镍的组成为 , 其中元数只有+2和+3两种价态,则为五、有机推断题
-
19. 有机物是一种药物中间体,其一种合成路线如图所示:
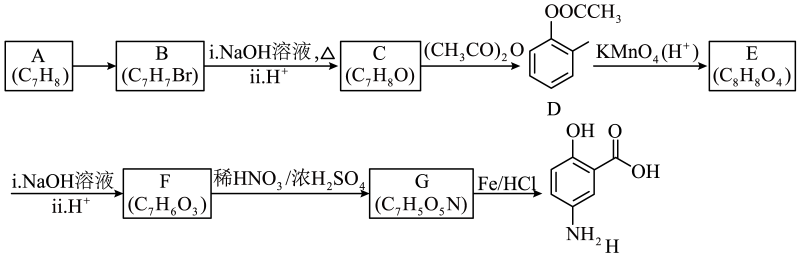
已知:① ② —烃基,—卤原子
回答下列问题:
(1)、的名称为;反应的试剂为。(2)、的反应类型为;E含有的官能团名称为。(3)、反应的化学方程式为。(4)、同时满足下列条件的D的同分异构体有种(不考虑立体异构);其中苯环上的一氮代物只有2种的同分异构体的结构简式为。①含有苯环;
②能使新制转化为砖红色沉淀
③能发生水解反应,且水解产物中苯环只与碳原子成健
六、结构与性质
-
20. 近年来,我国以风电、光伏发电为代表的新能源发展成效显著,推动了绿色生态文明的建设。回答下列问题:(1)、光伏发电的传统材料是硅,基态硅原子核外电子有种空间运动状态,与硅同主族的第四周期元素基态原子的价层电子排布式为。(2)、与N—甲基咪唑
 反应可以得到 , 其结构如图1所示。
反应可以得到 , 其结构如图1所示。

图1
①已知—甲基咪唑分子具有类似苯环的结构,则该分子中存在的大健应表示为 , 连甲基的原子的价层孤电子对占据轨道。
②每个含有个键;除键外,中还存在的化学键有(填标号)。
A.极性键 B.非极性键 C.离子键 D.范德华力 E.配位键
(3)、武汉大学闵杰课题组研究出一种小分子有机光伏材料,结构如图2所示。
①该分子中属于第二周期的非金属元素第三电离能由大到小的顺序为(用元素符号表示)。
②是微电子工业中一种优良的等离子蚀刻气体,其分子空间构型与相似,键角(填“大于”“等于”或“小于”),原因是。
-
-
-
-