鲁教版(五四制)初中化学2023-2024学年九年级上学期第三单元 海水中的化学素养检测
试卷更新日期:2023-09-26 类型:单元试卷
一、选择题(每小题3分,共30分)
-
1. 下列盐的用途中,错误的是( )A、碳酸钠用于除水垢 B、用碳酸钙作补钙剂 C、用氯化钠配制生理盐水 D、用碳酸氢钠作焙制糕点的发酵粉2. 海洋是生命的摇篮,是巨大的资源宝库。下列有关海洋的叙述不正确的是( )A、海洋中含有丰富的矿物、生物、动力资源等 B、海水中含量最多的物质是氯化钠 C、海底开采出的可燃冰被科学家誉为“未来能源” D、海洋资源开发过程中,应注重保护海洋环境3. 海洋是人类宝贵的自然资源。下列说法错误的是( )A、海水淡化——利用物质的溶解度不同进行蒸馏分离 B、海水晒盐——利用太阳能和风能蒸发水分得到粗盐 C、海水制镁——利用碱将镁元素富集,提纯后电解 D、海水“制碱”——利用氨碱法以食盐等为原料制取纯碱4. 在除去粗盐中的难溶性杂质实验中,下列有关装置和操作正确的是( )A、溶解粗盐
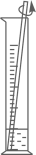 B、过滤粗盐水
B、过滤粗盐水 C、蒸发结晶
C、蒸发结晶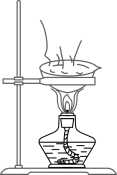 D、趁热取下蒸发皿
D、趁热取下蒸发皿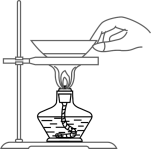 5. 下列关于纯碱的说法正确的是( )A、用pH试纸测出纯碱溶液的pH为7 B、纯碱中含有少量的小苏打可以用稀盐酸除去 C、侯氏制碱法中的“碱”指的是氢氧化钠 D、纯碱溶液可以跟含Ca2+的溶液发生复分解反应6. 已知元素化合价发生变化的反应是氧化还原反应,其中被还原的元素化合价降低,被氧化的元素化合价升高。海洋中有丰富的资源,如图所示利用海水可获得许多化工产品。下列有关说法正确的是( )
5. 下列关于纯碱的说法正确的是( )A、用pH试纸测出纯碱溶液的pH为7 B、纯碱中含有少量的小苏打可以用稀盐酸除去 C、侯氏制碱法中的“碱”指的是氢氧化钠 D、纯碱溶液可以跟含Ca2+的溶液发生复分解反应6. 已知元素化合价发生变化的反应是氧化还原反应,其中被还原的元素化合价降低,被氧化的元素化合价升高。海洋中有丰富的资源,如图所示利用海水可获得许多化工产品。下列有关说法正确的是( ) A、过程①中除去粗盐中的S、Ca2+、Mg2+等杂质,加入的试剂顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液,过滤后加盐酸 B、过程②中加入的试剂为CaCl2溶液 C、海水可通过蒸发结晶获得粗盐和母液,且母液一定是氯化钠的饱和溶液 D、在过程④中溴元素被还原7. 在密闭反应体系内加热碳酸氢钠溶液,利用数字化仪器测量碳酸氢钠分解产生的二氧化碳的体积分数随温度变化的曲线如图所示。下列说法正确的是( )
A、过程①中除去粗盐中的S、Ca2+、Mg2+等杂质,加入的试剂顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液,过滤后加盐酸 B、过程②中加入的试剂为CaCl2溶液 C、海水可通过蒸发结晶获得粗盐和母液,且母液一定是氯化钠的饱和溶液 D、在过程④中溴元素被还原7. 在密闭反应体系内加热碳酸氢钠溶液,利用数字化仪器测量碳酸氢钠分解产生的二氧化碳的体积分数随温度变化的曲线如图所示。下列说法正确的是( )
 A、40 ℃~50 ℃之间的某一温度时碳酸氢钠开始分解 B、随着温度的升高,二氧化碳的体积分数一直增大 C、使碳酸氢钠从其溶液中析出应用加热蒸发的方法 D、温度升高,溶液中钠元素和碳元素质量始终不变8. 在化学知识中有许多规律,下列具体物质的性质符合对应规律的是( )A、某些固体物质溶于水时会使水的温度降低,例如:硝酸铵和氢氧化钠 B、一般固体物质的溶解度随温度的升高而增大,例如:硝酸钾和氢氧化钙 C、某些非金属氧化物能和碱溶液反应生成盐和水,例如:二氧化碳和二氧化硫 D、某些盐的水溶液显碱性,能使酚酞试液变红,例如:碳酸钠和氯化钠9. 查阅资料得知:在复分解反应中,酸性强的物质可以反应生成酸性弱的物质。已知酸性强弱:HCl>H2SO3>CH3COOH>H2CO3>HClO。下列反应能发生且化学方程式书写正确的是( )A、HClO+CH3COONa= NaClO+CH3COOH B、H2SO3+2NaHCO3= Na2SO4+CO2↑+H2O C、2CH3COOH+K2CO3= 2CH3COOK+CO2↑+H2O D、BaCl2+CO2+H2O= BaCO3↓+2HCl10. 为了达到实验目的,下列方案或结论正确的是( )
A、40 ℃~50 ℃之间的某一温度时碳酸氢钠开始分解 B、随着温度的升高,二氧化碳的体积分数一直增大 C、使碳酸氢钠从其溶液中析出应用加热蒸发的方法 D、温度升高,溶液中钠元素和碳元素质量始终不变8. 在化学知识中有许多规律,下列具体物质的性质符合对应规律的是( )A、某些固体物质溶于水时会使水的温度降低,例如:硝酸铵和氢氧化钠 B、一般固体物质的溶解度随温度的升高而增大,例如:硝酸钾和氢氧化钙 C、某些非金属氧化物能和碱溶液反应生成盐和水,例如:二氧化碳和二氧化硫 D、某些盐的水溶液显碱性,能使酚酞试液变红,例如:碳酸钠和氯化钠9. 查阅资料得知:在复分解反应中,酸性强的物质可以反应生成酸性弱的物质。已知酸性强弱:HCl>H2SO3>CH3COOH>H2CO3>HClO。下列反应能发生且化学方程式书写正确的是( )A、HClO+CH3COONa= NaClO+CH3COOH B、H2SO3+2NaHCO3= Na2SO4+CO2↑+H2O C、2CH3COOH+K2CO3= 2CH3COOK+CO2↑+H2O D、BaCl2+CO2+H2O= BaCO3↓+2HCl10. 为了达到实验目的,下列方案或结论正确的是( )选项
实验目的
实验方案或结论
A
鉴别碳粉、铁粉和氧化铁粉末
取样后,分别加入稀盐酸
B
除去KOH溶液中的K2CO3
加入足量的稀盐酸,蒸发
C
除去生石灰中的碳酸钙
加入足量盐酸,过滤
D
鉴别某溶液中是否含有S
取少量溶液于试管中,滴加BaCl2溶液,有白色沉淀生成,则该溶液中一定有S
A、A B、B C、C D、D二、填空及简答题(共44分)
-
11. 酷爱化学和卡通的小玉同学在学习碳酸钠时,发现碳酸钠“神通广大”,它竟然与酸碱指示剂、酸、碱、盐都反应,画出的卡通图如图所示。

【温馨提示】氯化钡溶液呈中性。
(1)、碳酸钠的俗名是(写一种)。(2)、写出用碳酸钠制取少量氢氧化钠的化学方程式:。(3)、向滴有酚酞的碳酸钠溶液中逐滴加入氯化钡溶液,直至反应完全,可以观察到的现象为 , 写出该反应的化学方程式:。(4)、若氯化钠中混有少量的碳酸钠,小玉同学选择了一种酸将碳酸钠除去,她选的酸是。12. 我国有漫长的海岸线,海洋蕴藏着丰富的资源。请按要求填空。(1)、南海蕴藏着大量的可燃冰。可燃冰(主要成分是CH4)被科学家誉为“未来能源”,CH4完全燃烧的化学方程式是。(2)、目前能规模化和产业化淡化海水的方法主要是。(3)、从海水中得到金属镁。用苦卤制取金属镁的流程图如图1所示:
①步骤Ⅰ发生反应的化学方程式为。
②验证苦卤中MgCl2已完全转化为Mg(OH)2沉淀的方法是。
(4)、海水制碱流程如图2所示:
①该厂最终产品是(填物质化学式)。
②流程Ⅰ中加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,除掉的离子分别是(填离子符号,注意顺序)。
③写出流程Ⅱ中发生反应的化学方程式:。
13. 某实验废液中可能含有 Cl-、C、Na+、Mg2+、Fe3+六种离子中的几种。为确定废液中存在的离子,进行了下面实验:①取少量废液,向废液中滴加NaOH溶液,有白色沉淀生成;
②另取少量废液,向其中滴加BaCl2溶液,无明显现象;
③最后取少量废液,滴加AgNO3溶液,产生白色沉淀,滴加稀硝酸后沉淀不溶解。
请分析实验后回答:
(1)、废液中含有离子的情况:。(2)、有同学认为实验③可以省略,理由是。14. 实验室有失去标签的两瓶无色溶液,分别是氢氧化钡溶液和稀硫酸中的一种。为了鉴别它们,设计如下鉴别方法:先把两瓶溶液分别贴上标签A、B,然后进行实验。加入的
试剂
实验现象
实验结论
方法1
锌粒
A中无明显现象;B中产生气泡
A是____
B是____
方法2
碳酸钠
溶液
A中____
B中____
化学小组同学对方法2进一步探究,设计了如下实验方案。
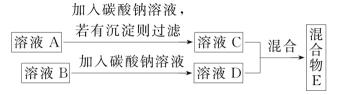
溶液C和溶液D混合,可能有以下三种情况:
(1)、若有气泡产生,写出反应的化学方程式:。(2)、若有沉淀产生,通过现象可推出溶液C中的溶质除了生成物NaOH外,还有;写出溶液A→溶液C发生反应的化学方程式:。(3)、若无明显现象,混合物E中所含溶质种类最多时,写出所有溶质的化学式:。三、实验探究题(共14分)
-
15.(1)、实验室中有两瓶失去标签的无色溶液,已知是NaOH溶液和Ca(OH)2溶液中的各一种,小明和小红同学想用化学方法确定各是哪种溶液,并进行了实验探究。
①小明各取两种无色溶液少许,分别加入A、B两支试管中,用干净的长塑料管分别向两试管中的溶液里慢慢吹气,观察到A试管中有白色浑浊现象,B试管中无明显现象。则可判断A试管中加入的是(填化学式)溶液。
②小红从下列四种试剂中选取了一种试剂,进行鉴别实验,根据明显现象也成功鉴别了上述两种无色溶液。则小红所选的这种试剂是(填序号)。
A.酚酞试液
B.稀盐酸C.Na2CO3溶液
D.NaCl溶液(2)、化学小组的同学欲探究某固体混合物A的成分,已知A中可能含有NaCl、CaCO3、CuSO4、(NH4)2SO4四种物质中的两种或多种,按下图所示进行探究实验,出现的现象如图中所述。(设过程中所有发生的反应都恰好完全反应)试根据实验过程和图示提供的信息,进行分析推理,回答下列问题:

①无色气体B的化学式为。
②无色气体E的化学式为。
③白色沉淀G的化学式为。
④根据上述实验现象推断,在固体混合物A里,上述四种物质中,肯定不存在的物质是(填化学式);肯定存在的物质是(填化学式)。
四、计算题(共12分)
-
16. 纯碱可用于造纸、玻璃生产等领域。纯碱产品中常含有少量的氯化钠杂质,某兴趣小组的同学为测定某品牌纯碱样品中碳酸钠的质量分数,设计了如图方案并进行实验。
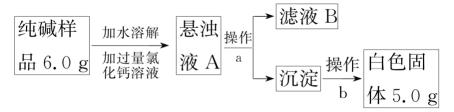 (1)、滤液B中含有的阳离子有(填化学符号)。(2)、若沉淀不经过操作b会使测定结果(填“偏大”“偏小”或“无影响”)。(3)、根据以上数据计算该样品中碳酸钠的质量分数。(写出计算过程,结果精确至0.1%)
(1)、滤液B中含有的阳离子有(填化学符号)。(2)、若沉淀不经过操作b会使测定结果(填“偏大”“偏小”或“无影响”)。(3)、根据以上数据计算该样品中碳酸钠的质量分数。(写出计算过程,结果精确至0.1%)
-