重庆市2022-2023学年高二下学期期末联合诊断检测化学试题
试卷更新日期:2023-09-22 类型:期末考试
一、单选题
-
1. 下列物质的主要成分属于天然有机高分子的是( )
A
B
C
D




飞机外壳——硬铝
汽车轮胎——合成橡胶
尼龙绳索——合成纤维
木头——纤维素
A、A B、B C、C D、D2. 最近,一组月球车辙照片在网络上开始流传,这组照片是由中国嫦娥四号任务上搭载的“玉兔二号”月球车所留下的,成为中国航天业的一大亮点。“玉兔二号”通过砷化镓(GaAs)太阳能电池提供能量进行工作,下列有关说法不正确的是( )A、镓的单质可作半导体材料 B、砷化镓太阳能电池能将化学能转化为电能 C、砷元素的电负性小于磷元素的电负性 D、砷的第一电离能比镓的第一电离能大3. 下列基态原子的原子核外未成对电子数最少的是( )A、P B、Cr C、Mg D、S4. 下列有机物的结构简式与对应的名称不正确的是( )A、HCOOC2H5:甲酸乙酯 B、CH3CH2CONH2:丙酰胺 C、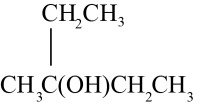 :3-甲基-3-戊醇
D、
:3-甲基-3-戊醇
D、 :聚乙烯
5. 有机化合物CH2Cl-CH2-CH=CH-CHO不可能发生的化学反应是( )A、酯化反应 B、加成反应 C、取代反应 D、氧化反应6. 下列分子或离子中,VSEPR模型和空间结构一致的是( )A、CO B、H2O C、NH3 D、SO27. 法匹拉韦常用于治疗流感,其结构如下图所示,下列有关说法正确的是( )
:聚乙烯
5. 有机化合物CH2Cl-CH2-CH=CH-CHO不可能发生的化学反应是( )A、酯化反应 B、加成反应 C、取代反应 D、氧化反应6. 下列分子或离子中,VSEPR模型和空间结构一致的是( )A、CO B、H2O C、NH3 D、SO27. 法匹拉韦常用于治疗流感,其结构如下图所示,下列有关说法正确的是( ) A、法匹拉韦属于氨基酸 B、法匹拉韦的分子式为C5H4FN3O2 C、法匹拉韦分子中的碳原子杂化方式为sp2、sp3 D、法匹拉韦分子只能跟酸反应,不能与碱反应8. 鉴别下列各组有机化合物,所选用试剂正确的是( )A、乙醇和乙酸乙酯:蒸馏水 B、乙醇和丙醛:酸性KMnO4溶液 C、苯酚稀溶液和丙醇:NaOH溶液 D、葡萄糖溶液和乙醛:新制银氨溶液9. 某短周期元素 M的各级电离能数据(用I1、I2……表示,单位为kJ/mol) 如下表所示。有关元素M的说法正确的是( )
A、法匹拉韦属于氨基酸 B、法匹拉韦的分子式为C5H4FN3O2 C、法匹拉韦分子中的碳原子杂化方式为sp2、sp3 D、法匹拉韦分子只能跟酸反应,不能与碱反应8. 鉴别下列各组有机化合物,所选用试剂正确的是( )A、乙醇和乙酸乙酯:蒸馏水 B、乙醇和丙醛:酸性KMnO4溶液 C、苯酚稀溶液和丙醇:NaOH溶液 D、葡萄糖溶液和乙醛:新制银氨溶液9. 某短周期元素 M的各级电离能数据(用I1、I2……表示,单位为kJ/mol) 如下表所示。有关元素M的说法正确的是( )I1
I2
I3
I4
……
M
740
1500
7700
10500
A、M的最高正化合价为+4价 B、M元素位于元素周期表中第ⅡA族 C、M元素可能属于非金属元素 D、M元素基态原子的价层电子排布式为np210. 下列实验装置及操作不能达到实验目的的是( )A
B
C
D
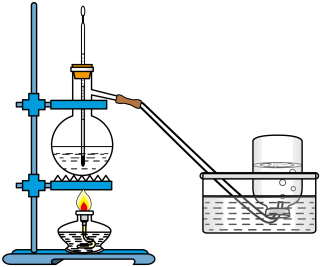



实验室制取乙烯
用饱和Na2CO3溶液除去乙酸乙酯中的乙酸
制备乙酸乙酯
证明酸性:硫酸>碳酸>苯酚
A、A B、B C、C D、D11. 在硫酸铜溶液中加入浓氨水,可形成配离子[Cu(NH3)4(H2O)2]2+。下列有关说法中正确的是( )A、中心离子的配位数为4 B、电负性由大到小为N>O>Cu C、基态原子的第一电离能:N>O>S D、键角:H2O>NH312. 由3-羟基丁酸可合成降解塑料聚羟基丁酸酯(PHB),下列说法正确的是( )A、3-羟基丁酸与乙酸互为同系物 B、3-羟基丁酸发生消去反应的产物只有一种 C、PHB的结构简式为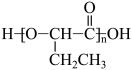 D、合成PHB的反应属于缩聚反应
13. “天然橡胶”(又称顺式聚异戊二烯),可以用下图所示流程合成顺式聚异戊二烯。有关说法正确的是( )
D、合成PHB的反应属于缩聚反应
13. “天然橡胶”(又称顺式聚异戊二烯),可以用下图所示流程合成顺式聚异戊二烯。有关说法正确的是( ) A、X中有2个手性碳原子 B、X可以被催化氧化成酮 C、顺式聚异戊二烯的结构简式为
A、X中有2个手性碳原子 B、X可以被催化氧化成酮 C、顺式聚异戊二烯的结构简式为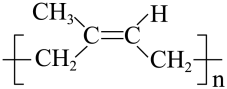 D、Y分子中量多有10个原子共平面
14. 由实验操作和现象,可以得出相应正确结论的是( )
D、Y分子中量多有10个原子共平面
14. 由实验操作和现象,可以得出相应正确结论的是( )选项
实验操作
现象
结论
A
向2%的氨水中滴加2%的AgNO3溶液
先有沉淀,后沉淀溶解
配制得到了银氨溶液
B
给石蜡油加强热,将产生的气体通入Br2的CCl4溶液
溶液由红棕色变成无色
产生的气体中含有不饱和烃
C
将溴乙烷与氢氧化钠的乙醇溶液共热,产生的气体直接通入酸性KMnO4溶液
酸性KMnO4溶液褪色
溴乙烷发生了消去反应
D
向含H2SO4的淀粉水解液中加入银氨溶液,加热
无现象
淀粉一定没有水解
A、A B、B C、C D、D二、填空题
-
15. 有四种从水仙花中提取出来的有机物,它们的结构简式如下所示。
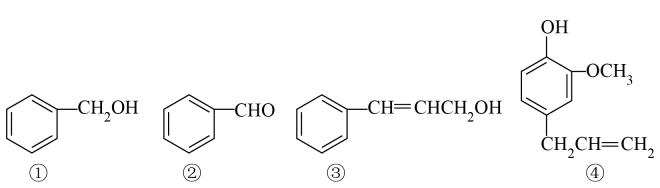
请回答下列问题:
(1)、能使酸性高锰酸钾溶液褪色的有(填序号, 后同);属于醇类的有机物是。(2)、1mol ④与溴水反应,最多消耗mol Br2。(3)、鉴别③和④所用的最佳试剂是。(4)、有机物M与③互为同分异构体,且遇FeCl3溶液发生显色反应,苯环上只有两个取代基,核磁共振氢谱只有5组峰的结构简式为(写出一种即可)。(5)、①经 (填反应类型) 可转化为②,写出其反应方程式;②发生银镜反应的化学方程式为。
三、结构与性质
-
16. 在月球玄武岩中发现了钛铁矿(主要成分的化学式含Ti、Fe、O三种元素),钛铁矿广泛应用于各个领域,包括冶金、化工、建筑、航空航天、电子等。请回答下列有关问题:(1)、铁在周期表中的位置是。(2)、基态钛原子的价层电子排布式为 , 其最外层电子的电子云轮廓图为。(3)、 中的配体为;其中 C原子的杂化类型为 , 1 mol 含有的σ键数目为。(4)、Ti的四卤化物的熔点如表所示,TiF4熔点高于其它三种卤化物,自TiCl4至TiI4熔点依次升高,其原因是。
化合物
TiF4
TiCl4
TiBr4
TiI4
熔点/℃
377
-24.12
38.3
155
(5)、钛铁矿主要成分的晶胞为立方体,其结构如图所示,钛铁矿主要成分的化学式为;已知该晶胞参数为a pm,NA为阿伏加德罗常数值,则该晶胞的密度为g/cm3(用含a、NA的代数式表示)。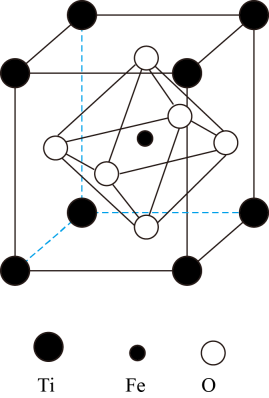
四、实验题
-
17. 有媒体报道:光催化涂料可以转化室内甲醛,生成无污染的物质。某课外活动小组设计了如下装置来检验光催化涂料对甲醛的催化氧化,并测定被氧化的甲醛的量(夹持仪器已略去)。
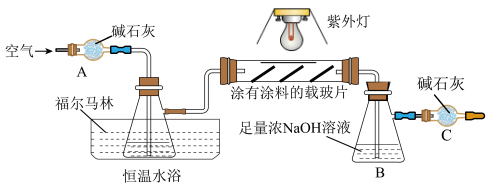
请回答下列问题:
(1)、仪器A的名称是。(2)、实验时,装入药品后,先 , 缓缓鼓入空气,一段时间后关闭紫外灯,再继续通入一会儿空气。开始鼓入空气的目的是 , 再继续通入一会儿空气的目的是。(3)、C中碱石灰的作用是 , 采用恒温水浴的目的是。(4)、甲醛在光催化涂料作用下发生反应的化学方程式为;B中反应的离子方程式为。(5)、当再继续通入一会儿空气后,向B装置加入足量CaCl2溶液,得到白色沉淀10.6g,则被氧化的甲醛的质量为g。五、有机推断题
-
18. 2-苯基丙烯酸甲酯(
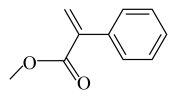 )是一种重要的化工原料、由芳香烃M (C9H10)合成2-苯基丙烯酸甲酯的流程如下图所示。
)是一种重要的化工原料、由芳香烃M (C9H10)合成2-苯基丙烯酸甲酯的流程如下图所示。  (1)、M→A、E→2-苯基丙烯酸甲酯的反应类型分别是。(2)、D中的官能团名称是。(3)、芳香烃M的结构简式为;两分子D反应得到含3个六元环的有机物的结构简式为。(4)、写出A→B的化学方程式。(5)、写出C与新制Cu(OH)2悬浊液反应的化学方程式。(6)、F与B互为同分异构体,满足下列条件的F的同分异构体有种(不考虑立体异构)。
(1)、M→A、E→2-苯基丙烯酸甲酯的反应类型分别是。(2)、D中的官能团名称是。(3)、芳香烃M的结构简式为;两分子D反应得到含3个六元环的有机物的结构简式为。(4)、写出A→B的化学方程式。(5)、写出C与新制Cu(OH)2悬浊液反应的化学方程式。(6)、F与B互为同分异构体,满足下列条件的F的同分异构体有种(不考虑立体异构)。①苯环上有三个取代基;②1mol F最多能消耗2 mol NaOH
-
-
-