湖北省鄂州市2023年中考模拟化学试题
试卷更新日期:2023-09-22 类型:中考模拟
一、单选题
-
1. 下列物质利用过程中,一定发生化学变化的是( )A、活性炭作吸附剂 B、水的汽化 C、生石灰作干燥剂 D、苛性钠潮解2. 如图所示的实验操作中正确的是( )A、
 测溶液的pH
B、
测溶液的pH
B、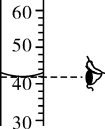 读液体体积
C、
读液体体积
C、 稀释浓硫酸
D、
稀释浓硫酸
D、 给液体加热
3. 下列实验对应的现象或化学方程式不正确的是( )A、将红热的木炭伸入盛满氧气的集气瓶中:木炭剧烈燃烧,发光放热,生成黑色固体 B、向滴有酚酞的氢氧化钠溶液中逐滴加入足量盐酸:溶液由红色变成无色 C、将稀盐酸滴入盛有镁条的试管中:Mg+2HCl=MgCl2+H2↑ D、将稀盐酸滴入盛有氧化铁粉末的试管中:Fe2O3+6HCl=2FeCl3+3H2O4. 我国自主研发的新冠疫苗,主要原料是胰蛋白酶,其中一种胰蛋白酶的化学式为C6H15O12P3 , 对于该胰蛋白酶说法正确的是( )A、该胰蛋白酶由36个原子构成 B、该胰蛋白酶中磷元素质量分数最小 C、该胰蛋白酶的相对分子质量为372g D、该胰蛋白酶中碳、氧元素质量比为3:85. 下列与水和溶液相关的说法不正确的是( )A、明矾可促进浑浊水中悬浮物的沉降 B、生活中可用煮沸的方法降低水的硬度 C、乳化后形成的乳液与溶液同样稳定 D、溶液加水稀释前后溶质的质量不变6. 为了缓解碳排放引起的温室效应,我国科学家成功合成新型催化剂,将二氧化碳转化为甲醇,该过程的微观示意图如图,下列说法正确的是( )
给液体加热
3. 下列实验对应的现象或化学方程式不正确的是( )A、将红热的木炭伸入盛满氧气的集气瓶中:木炭剧烈燃烧,发光放热,生成黑色固体 B、向滴有酚酞的氢氧化钠溶液中逐滴加入足量盐酸:溶液由红色变成无色 C、将稀盐酸滴入盛有镁条的试管中:Mg+2HCl=MgCl2+H2↑ D、将稀盐酸滴入盛有氧化铁粉末的试管中:Fe2O3+6HCl=2FeCl3+3H2O4. 我国自主研发的新冠疫苗,主要原料是胰蛋白酶,其中一种胰蛋白酶的化学式为C6H15O12P3 , 对于该胰蛋白酶说法正确的是( )A、该胰蛋白酶由36个原子构成 B、该胰蛋白酶中磷元素质量分数最小 C、该胰蛋白酶的相对分子质量为372g D、该胰蛋白酶中碳、氧元素质量比为3:85. 下列与水和溶液相关的说法不正确的是( )A、明矾可促进浑浊水中悬浮物的沉降 B、生活中可用煮沸的方法降低水的硬度 C、乳化后形成的乳液与溶液同样稳定 D、溶液加水稀释前后溶质的质量不变6. 为了缓解碳排放引起的温室效应,我国科学家成功合成新型催化剂,将二氧化碳转化为甲醇,该过程的微观示意图如图,下列说法正确的是( ) A、甲醇的化学式为CH3OH B、甲、丙、丁均为氧化物 C、参加反应的甲和乙分子个数比为1:1 D、生成丙和丁的质量比为9:167. 人们要强化安全意识,提升安全素养。下列有关燃烧和灭火说法中你认为不正确的是( )A、夜晚发现液化气泄漏,切忌立即开灯检查 B、炒菜时油锅中的油不慎着火,可用锅盖盖灭 C、水能浇灭燃着的木材,是水降低了其着火点 D、图书档案起火,用液态二氧化碳灭火器扑灭8. 化学知识在生产和生活中有着重要的应用,下列说法中正确的是( )A、铝制品比铁耐腐蚀,是因为铝比铁更难与O2反应 B、配制农药波尔多液时用到了石灰乳,因此要用铁桶盛装 C、合金的硬度一般比组成它们的纯金属硬度更高,性能更优越 D、“真金不怕火炼”主要是说黄金即使在高温时也很难熔化9. 下列各组物质在KOH溶液中能大量共存且溶液为无色的是( )A、NH4NO3、K2CO3、NaCl、Na2SO4 B、MgSO4、NaCl、Ba(NO3)2、FeCl3 C、KNO3、Na2SO4、KCl、Na2CO3 D、HCl、NaNO3、CuSO4、NH4Cl10. 一些物质的pH如图所示,下列有关说法不正确的是( )
A、甲醇的化学式为CH3OH B、甲、丙、丁均为氧化物 C、参加反应的甲和乙分子个数比为1:1 D、生成丙和丁的质量比为9:167. 人们要强化安全意识,提升安全素养。下列有关燃烧和灭火说法中你认为不正确的是( )A、夜晚发现液化气泄漏,切忌立即开灯检查 B、炒菜时油锅中的油不慎着火,可用锅盖盖灭 C、水能浇灭燃着的木材,是水降低了其着火点 D、图书档案起火,用液态二氧化碳灭火器扑灭8. 化学知识在生产和生活中有着重要的应用,下列说法中正确的是( )A、铝制品比铁耐腐蚀,是因为铝比铁更难与O2反应 B、配制农药波尔多液时用到了石灰乳,因此要用铁桶盛装 C、合金的硬度一般比组成它们的纯金属硬度更高,性能更优越 D、“真金不怕火炼”主要是说黄金即使在高温时也很难熔化9. 下列各组物质在KOH溶液中能大量共存且溶液为无色的是( )A、NH4NO3、K2CO3、NaCl、Na2SO4 B、MgSO4、NaCl、Ba(NO3)2、FeCl3 C、KNO3、Na2SO4、KCl、Na2CO3 D、HCl、NaNO3、CuSO4、NH4Cl10. 一些物质的pH如图所示,下列有关说法不正确的是( ) A、胃酸过多的人不宜多吃苹果 B、苹果汁的酸性比纯鲜牛奶的酸性强 C、肥皂水可以使无色酚酞溶液变红 D、厕所清洁剂与炉具清洁剂混用,清洁效果更好
A、胃酸过多的人不宜多吃苹果 B、苹果汁的酸性比纯鲜牛奶的酸性强 C、肥皂水可以使无色酚酞溶液变红 D、厕所清洁剂与炉具清洁剂混用,清洁效果更好二、填空题
-
11. 洋溢着绿色与科技元素的第24届冬奥会于2022年2月20日北京胜利闭幕,各项科技的运用向全世界展示了“中国智造”。(1)、衣:运动服中高科技材料石墨烯的使用,解决了超低温户外环境下运动员的取暖难题。石墨烯是由 元素组成的单质。(2)、食:人工智能带来的特色餐饮及服务使运动员们大饱口福。豆沙包受到很多人的喜爱,制作包子的面粉中富含的有机营养素是 。(3)、住:奥运村实现了5G网络的全覆盖。制造5G芯片的氮化镓(GaN)材料可由氯化镓(GaCl3)与氨气(NH3)反应制取,写出该过程的化学反应方程式 。(4)、行:冬奥会会务用车均使用氢能源汽车,基本实现了碳的零排放。实验室用锌与稀硫酸制取氢气时,反应的化学方程式为 。12. 化学与生产生活、人体健康密切相关。回答下列问题:(1)、2023年3月20日,鄂州花湖机场顺丰国际货站正式启用,在基础设施建设中选择应用新材料。机场使用了大量玻璃钢材料,玻璃钢是一种 ____(填字母序号)。A、复合材料 B、无机非金属材料 C、合成材料(2)、袁隆平院士的研究团队曾在我国高盐碱地区试种“海水稻”,高盐碱地区土壤的pH超过8.5,土壤pH越大,其碱性越 (填“强”或“弱”);化肥对提高农作物的产量具有重要作用,下列化肥中属于复合肥的是 (填选项序号)。
a.NH4NO3 b.NH4H2PO4 c.KNO3 d.KCl
(3)、鄂州市梁子湖太和千张,当地人习惯称“谢埠千张”,是鄂州著名的特产,以“薄、软、香”著称,是鄂东南地区的风味食品,堪称“湖北一绝”。千张中含有大量的蛋白质以及能够帮助人体形成骨骼,预防青少年佝偻病的 元素。三、推断题
-
13. 北京冬奥会的成功举办,让我们领略了无穷的冰雪魅力,如图“雪花”顶角上的A、B、C、D、E、F是初中化学常见的六种物质。其中D是金属单质,A、C是氧化物,A是黑色固体,C是气体;B、E、F依次是酸、碱、盐,B的浓溶液能夺取纸张里的水分,生成黑色的炭,E俗称熟石灰,F的溶液呈蓝色(图中“—”表示物质间能相互发生反应,“→”表示物质间能发生转化)。请写出你的推断:
 (1)、C和E之间的化学反应是否属于复分解反应?(填“是”或“否”)。(2)、D→A发生的反应的化学方程式为 。(3)、由B→F发生中和反应的化学方程式为 。
(1)、C和E之间的化学反应是否属于复分解反应?(填“是”或“否”)。(2)、D→A发生的反应的化学方程式为 。(3)、由B→F发生中和反应的化学方程式为 。四、填空题
-
14. 如图1是甲、乙、丙三种固体物质的溶解度曲线。请回答:
 (1)、t1℃时,甲和丙的饱和溶液溶质质量分数 (填“相等”或“不相等”)。(2)、t2℃时,将30g甲物质加入50g水中,充分溶解后,所得溶液的质量是 g。(3)、欲从含有少量乙的甲的饱和溶液中提纯甲,可采用 结晶的方法。(4)、某温度下,为使图2试管中的少量丙固体溶解,可向烧杯中加入 ____(填字母)。A、NaOH固体 B、NH4NO3固体 C、NaCl固体
(1)、t1℃时,甲和丙的饱和溶液溶质质量分数 (填“相等”或“不相等”)。(2)、t2℃时,将30g甲物质加入50g水中,充分溶解后,所得溶液的质量是 g。(3)、欲从含有少量乙的甲的饱和溶液中提纯甲,可采用 结晶的方法。(4)、某温度下,为使图2试管中的少量丙固体溶解,可向烧杯中加入 ____(填字母)。A、NaOH固体 B、NH4NO3固体 C、NaCl固体五、实验题
-
15. 某校化学兴趣小组学习了气体的制取和收集后,对相关知识进行总结,请你一起参与,并完成下面内容。
 (1)、写出下列仪器的名称:b 。(2)、请写出用一种纯净物加入装置A制取氧气的反应化学方程式 。若用E装置收集氧气,则氧气应该从 (选填“c”或“d”)口通入。(3)、装置B,C都可用来制取二氧化碳,装置C相对于装置B在操作方面的优势是 。
(1)、写出下列仪器的名称:b 。(2)、请写出用一种纯净物加入装置A制取氧气的反应化学方程式 。若用E装置收集氧气,则氧气应该从 (选填“c”或“d”)口通入。(3)、装置B,C都可用来制取二氧化碳,装置C相对于装置B在操作方面的优势是 。六、科学探究题
-
16. 工业铁红的主要成分是Fe2O3 , 还含有少量的FeO、Fe3O4。为了测定铁红中铁的质量分数,某化学兴趣小组的同学在胡老师的指导下进行了如下实验,请你参与过程分析。
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为H2C2O4•3H2OCO2↑+CO↑+4H2O。
【资料2】碱石灰为NaOH与CaO的混合物,可吸收CO2和H2O。
【问题讨论】用如图所示装置进行实验:
 (1)、草酸晶体在气体发生装置中分解,实验前应先 。(2)、实验过程中A、C装置中分别加入足量的NaOH溶液和浓硫酸,确保了进入D中的气体是纯净、干燥的CO,那么实验过程中B装置中的现象应该是 。(3)、写出D装置中主要成分发生反应的化学方程式 。(4)、【数据分析与计算】
(1)、草酸晶体在气体发生装置中分解,实验前应先 。(2)、实验过程中A、C装置中分别加入足量的NaOH溶液和浓硫酸,确保了进入D中的气体是纯净、干燥的CO,那么实验过程中B装置中的现象应该是 。(3)、写出D装置中主要成分发生反应的化学方程式 。(4)、【数据分析与计算】称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。实验前后称得E装置增重7.92g,则此铁红样品中铁元素的质量分数是 。
(5)、【实验评价】反思:胡老师指出了【问题讨论】中实验装置存在一个明显缺陷 。
七、计算题
-
17. 某补钙剂主要成分为碳酸钙(其他成分不溶于水也不与酸反应)。为了测定补钙剂中碳酸钙的质量分数,小明同学称取25g补钙剂放入烧杯中,再将加入100g足量的稀盐酸,充分反应后,测得烧杯中剩余物质总质量为119.5克,试回答:(1)、实验完成后,总产生CO2g。(2)、补钙剂中碳酸钙的质量分数是多少?(写出计算过程)
-
-
-
-