湖南省岳阳市2023年中考二模化学试题
试卷更新日期:2023-09-22 类型:中考模拟
一、单选题
-
1. 水是生命的源泉,是人类宝贵的资源。它有时能幻作朵朵白云,有时能化为绵绵细雨。下列过程中,你认为水分子发生了变化的是( )A、水蒸气遇冷凝结成水 B、蔗糖和水混合后得到糖水 C、水通电变成氢气和氧气 D、蒸馏法淡化海水2. 下列所述情况:①城市生活污水的任意排放;②农业生产中农药、化肥使用不当;③海上油轮石油泄漏;④工业生产中“三废”的任意排放,可能引起水污染的是( )A、①②③④ B、只有①④ C、只有②④ D、只有①③3. 下列实验操作的方法中正确的是( )A、将pH试纸浸入溶液中测溶液的pH B、用100 mL的量筒量取5.55 mL的稀硫酸 C、将氢氧化钠固体直接放在托盘天平的托盘上称量 D、配制10%的氯化钠溶液的主要步骤是:计算、称量、溶解4. 通常用的食醋中含有3%-5%的乙酸(化学式C2H4O2),有关乙酸的说法正确的是( )A、乙酸是一种氧化物 B、6g乙酸中含有2.4g碳元素 C、乙酸的相对分子质量为60g D、一个乙酸分子中含有2个碳原子、4个氢原子、1个氧分子5. 下列实验现象描述,正确的是( )A、硫在空气中燃烧发出明亮的蓝紫色火焰 B、氯化铵固体和熟石灰混合研磨,生成无色无味的气体 C、分别点燃一小块纯棉纤维和羊毛纤维,都产生了烧焦羽毛的气味 D、把带有火星的木条伸入盛有氧气的集气瓶中,木条复燃6.
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中不正确的是( )
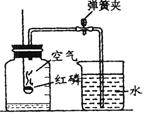 A、该实验证明空气中氧气的含量约占1/5 B、实验时红磷一定要过量 C、实验前一定要检验装置的气密性 D、红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹7. 据报道,用于清洗龙虾的“洗虾粉”中含有柠檬酸钠、亚硫酸钠(Na2SO3)等物质,可能对人体的健康产生危害。Na2SO3中S元素的化合价为()A、+6 B、+4 C、+2 D、-28. 在2A+B=2C+4D的反应中,14gA与48gB恰好完全反应生成44gC.若A的相对分子质量为28,则D的相对分子质量为( )A、36 B、72 C、18 D、649. 根据下图的微粒结构示意图,所获取信息不正确的是( )
A、该实验证明空气中氧气的含量约占1/5 B、实验时红磷一定要过量 C、实验前一定要检验装置的气密性 D、红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹7. 据报道,用于清洗龙虾的“洗虾粉”中含有柠檬酸钠、亚硫酸钠(Na2SO3)等物质,可能对人体的健康产生危害。Na2SO3中S元素的化合价为()A、+6 B、+4 C、+2 D、-28. 在2A+B=2C+4D的反应中,14gA与48gB恰好完全反应生成44gC.若A的相对分子质量为28,则D的相对分子质量为( )A、36 B、72 C、18 D、649. 根据下图的微粒结构示意图,所获取信息不正确的是( )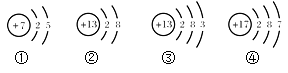 A、②、③表示的是同种元素的微粒 B、④表示的元素在化合物中通常显-1价 C、①、③、④表示的是原子 D、②、③化学性质相同10. 用一种试剂一次将澄清石灰水、氢氧化钠溶液、稀盐酸三种溶液区别开的是 ( )A、无色酚酞试液 B、二氧化碳气体 C、碳酸钠溶液 D、氯化钡溶液11. 将60℃饱和的硝酸钾溶液降温至20℃,没有发生变化的是( )A、溶液的质量 B、溶液里溶质的质量 C、溶液里溶剂的质量 D、溶液里溶质的质量分数12. 下列离子能在pH = 12的水溶液中大量共存的是( )A、Cl-、NO3-、K+、Na+ B、Na+、Cl-、OH-、Fe3+ C、SO42-、NO3-、K+、H+ D、Ag+、Cl-、CO32-、K+13. 向含有AgNO3、Fe(NO3)2、Mg(NO3)2的混合溶液中加入一定量的Zn粉,充分反应后过滤,再向滤渣中加入适量稀盐酸,发现有大量气泡产生,下列有关判断正确的是( )A、滤液中一定有Mg(NO3)2和Fe(NO3)2 B、滤液中不可能有AgNO3 C、滤渣中只有Fe D、滤渣中一定有Ag、Fe、Zn14.
A、②、③表示的是同种元素的微粒 B、④表示的元素在化合物中通常显-1价 C、①、③、④表示的是原子 D、②、③化学性质相同10. 用一种试剂一次将澄清石灰水、氢氧化钠溶液、稀盐酸三种溶液区别开的是 ( )A、无色酚酞试液 B、二氧化碳气体 C、碳酸钠溶液 D、氯化钡溶液11. 将60℃饱和的硝酸钾溶液降温至20℃,没有发生变化的是( )A、溶液的质量 B、溶液里溶质的质量 C、溶液里溶剂的质量 D、溶液里溶质的质量分数12. 下列离子能在pH = 12的水溶液中大量共存的是( )A、Cl-、NO3-、K+、Na+ B、Na+、Cl-、OH-、Fe3+ C、SO42-、NO3-、K+、H+ D、Ag+、Cl-、CO32-、K+13. 向含有AgNO3、Fe(NO3)2、Mg(NO3)2的混合溶液中加入一定量的Zn粉,充分反应后过滤,再向滤渣中加入适量稀盐酸,发现有大量气泡产生,下列有关判断正确的是( )A、滤液中一定有Mg(NO3)2和Fe(NO3)2 B、滤液中不可能有AgNO3 C、滤渣中只有Fe D、滤渣中一定有Ag、Fe、Zn14.下列图像能正确反映其对应操作中各量变化关系的是
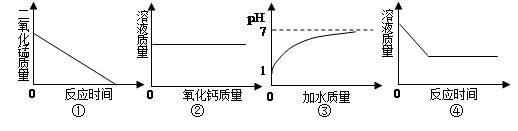 A、图①是给氯酸钾和二氧化锰的混合物加热 B、图②是向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体 C、图③是向pH=1的酸溶液中不断加水 D、图④是向一定质量的稀硫酸中加入锌粒
A、图①是给氯酸钾和二氧化锰的混合物加热 B、图②是向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体 C、图③是向pH=1的酸溶液中不断加水 D、图④是向一定质量的稀硫酸中加入锌粒二、多选题
-
15. 除去下列物质中混有的少量杂质(括号内为杂质),采用方法正确的是( )
选项
物质
操作方法
A.
NaCl(Na2CO3)
加入适量盐酸、蒸发、结晶
B.
KNO3溶液(CaCl2)
滴加K2CO3溶液至恰好完全反应,过滤
C.
CO2(HCl)
通过盛有足量氢氧化钠溶液的洗气瓶
D.
CuO(Cu)
通入足量氧气并加热
A、A B、B C、C D、D三、填空题
-
16. 化学就在我们身边,通过一年的学习,我有了许多收获:(1)、我认识了许多化学之最(用化学用语回答)
①空气中含量最多的气体单质是;
②最简单的有机物;
③地壳中含量最高的金属元素 .
(2)、我知道了许多鉴别物质的方法.①我会用鉴别软水和硬水.;
②我会用鉴别二氧化碳和一氧化碳;
③我会用法来鉴别合成纤维制品和羊毛制品.
17. 如图是a、b、c三种固体物质的溶解度曲线。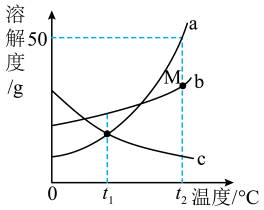 (1)、t1℃时,a、b、c三种固体物质的溶解度的大小关系是;(2)、t2℃,将30g物质a加到50g水中,形成溶液的质量为g。(3)、t2℃时,将a、b、c三种物质的饱和溶液降温到t1℃,仍为饱和溶液的是;(4)、在t2℃时,M点的a、b两种溶液的溶质质量分数大小关系为:ab(填“>”或“<”或“=”)。
(1)、t1℃时,a、b、c三种固体物质的溶解度的大小关系是;(2)、t2℃,将30g物质a加到50g水中,形成溶液的质量为g。(3)、t2℃时,将a、b、c三种物质的饱和溶液降温到t1℃,仍为饱和溶液的是;(4)、在t2℃时,M点的a、b两种溶液的溶质质量分数大小关系为:ab(填“>”或“<”或“=”)。四、推断题
-
18. A为含三种元素的钠盐,C为相对分子质量为100的白色不溶物,请填空:
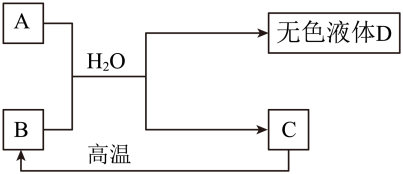 (1)、A、B、C(填写化学式)。(2)、D中一定含有的溶质是 , 理由是(用化学方程式表示)。(3)、D还可能含有溶质是。
(1)、A、B、C(填写化学式)。(2)、D中一定含有的溶质是 , 理由是(用化学方程式表示)。(3)、D还可能含有溶质是。五、实验题
-
19. 化学课上,小亮与老师一起演示了下图所示的实验:

请回答下列问题:
(1)、甲中铜丝受热时因生成了氧化铜而变黑,该变化属于(填“物理”或“化学”)变化。(2)、小亮将变黑的铜丝a伸入试管内的稀硫酸中,再取出时,铜丝表面又变红了,试管内发生反应的化学方程式是 , 该反应属于基本反应类型中的反应。(3)、老师将加热变黑的铜丝b趁热迅速伸入试管内的活性炭中,再取出时,铜丝表面也变红了,则试管内活性炭的质量一定会(填“增大”或“减小”)。六、计算题
-
20. 地沟油中含有一种强烈致癌物黄曲霉素B2(C17H14O6),长期食用会引起消化道癌变,请回答:(1)、黄曲霉素B2中碳、氢、氧三种元素的原子个数比为;(2)、15.7g黄曲霉素B2中含有克氧元素.
七、实验题
-
21. 实验室中,利用下列装置可以制取某些气体,请回答下列问题。
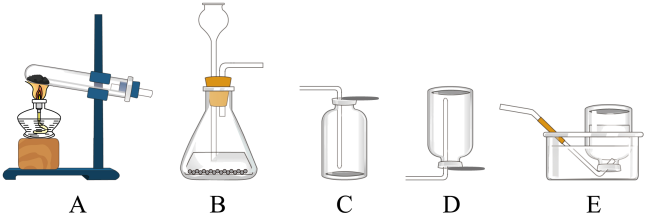 (1)、在加入药品之前应对实验装置进行。(2)、选用装置B和C可组成一套实验室制气装置。写出能用此装置制备气体的反应方程式。(3)、若选用A装置制备气体时应考虑的因素是。(4)、乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔。你认为制取较纯净的乙炔应选择的发生装置和收集装置是。
(1)、在加入药品之前应对实验装置进行。(2)、选用装置B和C可组成一套实验室制气装置。写出能用此装置制备气体的反应方程式。(3)、若选用A装置制备气体时应考虑的因素是。(4)、乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔。你认为制取较纯净的乙炔应选择的发生装置和收集装置是。八、科学探究题
-
22. 在一次化学课上,老师将几滴酚酞试液滴入氢氧化钠溶液中,溶液奇迹般地变红色。
【提出问题】在NaOH溶液中究竟哪种粒子使酚酞试液变红呢?
【查阅资料】NaOH溶液中存在粒子有:H2O、Na+、OH-。
【小凯猜想】①使酚酞试液变红色的是H2O;②使酚酞试液变红色的是Na+;③使酚酞试液变红色的是OH-。
【实验探究1】制三朵用酚酞试液染成无色的干燥纸花,按如图实验进行操作。
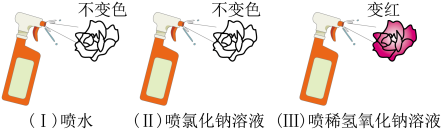
仔细观察上述实验,请回答:
(1)、实验(Ⅰ)、(Ⅱ)证实。(2)、猜想成立(填序号)。(3)、【思考】做完探究实验后,小凯同学欣喜异常,马上联想到氨气和氨水是否也能使酚酞试液变红呢?
【查阅资料】实验室常采用加热固体氢氧化钙和氯化铵的混合物来制取氨气;氨气极易溶于水,常温下,1体积水能吸收700体积的氨气,密度比空气小.
【实验探究2】制取氨气
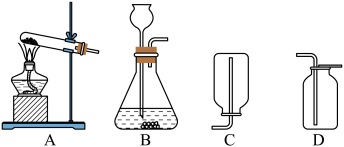
请你从以上装置中选择适合制取氨气的发生装置(填字母);收集装置(填字母);(4)、小凯同学又制两朵用酚酞试液染成无色的干燥纸花,按如图进行实验探究。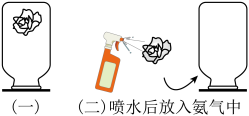
观察发现:(一)中纸花不变色,(二)中纸花变红,请回答下列问题:
通过(一)、(二)实验得出的结论是。
(5)、【实验探究3】小凯同学探究欲望持续上升,于是设计了以下装置:用甲、乙两套装置进行如下实验:胶头滴管吸取某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管,一段时间后两装置中气球明显胀大.
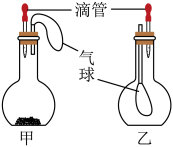
你认为甲装置中滴管和烧瓶所取的试剂是;所发生反应的化学方程式是。(6)、若乙胶头滴管中吸入的是水,则乙烧瓶中应充入的气体是。九、计算题
-
23. 刘彬同学父亲得知某地盛产石灰石,准备兴建一座碳酸钙精粉厂.为检测当地石灰石中碳酸钙的纯度,他在实验室用6g石灰石样品(杂质不参加反应)与19g稀盐酸恰好完全反应,测得残留物为22.8g.求:(1)、依椐质量守恒定律,生成二氧化碳g.(2)、样品中碳酸钙的质量分数 .(3)、所用稀盐酸溶液中溶质的质量分数 .
-
-
-
-
-
-