广西壮族自治区河池市2022-2023学年高一下学期化学期末教学质量检测试题
试卷更新日期:2023-09-21 类型:期末考试
一、单选题
-
1. 下列关于氮及其化合物的说法中不正确的是( )A、氮的固定过程中一定发生了氧化还原反应 B、氮氧化物大量排放到空气中会造成酸雨 C、NO和N2都可稳定存在于空气中 D、N2既可作氧化剂又可作还原剂2. 化学与科技、生产、生活密切相关,下列说法错误的是( )A、卡塔尔AIJanoub体育场屋顶采用聚四氟乙烯板材,该板材属于有机高分子材料 B、大飞机C919用到了铝锂合金,铝锂合金属于金属材料 C、光导纤维在信息技术发展中应用广泛,制造光导纤维的主要材料是单质硅 D、葡萄酒中通常含有微量的SO2 , 既可以杀菌又可以防止营养成分被氧化3. 从微观角度认识物质是掌握物质性质的途径之一。下列有关说法不正确的是( )A、乙烷的分子式:C2H6 B、的结构示意图:
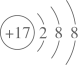 C、甲烷分子的空间填充模型:
C、甲烷分子的空间填充模型: D、氨气的电子式:
4. 已知化学反应的能量变化如图所示,则有关说法错误的是( )
D、氨气的电子式:
4. 已知化学反应的能量变化如图所示,则有关说法错误的是( )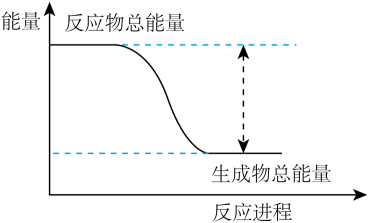 A、随着反应的进行,该反应向环境放出热量 B、A2的稳定性大于物质AB C、该反应中,化学键断裂吸收的总能量小于化学键形成放出的总能量 D、铝片与盐酸反应的能量变化趋势与图示相似5. “绿色化学”也称作环境友好化学,其核心思想就是改变“先污染后治理”的观念和做法。下列实验或叙述中不符合“绿色化学”理念的是( )A、用乙醇汽油代替普通汽油作汽车燃料 B、工业合成氨时,氨分离后剩余的气体再利用 C、制CuSO4时先将Cu氧化成CuO后再与稀硫酸反应 D、通过化学方法去治理排放到环境中的废气、废渣、废液6. 乙醇和乙酸是人们生活和生产中常用的有机物。下列有关说法错误的是( )A、乙醇的催化氧化可以得到乙酸 B、1 mol乙醇可以和足量的金属钠反应产生0.5 mol H2 C、可用酸性高锰酸钾溶液鉴别乙醇和乙酸 D、可用饱和的碳酸钠溶液除去乙酸乙酯中的乙酸7. 设为阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,1 mol苯的体积为22.4 L B、1 mol S在足量氧气中燃烧生成SO3的数目为 C、1 mol铁和过量稀硝酸反应,转移的电子数目为 D、30 g乙烷中含有C—H键的数目为8. 煤、石油和天然气的综合利用能够提高利用率,减少污染,获得多种化工产品。下列说法错误的是( )A、天然气的主要成分为CH4 B、通过石油裂化和裂解可获得乙烯、丙烯等重要的基本化工原料 C、煤的干馏和石油的分馏均属于化学变化 D、石油分馏后得到的汽油、煤油、柴油均是混合物9. 一定量的一氧化氮和足量碳在恒容密闭容器中发生反应: , 下列不能说明反应已达平衡状态的是( )A、NO的转化率不再发生变化 B、容器内压强不再发生变化 C、容器内混合气体的平均相对分子质量不再发生变化 D、容器内混合气体的密度不再发生变化10. 下列各组物质互为同分异构体的是( )A、16O2与18O2 B、CH4与CH3CH3 C、正丁烷与异丁烷 D、乙烷与乙烯11. 部分含铁物质的分类与相应化合价关系如图所示。下列推断合理的是( )
A、随着反应的进行,该反应向环境放出热量 B、A2的稳定性大于物质AB C、该反应中,化学键断裂吸收的总能量小于化学键形成放出的总能量 D、铝片与盐酸反应的能量变化趋势与图示相似5. “绿色化学”也称作环境友好化学,其核心思想就是改变“先污染后治理”的观念和做法。下列实验或叙述中不符合“绿色化学”理念的是( )A、用乙醇汽油代替普通汽油作汽车燃料 B、工业合成氨时,氨分离后剩余的气体再利用 C、制CuSO4时先将Cu氧化成CuO后再与稀硫酸反应 D、通过化学方法去治理排放到环境中的废气、废渣、废液6. 乙醇和乙酸是人们生活和生产中常用的有机物。下列有关说法错误的是( )A、乙醇的催化氧化可以得到乙酸 B、1 mol乙醇可以和足量的金属钠反应产生0.5 mol H2 C、可用酸性高锰酸钾溶液鉴别乙醇和乙酸 D、可用饱和的碳酸钠溶液除去乙酸乙酯中的乙酸7. 设为阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,1 mol苯的体积为22.4 L B、1 mol S在足量氧气中燃烧生成SO3的数目为 C、1 mol铁和过量稀硝酸反应,转移的电子数目为 D、30 g乙烷中含有C—H键的数目为8. 煤、石油和天然气的综合利用能够提高利用率,减少污染,获得多种化工产品。下列说法错误的是( )A、天然气的主要成分为CH4 B、通过石油裂化和裂解可获得乙烯、丙烯等重要的基本化工原料 C、煤的干馏和石油的分馏均属于化学变化 D、石油分馏后得到的汽油、煤油、柴油均是混合物9. 一定量的一氧化氮和足量碳在恒容密闭容器中发生反应: , 下列不能说明反应已达平衡状态的是( )A、NO的转化率不再发生变化 B、容器内压强不再发生变化 C、容器内混合气体的平均相对分子质量不再发生变化 D、容器内混合气体的密度不再发生变化10. 下列各组物质互为同分异构体的是( )A、16O2与18O2 B、CH4与CH3CH3 C、正丁烷与异丁烷 D、乙烷与乙烯11. 部分含铁物质的分类与相应化合价关系如图所示。下列推断合理的是( )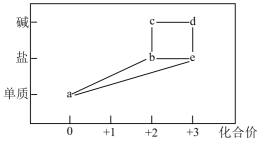 A、a可与e反应生成b B、b只有还原性,没有氧化性 C、可将溶液e加入浓碱液中制得d的胶体 D、不可能存在b→c→d→e→b的循环转化关系12. 下列实验操作能达到实验目的的是( )
A、a可与e反应生成b B、b只有还原性,没有氧化性 C、可将溶液e加入浓碱液中制得d的胶体 D、不可能存在b→c→d→e→b的循环转化关系12. 下列实验操作能达到实验目的的是( )选项
实验操作
实验目的
A
将海带灰溶于水,过滤,向滤液中滴加淀粉溶液
检测海带中含有碘元素
B
将SO2通入滴有酚酞的NaOH溶液中,溶液红色褪去
证明SO2的漂白性
C
向硅酸钠溶液中通入CO2气体,有白色沉淀产生
验证H2CO3的酸性强于H2SiO3
D
向市售乙醇中加入一小粒钠,有气泡产生
检测市售乙醇中存在水
A、A B、B C、C D、D13. 生命活动需要一系列的复杂的化学过程来维持,食物中的营养物质是这些过程的能量基础。下列关于糖类、油脂、蛋白质的说法正确的是( )A、糖类、油脂、蛋白质是人体必需的基本营养物质,在人体内都可以发生水解 B、向蔗糖溶液中加入稀硫酸并加热,再加入新制悬浊液,加热,未见砖红色沉淀,则蔗糖不发生水解 C、油脂在酸性条件下水解的反应叫皂化反应 D、农业上用波尔多液(由硫酸铜溶液和石灰乳制成)来防治植物病毒的原理是重金属阳离子和强碱能使蛋白质发生变性14. 下列热化学方程式书写正确的是( )A、1 mol CH4(g)完全燃烧生成CO2(g)和H2O(l)时放出890 kJ的热量,其热化学方程式为 B、1 mol H2在氧气中完全燃烧放出热量为285.8 kJ,其热化学方程式为 C、2 mol NO2分解生成1 mol O2和2 mol NO,并吸收116.2 kJ热量,其热化学方程式为 D、1 mol CaCO3吸收178.2 kJ的热量完全分解,则该反应的热化学方程式为15. 维生素A常作为保健药物,缓解视觉疲劳,维生素A的结构简式为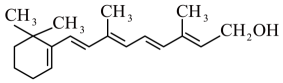 。下列有关维生素A的叙述正确的是( ) A、维生素A含有3种官能团 B、维生素A不能使溴的四氯化碳溶液褪色 C、1 mol维生素A最多可以和5 mol H2加成 D、维生素A不能和氧气发生催化氧化反应16. 理论上讲,任何自发的氧化还原反应都可以设计成原电池。某同学利用反应“”设计了一个化学电池(如图所示)。该电池在外电路中,电流从a极流向b极。下列说法正确的是( )
。下列有关维生素A的叙述正确的是( ) A、维生素A含有3种官能团 B、维生素A不能使溴的四氯化碳溶液褪色 C、1 mol维生素A最多可以和5 mol H2加成 D、维生素A不能和氧气发生催化氧化反应16. 理论上讲,任何自发的氧化还原反应都可以设计成原电池。某同学利用反应“”设计了一个化学电池(如图所示)。该电池在外电路中,电流从a极流向b极。下列说法正确的是( )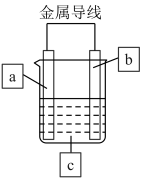 A、电极b的电极材料为铜,电极反应式为 B、电极a的电极材料可以为Ag,也可以是石墨或铁 C、c溶液为AgNO3溶液,放电时向b极移动 D、装置放电时主要将电能转化为化学能
A、电极b的电极材料为铜,电极反应式为 B、电极a的电极材料可以为Ag,也可以是石墨或铁 C、c溶液为AgNO3溶液,放电时向b极移动 D、装置放电时主要将电能转化为化学能二、填空题
-
17.(1)、Ⅰ.在一定温度下,4 L恒容密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图所示。回答下列问题:
根据题中数据写出该反应的化学方程式: , 时刻,N的平均速率为。 (2)、、、三个时刻中,处于平衡状态的为(填“”“”或“”),后的某一时刻给体系升高温度,v(正)将(填“增大”或“减小”)。(3)、平衡后容器中气体的压强和反应前气体的压强之比是 , 平衡时N的转化率为。(4)、Ⅱ.某学习小组利用铁与稀硫酸的反应,探究影响化学反应速率的因素,结果如下表:
(2)、、、三个时刻中,处于平衡状态的为(填“”“”或“”),后的某一时刻给体系升高温度,v(正)将(填“增大”或“减小”)。(3)、平衡后容器中气体的压强和反应前气体的压强之比是 , 平衡时N的转化率为。(4)、Ⅱ.某学习小组利用铁与稀硫酸的反应,探究影响化学反应速率的因素,结果如下表:实验序号
铁的质量(g)
铁的形态
V(H2SO4)(mL)
c(H2SO4)()
反应前溶液的温度(℃)
金属完全消失的时间(s)
1
0.10
片状
50
0.8
20
200
2
0.10
粉状
50
0.8
20
25
3
0.10
片状
50
1.0
20
125
4
0.10
片状
50
1.0
35
50
实验1、2表明对反应速率有影响。
(5)、探究温度对反应速率的影响的实验是(填实验序号)。(6)、实验开始后,会出现速率加快,一段时间后速率减慢,分析其原因。三、实验题
-
18. 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。(1)、请写出实验室制取乙酸乙酯的化学方程式:。(2)、实验室制取乙酸乙酯的主要步骤如下:
Ⅰ.在甲试管(如图)中先加入3 mL乙醇,然后边振荡试管边慢慢加入2 mL浓硫酸和2 mL乙酸,再加入几片碎瓷片;
Ⅱ.按图连接好装置(装置气密性良好),小火均匀地加热3~5 min;
Ⅲ.待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。

①加入碎瓷片的目的是。
②与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是。
(3)、为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用如图所示装置进行了以下4个实验。实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后,充分振荡乙试管,再测有机层的厚度,实验记录如下:实验编号
甲试管中试剂
乙试管中试剂
有机层的厚度/cm
A
2 mL乙醇、1 mL乙酸、3 mL 浓硫酸
饱和Na2CO3溶液
3.0
B
2 mL乙醇、1 mL乙酸、3 mL H2O
0.1
C
2 mL乙醇、1 mL乙酸、3 mL H2SO4溶液
0.6
D
2 mL乙醇、1 mL乙酸、盐酸
0.6
①实验D的目的是与实验C相对照,证明对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是mL和。
②若加入的乙酸为120 g,乙醇为138 g,发生酯化反应得到132 g乙酸乙酯,试计算该反应的产品的产率为(产率)。
(4)、乙酸乙酯的某种同分异构体分子中含有2个甲基,且能与碳酸氢钠溶液反应,则该物质的结构简式为。19. 某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,装置气密性良好,F是用于鼓入空气的双连打气球)。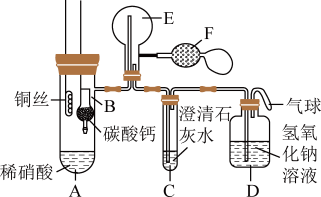
实验步骤与现象如下:
Ⅰ.将B装置下移,使碳酸钙与稀硝酸接触,产生气体;
Ⅱ.当C装置中产生白色沉淀时,立刻将B装置上提;
Ⅲ.将A装置中铜丝放入稀硝酸中,给A装置微微加热,A装置中产生无色气体,E装置中开始时出现浅红棕色气体;
Ⅳ.用F装置向E装置中鼓入空气,E装置中气体颜色逐渐加深;一段时间后,装置C中白色沉淀溶解。
回答下列问题:
(1)、写出操作Ⅰ中的化学方程式:。(2)、C装置中白色沉淀的化学式是。操作Ⅱ中当C装置中产生白色沉淀时立刻将B装置上提的原因是。(3)、写出操作Ⅲ中A装置中产生无色气体的化学方程式:。(4)、E装置内气体颜色逐渐加深的原因是。(5)、若该小组另取30 mL 的硝酸溶液与上述实验剩余的6.4 g铜丝在加热条件下反应,恰好完全反应,产生一定量NO和NO2的混合气体(反应过程中溶液体积变化忽略不计),则反应后的溶液中硝酸铜的物质的量浓度为(保留3位有效数字)。混合气体中NO的物质的量为mol。四、工业流程题
-
20. 工业上常以高硫铝土矿(主要成分为Al2O3、Fe2O3 , 还含有少量FeS2等)为原料,生产Fe3O4(Fe3O4中1个Fe呈+2价,2个Fe呈+3价)和铝单质的工艺流程如图所示:
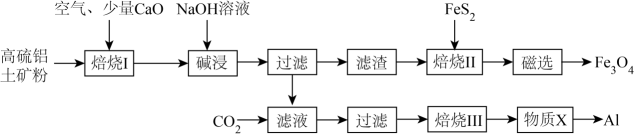
已知:①FeS2在“焙烧Ⅰ”过程中,发生反应的化学方程式为;②“焙烧Ⅱ”在隔绝空气的条件下发生反应的化学方程式为。
(1)、FeS2中硫的化合价为价;碱浸后滤渣的主要成分有(填化学式)。(2)、矿粉经过“焙烧Ⅰ”后,所得的大块烧渣需要进行“碱浸”,为了加快浸取的速率,可采取的措施有、(任写两点)。(3)、写出流程中过量CO2通入滤液中发生反应的离子方程式:。(4)、反应中产生的污染性气体SO2 , 可用下列哪种溶液吸收____(填字母)。A、浓硫酸 B、硝酸 C、NaOH溶液 D、氨水(5)、工业上,常用熔融的氧化铝为原料冶炼金属Al,发生反应的化学方程式为。生成的气体可以在流程的(填“焙烧Ⅰ”“焙烧Ⅱ”或“焙烧Ⅲ”)中循环使用。
-