沪教版初中化学2023-2024学年九年级上学期第3章 物质构成的奥秘素养检测
试卷更新日期:2023-09-18 类型:单元试卷
一、选择题(每小题3分,共36分)
-
1. 下列物质由分子构成的是( )A、金 B、金刚石 C、干冰 D、氯化钠2. 分类是学习和研究化学物质的重要方法,下列物质属于单质的是( )A、空气 B、水蒸气 C、氧气 D、天然气3. 日常生活中,人们常用84消毒液对环境进行消毒。84消毒液是常见的含氯消毒剂,其有效成分中的氯元素为+1价,则84消毒液的有效成分是( )A、氯化钠(NaCl) B、次氯酸钠(NaClO) C、氯酸钠(NaClO3) D、亚氯酸钠(NaClO2)4. 图中“●”和“○”分别表示两种质子数不同的原子,其中表示化合物的是 ( )A、
 B、
B、 C、
C、 D、
D、 5. 从分子的角度分析,下列解释不合理的是( )A、品红在水中扩散,说明分子在不断运动 B、水受热变为水蒸气体积变大,说明分子的大小随温度的升高而增大 C、将氧气压缩贮存于钢瓶中,说明分子之间有间隔 D、H2在Cl2中燃烧生成HCl,说明化学变化中分子发生改变6. 氚(chuān)和氚的化合物在核反应、医学、生命科学等领域有重要的用途。如图为氚原子微观构成的示意图,下列说法正确的是( )
5. 从分子的角度分析,下列解释不合理的是( )A、品红在水中扩散,说明分子在不断运动 B、水受热变为水蒸气体积变大,说明分子的大小随温度的升高而增大 C、将氧气压缩贮存于钢瓶中,说明分子之间有间隔 D、H2在Cl2中燃烧生成HCl,说明化学变化中分子发生改变6. 氚(chuān)和氚的化合物在核反应、医学、生命科学等领域有重要的用途。如图为氚原子微观构成的示意图,下列说法正确的是( ) A、氚原子含有2个质子 B、氚原子核电荷数为1 C、氚原子核外有2个电子 D、氚原子质子数和中子数相等7. 某元素X的原子序数为a,能够形成Xn- , 另一元素Y能够形成与Xn-具有相同电子层结构的Ym+ , 则Y元素的质子数是( )A、a+m-n B、a+m+n C、a-m-n D、a-m+n8. 关于下列符号或图示的说法正确的是( )
A、氚原子含有2个质子 B、氚原子核电荷数为1 C、氚原子核外有2个电子 D、氚原子质子数和中子数相等7. 某元素X的原子序数为a,能够形成Xn- , 另一元素Y能够形成与Xn-具有相同电子层结构的Ym+ , 则Y元素的质子数是( )A、a+m-n B、a+m+n C、a-m-n D、a-m+n8. 关于下列符号或图示的说法正确的是( )①2N ②2Fe2+ ③
 ④
④ ⑤
⑤ A、①表示2个氮分子 B、②表示2个铁离子 C、③和④构成物质的化学式为Al2O3 D、由⑤可知锡的相对原子质量为118.7 g9. “推理归纳”是化学学习过程中常用的方法,下列推理不合理的是( )A、化学变化一定有新物质生成,所以有新物质生成的变化一定是化学变化 B、原子都是由原子核和核外电子构成的,但原子中不一定都含有质子、中子和核外电子 C、单质是由一种元素组成的,所以由一种元素组成的纯净物都是单质 D、化学变化通常会伴随发光放热、颜色变化等现象,所以有这些现象的一定是化学变化10. 镁被誉为“国防金属”,是制造军事装备的重要原料。镁合金可以提高结构件强度,减轻装备重量和提高武器命中率。如图为镁原子的结构示意图,有关镁原子的说法不正确的是( )
A、①表示2个氮分子 B、②表示2个铁离子 C、③和④构成物质的化学式为Al2O3 D、由⑤可知锡的相对原子质量为118.7 g9. “推理归纳”是化学学习过程中常用的方法,下列推理不合理的是( )A、化学变化一定有新物质生成,所以有新物质生成的变化一定是化学变化 B、原子都是由原子核和核外电子构成的,但原子中不一定都含有质子、中子和核外电子 C、单质是由一种元素组成的,所以由一种元素组成的纯净物都是单质 D、化学变化通常会伴随发光放热、颜色变化等现象,所以有这些现象的一定是化学变化10. 镁被誉为“国防金属”,是制造军事装备的重要原料。镁合金可以提高结构件强度,减轻装备重量和提高武器命中率。如图为镁原子的结构示意图,有关镁原子的说法不正确的是( ) A、核外有3个电子层 B、质子数为12 C、该原子在化学反应中易失电子 D、“+”表示镁原子带正电11. 云南文山有“中国三七之乡”的美誉。《本草纲目》记载:“三七近时始出,南人军中,用为金疮要药,云有奇功”。三七中止血的活性成分主要是田七氨酸(C5H8N2O5),下列说法正确的是( )A、田七氨酸是由碳、氢、氮、氧四种元素组成的 B、田七氨酸中含N2O5分子 C、田七氨酸中碳元素的质量分数最大 D、田七氨酸中碳、氢、氮、氧元素的质量比为5∶8∶2∶512. 下列说法完全正确的是( )
A、核外有3个电子层 B、质子数为12 C、该原子在化学反应中易失电子 D、“+”表示镁原子带正电11. 云南文山有“中国三七之乡”的美誉。《本草纲目》记载:“三七近时始出,南人军中,用为金疮要药,云有奇功”。三七中止血的活性成分主要是田七氨酸(C5H8N2O5),下列说法正确的是( )A、田七氨酸是由碳、氢、氮、氧四种元素组成的 B、田七氨酸中含N2O5分子 C、田七氨酸中碳元素的质量分数最大 D、田七氨酸中碳、氢、氮、氧元素的质量比为5∶8∶2∶512. 下列说法完全正确的是( )A
氖气的化学式——Ne
1个硅原子——Si
1个钠离子——Na+1
B
决定元素种类——质子数
决定元素化学性质——最外层电子数
决定元素在周期表中的周期数——电子层数
C
铁——由分子构成
二氧化碳——由原子构成
硫酸铜——由离子构成
D
分子——化学变化中的最小粒子
原子——保持物质化学性质的最小粒子
离子——带电的原子或原子团
A、A B、B C、C D、D二、填空题(共37分)
-
13. 请用化学用语填空:(1)、地壳中含量最高的金属元素:;(2)、2个二氧化硫分子:;(3)、与
 对应的粒子符号:; (4)、标出氧化镁中镁元素的化合价:;(5)、2N2中前面的“2”表示 , 右下角的“2”表示。14. 钙是人体必需元素。
对应的粒子符号:; (4)、标出氧化镁中镁元素的化合价:;(5)、2N2中前面的“2”表示 , 右下角的“2”表示。14. 钙是人体必需元素。 (1)、如图为钙元素在元素周期表中的部分信息。钙元素的相对原子质量为 , 钙原子的核外电子数为。(2)、牛奶、豆类等食物含钙丰富,这里的“钙”指的是(填“单质”“元素”或“原子”)。(3)、人体若缺钙,可服用补钙剂。
(1)、如图为钙元素在元素周期表中的部分信息。钙元素的相对原子质量为 , 钙原子的核外电子数为。(2)、牛奶、豆类等食物含钙丰富,这里的“钙”指的是(填“单质”“元素”或“原子”)。(3)、人体若缺钙,可服用补钙剂。①缺钙可能导致的健康问题是(填“骨质疏松”或“贫血”)。
②服用主要成分为CaCO3的某钙片,与胃酸(含有HCl)反应后钙才能被吸收。该反应的符号表达式为。
15. 2019年诺贝尔化学奖授予约翰·古迪纳夫(以下简称约翰)、斯坦利·威廷汉和吉野彰(以下简称吉野)三人,以表彰他们在锂离子电池领域的贡献。
电池工作原理图
(1)、吉野用钴酸锂(LiCoO2)作电池正极,负极使用了石油工业副产品——石油焦,制造了首款商业锂离子电池。锂在化合物中常显+1价,则LiCoO2中Co的化合价为。(2)、约翰用磷酸铁取代钴酸锂,使电池更环保。磷酸铁的化学式为(磷酸化学式为H3PO4)。16. 回答下列问题。(1)、镓是一种奇妙的金属,放在手心马上熔化,犹如荷叶上的水珠流来流去。请阅读信息后回答:
①放在手心马上熔化,说明金属镓(填物理性质)。
②镓原子结构示意图中x的数值是 , 该元素的原子在化学反应中容易(填“得到”或“失去”)电子,形成的离子符号为;镓的相对原子质量为。
(2)、如图所示是氢分子和氧分子运动的示意图。
①在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是(填标号)。
②由图可知,影响分子运动速率的因素除温度外,还有。
③举一个能说明“温度升高,分子运动速率加快”的生活事例:。
17. 刘慈欣的科幻小说《中国太阳》中,中国科学家们通过在地球同步轨道上组装大型反射阵列,达到“指哪打哪”的效果。在现实情况中,“人造太阳”是利用了可控核聚变原理,过程如下图所示:
 (1)、图中“
(1)、图中“ ”代表中子,“
”代表中子,“ ”代表质子,则上述核聚变的过程中涉及种元素。 (2)、图中“
”代表质子,则上述核聚变的过程中涉及种元素。 (2)、图中“ ”可表示为 H,即质子数为1、质子数和中子数的和为3,“
”可表示为 H,即质子数为1、质子数和中子数的和为3,“ ”用上述符号表示为。 (3)、人类探测月球发现,其土壤中存在较丰富的“
”用上述符号表示为。 (3)、人类探测月球发现,其土壤中存在较丰富的“ ”,则其相对原子质量为 , 其原子结构示意图正确的是(填字母)。
”,则其相对原子质量为 , 其原子结构示意图正确的是(填字母)。
 18. 如表为元素周期表的一部分,表中数字表示原子序数。
18. 如表为元素周期表的一部分,表中数字表示原子序数。1
8
12
17
(1)、1号元素原子与17号元素原子相结合形成的化合物的化学式:;(2)、8号元素的原子结构示意图:;(3)、12号元素原子形成的离子符号:。三、实验探究题(共12分)
-
19. U形管是化学实验中常用的一种仪器。某同学利用U形管对分子运动及其影响因素进行了探究,实验装置如图1所示(U形管平放在实验台上)。已知:浓盐酸会挥发出氯化氢(HCl)气体,浓氨水会挥发出氨气(NH3),两种气体反应生成白色固体氯化铵(NH4Cl)。
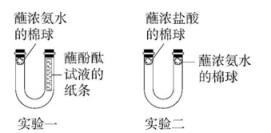 (1)、实验一中观察到的现象是。(2)、将实验一的U形管放入热水中,发现比常温下进行的实验更快观察到实验现象,这说明分子运动速率与有关。(3)、实验二中观察到产生白烟,白烟较多的位置是在U形管的偏左侧,这说明气体的相对分子质量越小,分子运动速率越(填“快”或“慢”)。(4)、【反思与提高】
(1)、实验一中观察到的现象是。(2)、将实验一的U形管放入热水中,发现比常温下进行的实验更快观察到实验现象,这说明分子运动速率与有关。(3)、实验二中观察到产生白烟,白烟较多的位置是在U形管的偏左侧,这说明气体的相对分子质量越小,分子运动速率越(填“快”或“慢”)。(4)、【反思与提高】用U形管探究分子运动的优点是。
(5)、U形管还可以用于空气中氧气含量的测定(如图2,夹持仪器省略),通电加热电阻丝可以点燃白磷,白磷燃烧的文字表达式是;得出空气中氧气的体积约占空气总体积的五分之一的实验现象是。
四、计算题(共15分)
-
20. 甲醇(CH3OH)是一种燃料。计算:(1)、甲醇的相对分子质量为;(2)、甲醇中碳、氢元素的质量比为(填最简比);(3)、甲醇中氧元素的质量分数为。21. 中国首位诺贝尔奖获得者屠呦呦继发现青蒿素后又发明了双氢青蒿素。图示是双氢青蒿素片的部分说明,请回答:
双氢青蒿素片
主要成分:C15H24O5
功能主治:适用于各种疟疾的症状控制
用法用量:口服1日1次,
成人1日3片
规格:每片含双氢青蒿素20 mg
(1)、双氢青蒿素中C、H、O的质量比为(填最简整数比)。(2)、双氢青蒿素中所含碳元素的质量分数为(结果精确到0.1%)。(3)、成人连用7日该药物,其中所含碳元素的质量为mg(假设其他成分不含碳元素,结果精确到0.1 mg)。
-