“高效课堂”1.4.1 NaOH的性质(提升版)--2023-2024学年浙教版科学九年级上册
试卷更新日期:2023-09-17 类型:同步测试
一、选择题
-
1. 图像能直观体现化学中的各种变化关系,下列图象中,能正确反映对应变化关系的是( )A、
 将等质量的锌粉、铁粉分别放入盛有足量且相同浓度稀盐酸的容器中
B、
将等质量的锌粉、铁粉分别放入盛有足量且相同浓度稀盐酸的容器中
B、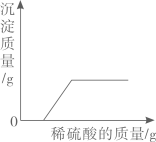 向NaOH和BaCl2的混合溶液中滴加H2SO4溶液
C、
向NaOH和BaCl2的混合溶液中滴加H2SO4溶液
C、 实验室的浓硫酸、浓盐酸敞口放置一段时间
D、
实验室的浓硫酸、浓盐酸敞口放置一段时间
D、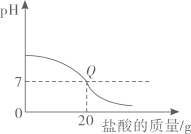 向20g10%氢氧化钠溶液中逐滴滴入7.3%的稀盐酸(Q点表示恰好完全反应)
2. 氢氧化钠能与多种物质发生反应。如图,其中能反应且观察到蓝色沉淀的是( )A、
向20g10%氢氧化钠溶液中逐滴滴入7.3%的稀盐酸(Q点表示恰好完全反应)
2. 氢氧化钠能与多种物质发生反应。如图,其中能反应且观察到蓝色沉淀的是( )A、 B、
B、 C、
C、 D、
D、 3. 将CO2通入NaOH溶液,为验证NaOH是否已被完全反应,有以下几种验证方法:①滴加酚酞试剂,如果变红,表示NaOH未反应完;②滴加过量的稀盐酸,如果出现气泡,表示NaOH已反应完;③滴加过量CaCl2,过滤后在滤液中滴加酚酞,如果不变红,表示NaOH已反应完;④加入过量BaCl2 , 充分反应后取上层清液,滴加CuCl2,如有蓝色絮状沉淀生成,表示NaOH未反应完。其中正确的是( )A、①② B、③④ C、①③ D、②④4. 下列有关氢氧化钠溶液的配制、保存和酸碱度测定的操作中,正确的是( )A、
3. 将CO2通入NaOH溶液,为验证NaOH是否已被完全反应,有以下几种验证方法:①滴加酚酞试剂,如果变红,表示NaOH未反应完;②滴加过量的稀盐酸,如果出现气泡,表示NaOH已反应完;③滴加过量CaCl2,过滤后在滤液中滴加酚酞,如果不变红,表示NaOH已反应完;④加入过量BaCl2 , 充分反应后取上层清液,滴加CuCl2,如有蓝色絮状沉淀生成,表示NaOH未反应完。其中正确的是( )A、①② B、③④ C、①③ D、②④4. 下列有关氢氧化钠溶液的配制、保存和酸碱度测定的操作中,正确的是( )A、 称量NaOH固体
B、
称量NaOH固体
B、 溶解NaOH固体
C、
溶解NaOH固体
C、 保存NaOH溶液
D、
保存NaOH溶液
D、 测NaOH溶液的pH
5. 实验室有一瓶变质的氢氧化钠溶液,小嘉想探究试剂瓶中的氢氧化钠是否已完全变质,设计了两种方案:①取部分试液,滴入过量CaCl2溶液,取上层清液滴入酚酞,观察溶液颜色变化;②取部分试液,滴入过量CuCl2溶液,取上层清液滴入酚酞,观察溶液颜色变化。对于上述两种方案,你认为( )A、两种方案都行 B、方案①行,方案②不行 C、两种方案都不行 D、方案①不行,方案②行6. 小科同学为了区别氢氧化钠溶液和氢氧化钡溶液,设计了如图所示的四组实验方案,其中能达到目的的是( )A、
测NaOH溶液的pH
5. 实验室有一瓶变质的氢氧化钠溶液,小嘉想探究试剂瓶中的氢氧化钠是否已完全变质,设计了两种方案:①取部分试液,滴入过量CaCl2溶液,取上层清液滴入酚酞,观察溶液颜色变化;②取部分试液,滴入过量CuCl2溶液,取上层清液滴入酚酞,观察溶液颜色变化。对于上述两种方案,你认为( )A、两种方案都行 B、方案①行,方案②不行 C、两种方案都不行 D、方案①不行,方案②行6. 小科同学为了区别氢氧化钠溶液和氢氧化钡溶液,设计了如图所示的四组实验方案,其中能达到目的的是( )A、 B、
B、 C、
C、 D、
D、 7. 向某无色溶液中加入NaOH后能产生沉淀,则该溶液可能是( )A、MgCl2溶液 B、Ba(NO3)2溶液 C、K2CO3溶液 D、CuSO4溶液8. 将稀盐酸分别滴入氢氧化钠溶液和氯化钠溶液中,充分混合后均无明显现象。混合后相关变化的微观示意图如下,下列说法正确的是( )
7. 向某无色溶液中加入NaOH后能产生沉淀,则该溶液可能是( )A、MgCl2溶液 B、Ba(NO3)2溶液 C、K2CO3溶液 D、CuSO4溶液8. 将稀盐酸分别滴入氢氧化钠溶液和氯化钠溶液中,充分混合后均无明显现象。混合后相关变化的微观示意图如下,下列说法正确的是( ) A、物质间均未发生化学反应 B、变化中都有新物质产生 C、混合后溶液酸碱性都不变 D、图甲可用来表示酸碱反应的实质9. 一定温度下,向ag FeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如图所示。下列叙述错误的是( )
A、物质间均未发生化学反应 B、变化中都有新物质产生 C、混合后溶液酸碱性都不变 D、图甲可用来表示酸碱反应的实质9. 一定温度下,向ag FeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如图所示。下列叙述错误的是( ) A、P点对应的溶液中NaOH达到饱和状态 B、加入 ngNaOH时,NaOH固体和FeCl3溶液恰好完全反应 C、m>c-a D、生成Fe(OH)3的质量为(b-a)g
A、P点对应的溶液中NaOH达到饱和状态 B、加入 ngNaOH时,NaOH固体和FeCl3溶液恰好完全反应 C、m>c-a D、生成Fe(OH)3的质量为(b-a)g二、单选题
-
10. 在氢氧化钠溶液中加入一定量的稀盐酸,下列实验能证明两者恰好完全反应的是( )A、滴入适量FeCl3溶液,溶液变黃,但无沉淀生成 B、滴入几滴酚酞试液,酚酞试液不变色 C、测得反应后溶液中Na+与Cl-的个数比为1:1 D、滴入适量AgNO3溶液和稀硝酸;观察到有白色沉淀
三、填空题
-
11. 袋装食品中一般会放置一包干燥剂,干燥剂种类各不相同,氧化钙是比较常见的一种。(1)、氧化钙吸水的过程会 (选填“吸收”或 者“释放")热量。(2)、取少量氧化钙放入水中,所得溶液呈 (选填“酸性”、“碱性"或者“中性")。(3)、暴露在空气中的氧化钙,可能会转变成。12. 物质的结构决定性质,性质决定用途。请回答下列问题:(1)、氢氧化钠和氢氧化钙具有相似的化学性质,原因是它们在电离时都产生;(2)、氢氧化钠和氢氧化钙溶液都是无色透明的液体,为鉴别它们,小柯设计了如图四种方案(每种方案的两支试管中事先分别加入等量的上述两种碱)。其中可行的方案是。
 13. 图甲是关于氢氧化钠化学性质的思维导图,请据图回答问题。
13. 图甲是关于氢氧化钠化学性质的思维导图,请据图回答问题。 (1)、性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈色。(2)、性质②,将氢氧化钠溶液滴入稀盐酸中、图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是(填化学式)。(3)、依据性质③,除去硫酸厂在生产过程中产生的二氧化硫气体,化学方程式为。14. 将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题:
(1)、性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈色。(2)、性质②,将氢氧化钠溶液滴入稀盐酸中、图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是(填化学式)。(3)、依据性质③,除去硫酸厂在生产过程中产生的二氧化硫气体,化学方程式为。14. 将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题: (1)、请解释OA段的反应是缘故。(2)、请写出AB段发生反应的化学方程式。(3)、C点处溶液的pH7(填“>”、“=”或“<”)。15. 敞口放置的氢氧化钠溶液易变质,请写出此过程的化学方程式:。现向一定质量且部分变质的氢氧化钠溶液中滴加入稀盐,并振荡。(如下图)表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况。那么,图线BC段对应的实验现象是 , 在C点时溶液中的溶质是。
(1)、请解释OA段的反应是缘故。(2)、请写出AB段发生反应的化学方程式。(3)、C点处溶液的pH7(填“>”、“=”或“<”)。15. 敞口放置的氢氧化钠溶液易变质,请写出此过程的化学方程式:。现向一定质量且部分变质的氢氧化钠溶液中滴加入稀盐,并振荡。(如下图)表示反应过程中溶液质量随加入盐酸质量的变化而变化的情况。那么,图线BC段对应的实验现象是 , 在C点时溶液中的溶质是。
四、实验探究题
-
16. 小科将酚酞滴入氢氧化钠溶液时,发现了意想不到的现象:有的溶液变红后褪色;有的出现白色浑浊物。产生这些现象的原因是什么?他查阅资料得知酚酞试液由酚酞固体溶于酒精配制而成,并进行了以下探究:

试管编号 实验现象 1 0.1min红色褪去 2 5min红色褪去 3 30min红色明显变浅 4 120min红色无明显变浅 试管编号 实验现象 5 大量浑浊物 6 少量浑浊物 7 无浑浊物 猜想Ⅰ:红色褪去,与NaOH溶液和空气中的CO2反应有关。
猜想Ⅱ:红色褪去,与 有关。
猜想Ⅲ:出现白色浑浊物,与酚酞试液的浓度有关。为验证猜想Ⅱ和猜想Ⅲ,小科分别设计了如下实验:
(1)、实验1:同学们经过讨论,认为猜想Ⅰ是不可能的,其理由是。(2)、请将猜想Ⅱ补充完整。(3)、依据上述实验现象,为使酚酞滴入氢氧化钠溶液实验现象更明显,你认为实验中的药品应如何选择。17. 某科学兴趣小组在学完碱的化学性质时,进行了如图所示的实验:
实验1结束后,同学们对反应后的物质进行过滤,并对滤液中溶质的成分进行了探究。
[建立猜想]
猜想一:溶质为;
猜想二:溶质为NaOH和Na2CO3;
猜想三:溶质为NaOH和Ba(OH)2。
[实验探究]
组内同学采取不同的方法开展了实验2的研究,具体情况如下:
实验操作
实验现象
实验结论
甲同学:取少量滤液于试管中,向其中滴加适量的Na2CO3溶液。
无白色沉淀
①
乙同学:②
开始无现象,一段时间后有气泡产生
猜想二成立
请将表格中的实验结论①与实验操作②补充完整.
[反思与评价]
①从微观分析,实验1中OH-并没有实质参与反应,无法准确得出可溶性碱能与盐反应这一化学通性。有同学提出可以将Na2CO3溶液更换为溶液进行实验,让OH-实质参与反应来得出可溶性碱的这一化学通性。
②实验后的废液直接倒入下水道,会造成环境污染,需将废液处理后再排放。
五、解答题
-
18. 为探究一瓶久置的氢氧化钠固体样品是“部分变质还是完全变质”,小德取少量样品配制成溶液,进行了如图所示的实验(提示:BaCl2溶液呈中性)。
 (1)、实验一:定性分析。按下图所示进行实验。
(1)、实验一:定性分析。按下图所示进行实验。①试管乙中的白色沉淀是。
②实验中,下列溶液能代替氯化钡溶液,起到相同的作用的有。(可多选)
A.氢氧化钡
B.硝酸钡
C.硝酸钙
D.氯化钙
(2)、实验二:定量测量如图戊,准确称取10g变质的NaOH样品放入锥形瓶中,用电子秤称得锥形瓶及样品的总质量为46.95g,再把150.00g7.3%稀盐酸平均分成5等份,每份30.00g依次加入锥形瓶中,充分反应后用电子秤称得锥形瓶及所盛物质的总质量,实验数据记录如下:
加入盐酸的次数
第一次
第二次
第三次
第四次
第五次
锥形瓶及所盛物质总质量/g
76.95
106.95
136.73
164.09
193.65
根据上述实验数据,计算样品中氢氧化钠的质量的质量分数。
-