鲁教版(五四制)初中化学2023-2024学年八年级全册专项练习(五)化学方程式的计算
试卷更新日期:2023-09-14 类型:单元试卷
一、
-
1. 实验室可以通过分解过氧化氢溶液制取氧气。向盛有少量二氧化锰的烧杯中加入136 g过氧化氢溶液,充分反应后称得烧杯中物质总质量减少3.2 g。请计算:(1)、生成氧气的质量是g。(2)、所用过氧化氢溶液中过氧化氢的质量。2. 在海底和冻土层中存在着储量巨大的“天然气水合物”,其具有良好的开发和应用前景。科学家开采得到一种天然气水合物样品,取96 g 样品放置在一密闭容器内,该样品迅速转化为甲烷气体(CH4)和水,将甲烷气体分离出来并使其完全燃烧,得到33 g二氧化碳。求该天然气水合物样品中甲烷的质量分数。3. 为测定某石灰石样品中碳酸钙的质量分数,取一定质量的石灰石样品于烧杯中,将20 g 稀盐酸分4次加入样品中,每次充分反应后过滤、干燥、称重,实验数据如表所示。已知石灰石中的杂质既不与盐酸反应,也不溶于水。下列说法不正确的是( )
实验次数
一
二
三
四
稀盐酸的用量/g
5.0
5.0
5.0
5.0
剩余固体的质量/g
1.5
1.0
0.5
0.3
A、第三次实验后碳酸钙无剩余 B、第三次实验后已加入的盐酸无剩余 C、实验中所取样品质量为2 g D、样品中碳酸钙的质量分数是85%4. 我国约在南北朝时就开始冶炼黄铜(主要成分是铜和锌)。小华利用一瓶稀盐酸和相关的仪器测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30 mL稀盐酸分三次加入10 g黄铜样品粉末中,每次充分反应后测定生成氢气的质量,实验数据如表所示:实验次数
一
二
三
加入稀盐酸的体积/mL
10
10
10
生成氢气的质量/g
m
0.08
0.04
(1)、表中m的数值为。(2)、求该黄铜中铜的质量分数。(已知铜与稀盐酸不反应,Zn+2HCl= ZnCl2+H2↑)5. 为测定大理石中碳酸钙的质量分数,某化学兴趣小组取25 g大理石样品于烧杯中,向其中逐滴加入稀盐酸,测定生成CO2的质量。滴加稀盐酸的质量与生成CO2的质量关系如图所示。求此大理石中碳酸钙的质量分数。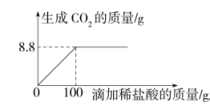 6. 为测定石灰石中碳酸钙的含量,取2.5 g 石灰石样品,加入稀盐酸,充分反应后测得剩余固体的质量与加入稀盐酸的质量关系如图所示(杂质既不参与反应,也不溶于水)。
6. 为测定石灰石中碳酸钙的含量,取2.5 g 石灰石样品,加入稀盐酸,充分反应后测得剩余固体的质量与加入稀盐酸的质量关系如图所示(杂质既不参与反应,也不溶于水)。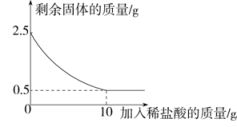 (1)、石灰石样品中碳酸钙的质量为g。(2)、反应中生成二氧化碳的质量是多少?7. 牙膏中常用轻质碳酸钙粉末等作摩擦剂。已知某品牌牙膏中的摩擦剂是CaCO3和SiO2(SiO2既不溶于水也不与稀盐酸反应)。化学兴趣小组用该牙膏的摩擦剂测定某盐酸的浓度,实验流程如图(假设产生的气体全部逸出):
(1)、石灰石样品中碳酸钙的质量为g。(2)、反应中生成二氧化碳的质量是多少?7. 牙膏中常用轻质碳酸钙粉末等作摩擦剂。已知某品牌牙膏中的摩擦剂是CaCO3和SiO2(SiO2既不溶于水也不与稀盐酸反应)。化学兴趣小组用该牙膏的摩擦剂测定某盐酸的浓度,实验流程如图(假设产生的气体全部逸出):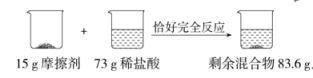 (1)、生成CO2的质量为g。(2)、求摩擦剂中CaCO3的质量分数。(写出计算过程)8. “追梦”学习小组为测定锌元素的相对原子质量,设计了下图所示实验方案进行探究(装置中盛放锌粒的网兜不与稀硫酸反应)。请根据他们的实验过程和测定的数据进行分析与计算。(电子秤示数单位为克)
(1)、生成CO2的质量为g。(2)、求摩擦剂中CaCO3的质量分数。(写出计算过程)8. “追梦”学习小组为测定锌元素的相对原子质量,设计了下图所示实验方案进行探究(装置中盛放锌粒的网兜不与稀硫酸反应)。请根据他们的实验过程和测定的数据进行分析与计算。(电子秤示数单位为克)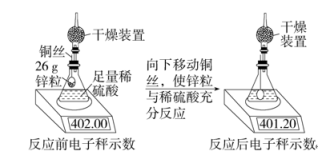 (1)、实验中设计干燥装置的目的是。(2)、锌完全反应后,产生氢气的质量为g。(3)、计算锌元素的相对原子质量。(提示:Zn+H2SO4=ZnSO4+H2↑)(写出计算步骤)
(1)、实验中设计干燥装置的目的是。(2)、锌完全反应后,产生氢气的质量为g。(3)、计算锌元素的相对原子质量。(提示:Zn+H2SO4=ZnSO4+H2↑)(写出计算步骤)