安徽省滁州市2022-2023学年高二下学期化学教学质量监测试题
试卷更新日期:2023-09-11 类型:期末考试
一、单选题
-
1. 化学与生产、生活密切相关。下列有关说法正确的是( )A、医用消毒酒精中乙醇的浓度(体积分数)为95% B、使用可降解的聚碳酸酯塑料有利于减少白色污染 C、丝绸、棉花和尼龙的主要成分均为合成纤维 D、燃煤中加入CaO可减少酸雨的形成和温室气体的排放2. 下列化学用语表述正确的是( )A、中子数为18的氯原子: B、的结构示意图:
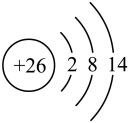 C、的空间结构:
C、的空间结构: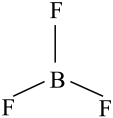 (平面三角形)
D、基态碳原子的轨道表示式:
(平面三角形)
D、基态碳原子的轨道表示式: 3. 是一种重要的染料及合成农药中间体。下列说法错误的是( )A、基态O原子的核外电子有8种空间运动状态 B、是由极性键构成的极性分子 C、电负性:O>N>S>H D、基态Cu原子介电子排布式是4. 我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程,下图为该历程示意图,下列说法不正确的是( )
3. 是一种重要的染料及合成农药中间体。下列说法错误的是( )A、基态O原子的核外电子有8种空间运动状态 B、是由极性键构成的极性分子 C、电负性:O>N>S>H D、基态Cu原子介电子排布式是4. 我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程,下图为该历程示意图,下列说法不正确的是( ) A、①→②放出能量并形成了C-C键 B、催化剂可提高反应物的平衡转化率 C、生成CH3COOH总反应的原子利用率为100% D、CH4→CH3COOH过程中,有C-H键发生断裂5. 下列对实验事实的理论解释错误的是( )
A、①→②放出能量并形成了C-C键 B、催化剂可提高反应物的平衡转化率 C、生成CH3COOH总反应的原子利用率为100% D、CH4→CH3COOH过程中,有C-H键发生断裂5. 下列对实验事实的理论解释错误的是( )选项
实验事实
理论解释
A
N原子的第一电离能大于O原子
N原子2p轨道上的电子处于半充满状态
B
键角:
电负性:N>P
C
酸性:
甲基是推电子基团
D
HF的沸点高于HCl
键能:H—F>H—Cl
A、A B、B C、C D、D6. HCHO与在水溶液中发生反应:。下列说法正确的是( )A、中含σ键的数目为8 B、中的配位数为6 C、中碳原子杂化方式有两种 D、HCHO分子空间构型为平面三角形,分子间可形成氢键7. 下图为几种晶体或晶胞的结构示意图。下列说法错误的是( ) A、1mol冰晶体中含有氢键数目为2NA B、四种晶体的熔点高低为:金刚石>MgO>冰>碘单质 C、碘晶体属于分子晶体,每个碘晶胞中实际占有8个碘原子 D、金刚石属于共价晶体,每个碳原子周围距离最近的碳原子数为48. 丹参酮是从中药丹参中提取的脂溶性化合物,具有抗菌消炎、活血化瘀和促进创口愈合等作用,其结构简式如下图所示。下列有关丹参酮说法错误的是( )
A、1mol冰晶体中含有氢键数目为2NA B、四种晶体的熔点高低为:金刚石>MgO>冰>碘单质 C、碘晶体属于分子晶体,每个碘晶胞中实际占有8个碘原子 D、金刚石属于共价晶体,每个碳原子周围距离最近的碳原子数为48. 丹参酮是从中药丹参中提取的脂溶性化合物,具有抗菌消炎、活血化瘀和促进创口愈合等作用,其结构简式如下图所示。下列有关丹参酮说法错误的是( ) A、分子式为 B、丹参酮不溶于水 C、能使酸性溶液褪色 D、与溴水既能发生取代反应,又能发生加成反应9. 有机物Y具有抗氧化、抗肿瘤作用,可由化合物X在一定条件下合成。
A、分子式为 B、丹参酮不溶于水 C、能使酸性溶液褪色 D、与溴水既能发生取代反应,又能发生加成反应9. 有机物Y具有抗氧化、抗肿瘤作用,可由化合物X在一定条件下合成。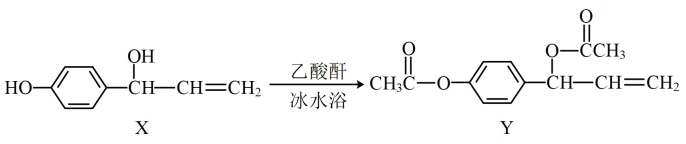
下列说法正确的是( )
A、不能用溶液鉴别X与Y B、X和邻苯二酚互为同系物 C、1molY与NaOH溶液反应,最多消耗3molNaOH D、X和Y均能发生取代反应、加成反应和消去反应10. 下列实验装置能达到实验目的的是( )选项
A
B
C
D
实验
目的
检验1-溴丙烷消去反应的产物
石油的分馏
实验室制硝基苯
验证酸性:盐酸>碳酸>苯酚
实验
装置
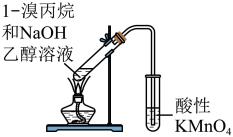
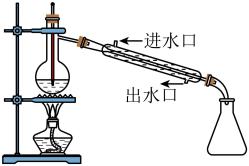
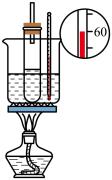
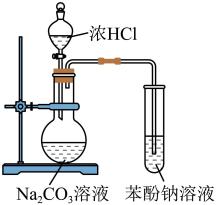 A、A B、B C、C D、D11. 实验室用0.1000HCl溶液滴定NaOH溶液,选用甲基橙作为指示剂。下列说法错误的是( )A、可用量筒量取25.00mLNaOH溶液置于锥形瓶中 B、应选用配带塑料塞的容量瓶配制NaOH溶液 C、用润洗过的酸式滴定管量取0.1000HCl溶液,赶走气泡、调节液面至“0”刻度 D、达到滴定终点时溶液显橙色12. 根据下列实验操作所得结论正确的是( )
A、A B、B C、C D、D11. 实验室用0.1000HCl溶液滴定NaOH溶液,选用甲基橙作为指示剂。下列说法错误的是( )A、可用量筒量取25.00mLNaOH溶液置于锥形瓶中 B、应选用配带塑料塞的容量瓶配制NaOH溶液 C、用润洗过的酸式滴定管量取0.1000HCl溶液,赶走气泡、调节液面至“0”刻度 D、达到滴定终点时溶液显橙色12. 根据下列实验操作所得结论正确的是( )选项
实验操作
结论
A
向某溶液中滴加溶液,产生蓝色沉淀
原溶液中有 , 无
B
2溶液与1KI溶液等体积混合,充分反应后滴加KSCN溶液,溶液变红
与的反应为可逆反应
C
向浓度均为0.05的NaI、NaCl混合溶液中滴加少量溶液,有黄色沉淀生成
D
对于与平衡体系,缩小容器体积,体系红棕色加深
平衡向生成的方向移动,使增大
A、A B、B C、C D、D13. 硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如下图所示。下列说法错误的是( )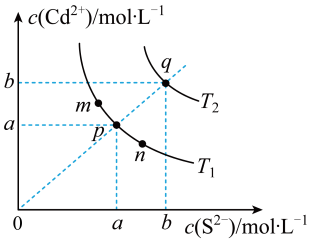 A、图中p和q分别为、温度下CdS达到沉淀溶解平衡 B、图中各点对应的的关系为: C、向m点的溶液中加入少量固体,溶液中浓度降低 D、温度降低时,q点饱和溶液的组成由q沿qp线向p方向移动14. 向体积均为1L的两恒容密闭容器中分别充入2molX发生反应 , 其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如下图所示。
A、图中p和q分别为、温度下CdS达到沉淀溶解平衡 B、图中各点对应的的关系为: C、向m点的溶液中加入少量固体,溶液中浓度降低 D、温度降低时,q点饱和溶液的组成由q沿qp线向p方向移动14. 向体积均为1L的两恒容密闭容器中分别充入2molX发生反应 , 其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如下图所示。
下列说法错误的是( )
A、该反应为放热反应 B、a和c点X的转化率相等 C、甲容器中温度不再改变时说明反应已达平衡 D、0-ts内,乙容器反应的平均速率为15. 钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。下图为电解方法制备金属钴的装置示意图。下列说法正确的是( )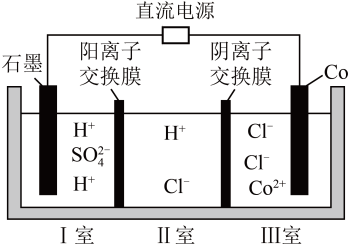 A、Co电极与电源的正极相连 B、电解过程中,Ⅱ室溶液的pH增大 C、移除阳离子交换膜后,石墨电极上发生的反应不变 D、外电路每通过1mol电子,Ⅲ室溶液质量理论上减少65g16. 常温下,用0.1mol·L-1HCl溶液滴定0.1mol·L-1 NH3·H2O溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列说法不正确的是( )
A、Co电极与电源的正极相连 B、电解过程中,Ⅱ室溶液的pH增大 C、移除阳离子交换膜后,石墨电极上发生的反应不变 D、外电路每通过1mol电子,Ⅲ室溶液质量理论上减少65g16. 常温下,用0.1mol·L-1HCl溶液滴定0.1mol·L-1 NH3·H2O溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列说法不正确的是( )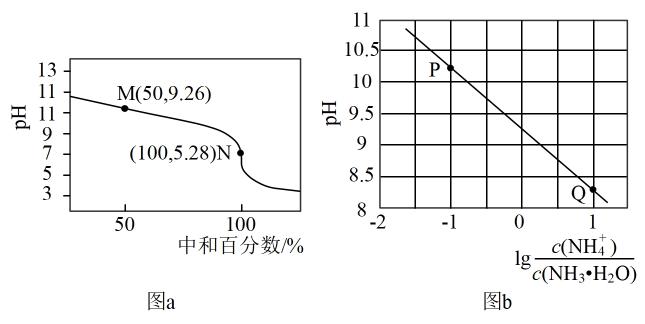 A、Kb(NH3·H2O)的数量级为10-5 B、P到Q过程中,水的电离程度逐渐增大 C、当滴定至溶液呈中性时,c(NH4+)>c(NH3·H2O) D、N点,c(Cl- ) - c(NH4+)=
A、Kb(NH3·H2O)的数量级为10-5 B、P到Q过程中,水的电离程度逐渐增大 C、当滴定至溶液呈中性时,c(NH4+)>c(NH3·H2O) D、N点,c(Cl- ) - c(NH4+)=二、结构与性质
-
17. 氮、硅和铬及其相关化合物用途非常广泛。回答下列问题:(1)、基态N原子的核外电子排布式是 , Cr位于元素周期表第四周期族。(2)、K和Cr属于同一周期,且核外最外层电子构型相同,两种元素原子第一电离能的大小关系是KCr(填“>”或“<”或“=”);的熔点(83℃)比的熔点(1100℃)低得多,这是因为。(3)、Cr的一种配合物结构如图所示:

①阴离子的空间构型是。
②配离子中,中心离子的配位数是 , N与中心原子形成的化学键是键。
(4)、Si与P形成的某化合物晶体的晶胞如图所示;该晶体类型是 , 该化合物的化学式是。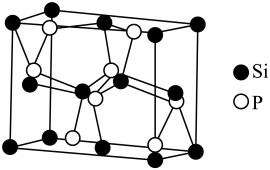
三、原理综合题
-
18. 将烟气中的还原为单质硫是一种具有经济效益和社会效益的脱硫方法。(1)、Ⅰ.氢气还原法: ……反应a
下图中曲线表示反应a,在有催化剂和无催化剂两种条件下反应过程中体系的能量变化。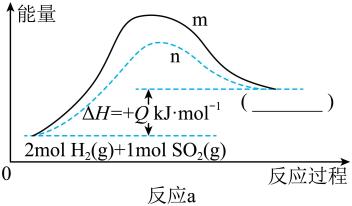
①曲线(填“m”或“n”)表示的是有催化剂参与反应的过程。
②图中括号内应该填写。
(2)、Ⅱ.一氧化碳还原法: ……反应b向恒温恒容密闭容器中充入一定量的CO和 , 发生反应b。下列描述可判断该反应达到平衡状态的是____。
A、气体的浓度不再变化 B、 C、 D、容器内的总压强不再变化(3)、某温度时,向2L的密闭容器中充入4molCO和2mol发生反应b,tmin时反应达平衡状态,测得CO的平衡转化率为90%。①0~tmin内,
②该温度下,反应b的平衡常数
(4)、Ⅲ.催化水煤气(CO、)还原该方法的部分反应过程如图所示。下列说法合理的是____。
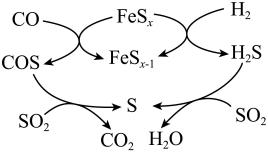 A、COS和为中间产物 B、可能存在反应 C、生成S的所有反应中,S均为还原产物 D、寻找更高效催化剂可提高S单质平衡回收率
A、COS和为中间产物 B、可能存在反应 C、生成S的所有反应中,S均为还原产物 D、寻找更高效催化剂可提高S单质平衡回收率四、实验题
-
19. 高铁酸钾()是一种高效净水剂,某实验小组制备高铁酸钾(为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生 , 在碱性溶液中较稳定。)并探究其性质。(1)、制备(夹持装置略)

请回答下列问题:
①A为氯气发生装置,发生反应的离子方程式是。(高锰酸根离子被还原为)。
②除杂装置B中盛放的试剂是 , 装置D的作用是。
③C中得到紫色固体和溶液,C中发生的反应有: , 另外还有。(用化学方程式表示)
(2)、探究的性质①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有。为证明是否是氧化了而产生 , 设计以下方案:
方案I
取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。
方案II
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将溶出,得到紫色溶液b;取少量溶液b,滴加盐酸,有产生。
I.由方案I中溶液变红可知溶液a中含有离子。
II.方案II可证明氧化了。用KOH溶液洗涤的目的是排除(填离子符号)的干扰。
②根据的制备实验可判定,氧化性:(填“>”或“<”);而方案II实验表明,和的氧化性强弱关系与上述判定相反,原因是。
五、有机推断题
-
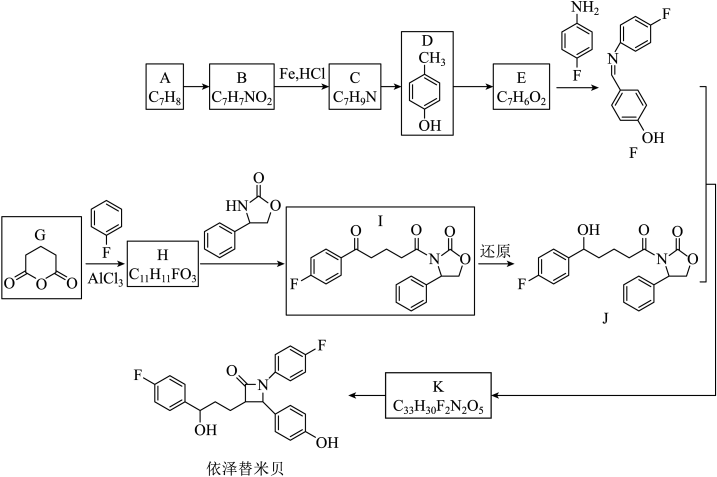
20. 依泽替米贝是一种新型高效、副作用低的调脂药,其合成路线如下图:
已知:R1-COOH+R2-NH-R3
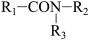
请回答下列问题:
(1)、A属于芳香烃,由A转化为B的反应类型是。(2)、C分子中含有氨基,其结构简式是。(3)、写出D的芳香族同分异构体的结构简式、(写出两种)。(4)、E分子中含有的官能团是、。(5)、G生成H的化学方程式是。六、工业流程题
-
21. 是锂离子电池中广泛应用的电解质。某工厂用LiF和为原料,低温条件下反应制备 , 其流程如下:
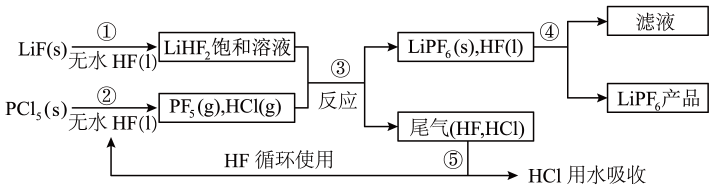
已知:HCl的沸点是−85.0℃,HF的沸点是19.5℃。
请回答下列问题:
(1)、第①步反应中无水HF的作用是、。反应设备不能用玻璃材质的原因是(用化学方程式表示)。(2)、该流程需在无水条件下进行,第③步反应中极易水解,其产物为两种酸,水解的化学方程式是。(3)、第④步分离采用的方法是。(4)、产品中通常混有少量LiF.取样品ng,测得Li的物质的量为wmol,则该样品中的物质的量是mol(用含w、n的代数式表示)。
-
-
-
-