云南省大理白族自治州2022-2023学年高二下学期7月化学期末试题
试卷更新日期:2023-09-11 类型:期末考试
一、单选题
-
1. 化学与生产生活密切相关,下列说法正确的是( )A、光导纤维的主要成分是二氧化硅 B、矿物油溅在衣物上可用热的纯碱溶液去除 C、垃圾填埋和焚烧可以减少对环境的污染 D、利用丁达尔效应可检测气溶胶中的冠状病毒2. 下列化学用语或图示表达正确的是( )A、基态Cr价层电子轨道表示式:
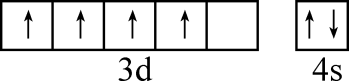 B、氯化氢的电子式:
C、丙烯球棍模型:
B、氯化氢的电子式:
C、丙烯球棍模型: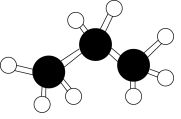 D、乙烯分子中的π键:
D、乙烯分子中的π键: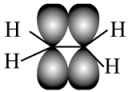 3. 醋酸乙烯酯是重要的化工原料,结构简式为
3. 醋酸乙烯酯是重要的化工原料,结构简式为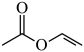 ,下列有关该物质说法正确的是( ) A、与乙酸乙酯互为同系物 B、不能发生加聚反应 C、该物质能与NaOH溶液反应 D、所有原子均处于同一平面4. 某元素基态原子价电子排布式为 , 下列说法不正确的是( )A、该原子位于周期表p区 B、该元素的最高正价为+4价 C、该基态原子中存在两个未成对电子 D、该元素最简单氢化物的空间构型是V形5. 为有效的保护环境,可以利用反应 减少汽车有害尾气排放,实现汽车尾气净化。下列措施能提高恒容容器中该反应NO转化率的是( )A、升高温度 B、充入一定量的 C、分离出部分氮气 D、通入稀有气体6. 下列说法正确的是( )A、和一定互为同系物 B、的名称是1,2-二氯乙烷 C、乙烯和异戊二烯互为同系物 D、甲苯和苯都能使酸性高锰酸钾溶液褪色7. 下列实验设计能达到实验目的的是( )
,下列有关该物质说法正确的是( ) A、与乙酸乙酯互为同系物 B、不能发生加聚反应 C、该物质能与NaOH溶液反应 D、所有原子均处于同一平面4. 某元素基态原子价电子排布式为 , 下列说法不正确的是( )A、该原子位于周期表p区 B、该元素的最高正价为+4价 C、该基态原子中存在两个未成对电子 D、该元素最简单氢化物的空间构型是V形5. 为有效的保护环境,可以利用反应 减少汽车有害尾气排放,实现汽车尾气净化。下列措施能提高恒容容器中该反应NO转化率的是( )A、升高温度 B、充入一定量的 C、分离出部分氮气 D、通入稀有气体6. 下列说法正确的是( )A、和一定互为同系物 B、的名称是1,2-二氯乙烷 C、乙烯和异戊二烯互为同系物 D、甲苯和苯都能使酸性高锰酸钾溶液褪色7. 下列实验设计能达到实验目的的是( )选项
实验目的
实验设计
A
证明非金属性Br>I
比较等浓度HI和HBr溶液的酸性
B
检验溶液中的
向溶液中加入酸化的 , 产生白色沉淀
C
除去中混有的
将混合气体通入饱和溶液
D
验证干燥是否具有漂白作用
将通入品红溶液,观察溶液是否褪色
A、A B、B C、C D、D8. 下列各组离子,在指定条件的溶液中能大量共存的是( )A、某无色澄清溶液中:、、、 B、常温下,由水电离出的浓度为: mol/L,的溶液:、、、 C、溶液中浓度为1 mol/L的溶液:、、、 D、常温下,的溶液:、、、9. 能正确表示下列反应的离子方程式的是( )A、铝溶解在NaOH溶液中: B、的水解: C、溶于硝酸反应: D、向氢氧化镁固体中滴加硫酸铁溶液:10. 短周期主族元素X、Y、Z、Q、W原子序数依次增大,X的一种核素常用于测定文物的年代,Z的一种单质常用来消毒杀菌,Q最外层有2个电子,W和Y同族。下列说法不正确的是( )A、第一电离能:X>Y>Z B、简单氢化物的沸点:Y>W C、最高价氧化物对应水化物的酸性:Y>X D、X、Y、Z的最简单氢化物的杂化方式均为杂化11. 下列说法不正确的是( )A、干冰和固体融化时,克服的作用力相同 B、氯化铯晶体中,每个周围紧邻8个 C、不能作为配合物的配体 D、离子化合物中可以存在非极性共价键12. 如图为等量和反应生成的微观示意图。下列说法正确的是( )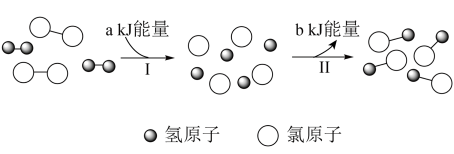 A、a>b B、过程I断开化学键,放出热量 C、、、HCl中均只存在共价键 D、HCl具有的能量低于和具有的能量13. 实验室利用铜与稀硝酸反应制少量NO,反应方程式为 , 设为阿伏加德罗常数的值,下列说法正确的是( )A、1 L 1 mol/L 溶液中含数为 B、标准状况下,22.4 L 中所含质子数为 C、192 g Cu参加反应,被还原分子数为 D、每生成1 mol NO,反应中转移的电子数为14. 下列说法不正确的是( )A、过度排放硫氧化物和氮氧化物会引起酸雨 B、亚硝酸钠是有毒物质,在食品工业中应禁止使用 C、利用丁达尔效应可以区别胶体和溶液 D、误食重金属盐可以服用大量的牛奶或蛋清解毒15. 硫酸工业是化学工业的基础工业之一。在密闭容器中充入一定量的和 , 发生反应: , 下列说法不正确的是( )A、保持容器压强不变,充入氦气,反应速率减小 B、保持容器体积不变,充入氦气,反应速率增加 C、保持容器体积不变,充入一定量的 , 反应后逆反应速率增加 D、升高温度,反应的正逆速率均增加16. 下列现象或事实的解释不正确的是( )
A、a>b B、过程I断开化学键,放出热量 C、、、HCl中均只存在共价键 D、HCl具有的能量低于和具有的能量13. 实验室利用铜与稀硝酸反应制少量NO,反应方程式为 , 设为阿伏加德罗常数的值,下列说法正确的是( )A、1 L 1 mol/L 溶液中含数为 B、标准状况下,22.4 L 中所含质子数为 C、192 g Cu参加反应,被还原分子数为 D、每生成1 mol NO,反应中转移的电子数为14. 下列说法不正确的是( )A、过度排放硫氧化物和氮氧化物会引起酸雨 B、亚硝酸钠是有毒物质,在食品工业中应禁止使用 C、利用丁达尔效应可以区别胶体和溶液 D、误食重金属盐可以服用大量的牛奶或蛋清解毒15. 硫酸工业是化学工业的基础工业之一。在密闭容器中充入一定量的和 , 发生反应: , 下列说法不正确的是( )A、保持容器压强不变,充入氦气,反应速率减小 B、保持容器体积不变,充入氦气,反应速率增加 C、保持容器体积不变,充入一定量的 , 反应后逆反应速率增加 D、升高温度,反应的正逆速率均增加16. 下列现象或事实的解释不正确的是( )选项
现象或事实
解释
A
对羟基苯甲醛沸点高于邻羟基苯甲醛
对羟基苯甲醛分子间形成氢键,而邻羟基苯甲醛形成分子内氢键。分子间氢键对沸点影响更大
B
在中的溶解度大于其在水中的溶解度
和均是非极性分子,水是极性分子,非极性分子易溶于非极性溶剂
C
三氟乙酸的酸性比乙酸的酸性强
F酸性强于H,三氟乙酸中具有多种酸性基团
D
乳酸(
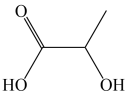 )存在两种空间结构
)存在两种空间结构乳酸中存在手性碳原子
A、A B、B C、C D、D17. 对于常温下等浓度和的溶液,下列说法正确的是( )A、两溶液均呈碱性,且pH相同 B、均存在 C、均存在 D、均存在18. 氮化镓(GaN)是一种直接能隙的半导体,是一种用途广泛的新材料。工业上利用Ga与高温条件下合成。反应方程式为 。如图,恒温恒容密闭体系内进行上述反应,下列说法正确的是( )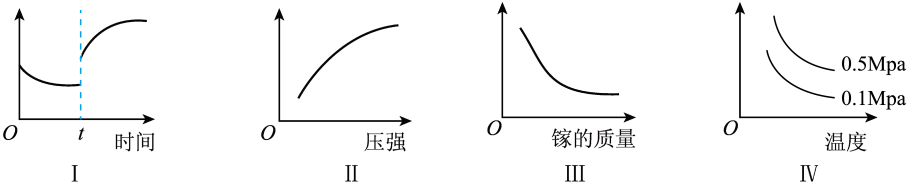 A、图Ⅰ可以表示催化剂对平衡的影响 B、图Ⅱ可以表示压强对平衡时体积分数的影响 C、图Ⅲ可以表示镓的质量对平衡常数的影响 D、图Ⅳ中纵坐标可以为体系内混合气体的密度19. 一种新型镁硫电池的工作原理如图所示。下列说法不正确的是( )
A、图Ⅰ可以表示催化剂对平衡的影响 B、图Ⅱ可以表示压强对平衡时体积分数的影响 C、图Ⅲ可以表示镓的质量对平衡常数的影响 D、图Ⅳ中纵坐标可以为体系内混合气体的密度19. 一种新型镁硫电池的工作原理如图所示。下列说法不正确的是( )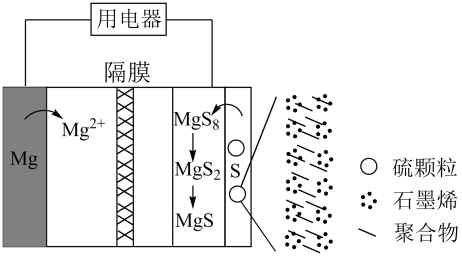 A、Mg电极是电源的负极 B、工作时,从左向右移动 C、工作时,正极反应为 D、若选用NaOH溶液作电解质,会降低该电池的工作效率20. 下列说法正确的是( )A、相同温度下,溶度积越大,溶解度越大 B、相同温度下,在水中和溶液中的相等 C、向悬浊液中,加入固体,溶液中增加 D、已知常温下 , 则常温下饱和AgCl溶液中为 mol/L21. 某温度下,在恒容密闭容器中发生可逆反应:。下列情况中不能说明该反应已达到化学平衡状态的是( )A、混合气体的颜色不变 B、混合气体的平均相对分子质量不变 C、混合气体的密度不再发生改变 D、密闭容器中的压强保持不变22. 常温时,分别向10mL浓度均为1mol/L的HCOOH和两种酸溶液加水稀释,所得pH与(V为溶液的体积)的关系如图所示。下列说法正确的是( )
A、Mg电极是电源的负极 B、工作时,从左向右移动 C、工作时,正极反应为 D、若选用NaOH溶液作电解质,会降低该电池的工作效率20. 下列说法正确的是( )A、相同温度下,溶度积越大,溶解度越大 B、相同温度下,在水中和溶液中的相等 C、向悬浊液中,加入固体,溶液中增加 D、已知常温下 , 则常温下饱和AgCl溶液中为 mol/L21. 某温度下,在恒容密闭容器中发生可逆反应:。下列情况中不能说明该反应已达到化学平衡状态的是( )A、混合气体的颜色不变 B、混合气体的平均相对分子质量不变 C、混合气体的密度不再发生改变 D、密闭容器中的压强保持不变22. 常温时,分别向10mL浓度均为1mol/L的HCOOH和两种酸溶液加水稀释,所得pH与(V为溶液的体积)的关系如图所示。下列说法正确的是( ) A、1mol/L溶液中水的电离程度: B、当时,HCOOH的 C、加入0.4g NaOH后,溶液中存在 D、中浓度小于中浓度
A、1mol/L溶液中水的电离程度: B、当时,HCOOH的 C、加入0.4g NaOH后,溶液中存在 D、中浓度小于中浓度二、实验题
-
23. 实验室中模拟工业上制取无水氯化铁的装置如图所示。
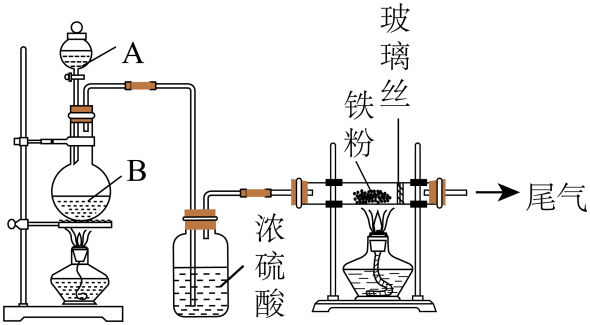
回答下列问题:
(1)、仪器B的名称是 , 仪器B中的药品可选择(填序号)。A.二氧化锰 B.固体 C.硝酸钠
(2)、硬质玻璃管的实验现象为。尾气处理可将尾气通入(填化学式)溶液。(3)、装置中,浓硫酸的作用是。反应后固体中常存在氯化亚铁杂质,改进方法是。(4)、为测定反应后样品中的质量分数,实验小组取a g样品,待样品全部溶于水后,向溶液中滴加NaI溶液。消耗0.1 mol⋅L-1 NaI溶液b mL。则反应后的样品中的质量分数为%(用含a、b的式子表示)。三、结构与性质
-
24. 铜是重要的战略资源,云南是我国铜资源储量较高的省份之一,回答下列问题:(1)、铜在周期表中位于第族(填族序数),属于区。(2)、铜可以形成多种配合物。
①的核外电子排布式是 , 过渡金属离子与水分子形成配合物时,若d轨道全空或全满时,化合物无颜色,否则有颜色。据此判断,(填“有”或“无”)颜色。
②可形成多种配合物,如 , 若其中两个被替换,得到的配合物只有两种结构,则的空间构型是 , 中N原子的杂化方式是 , 空间构型是。
(3)、铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:
①Cu原子的配位数是。
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为;B为;C为。则D原子的坐标参数为。
四、工业流程题
-
25. 是重要的化工原料,广泛应用于陶瓷、催化剂等工艺。实验室模拟用含钴废渣(主要成分为 , 还含有、ZnO、杂质)为原料制备的一种工艺流程如图:
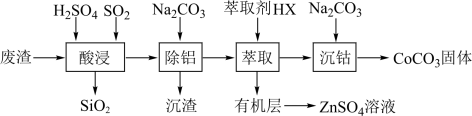
已知:①常温下,。
②相关金属离子[ mol⋅L]形成氢氧化物沉淀的pH范围如下:
金属离子
开始沉淀的pH
沉淀完全的pH
7.6
9.4
3.0
5.0
5.4
8.0
(1)、工业上,酸浸前通常将废渣粉碎,目的是 , 酸浸时,发生反应的化学方程式是 , 酸浸后分离的操作是。(2)、“除铝”过程中,发生反应的离子方程式为 , 应调节溶液pH的范围为。(3)、“萃取”过程可表示为(水层)+2HX(有机层)(有机层)(水层),实验室萃取时,用到的仪器有(填仪器名称)、烧杯、玻璃棒。从有机层获取溶液需要进行反萃取,下列溶液能作反萃取剂的是(填序号)。A.稀硫酸 B.NaOH溶液 C.酒精 D.四氯化碳
(4)、“沉钴”时,要使沉淀完全时[],溶液中应。五、原理综合题
-
26. 利用高效铜基催化剂,可以实现催化加氢合成甲醇。该技术是重要的碳捕获利用与封存技术,为我国碳达峰和碳中和目标提供技术支撑。回答下列问题:(1)、已知:反应Ⅰ. kJ⋅mol
反应Ⅱ. kJ⋅mol
则反应Ⅲ.的等于 , 该反应能自发的条件是(填“低温”或“高温”)。
(2)、保持温度不变,向体积恒定为2L的密闭容器中,充入2.0 mol 和6.0 mol , 发生反应Ⅲ测得的物质的量如下表所示:时间/min
0
2
4
6
8
/mol
2.0
1.5
1.2
1.0
1.0
①2~4 min内,用表示的化学反应速率。
②6 min时,的消耗速率的生成速率(填“大于”“小于”或“等于”)。
③写出既能加快反应Ⅲ的反应速率,又能提高反应Ⅲ中转化率的措施:(写出一条即可)。
(3)、在不同条件下,按起始量的配比发生反应Ⅲ。如图表示保持压强不变,不同温度时平衡体系中甲醇的物质的量分数。若210℃到达平衡时容器的体积为1L,则该温度下反应Ⅲ到达平衡的转化率 , 反应的平衡常数。 (4)、铜基催化剂可以用铜的氧化物制备。如图是铜的某种氧化物的晶胞示意图,该氧化物的化学式为。已知该晶胞参数为b nm,为阿伏加德罗常数,则该晶胞密度为g/cm。
(4)、铜基催化剂可以用铜的氧化物制备。如图是铜的某种氧化物的晶胞示意图,该氧化物的化学式为。已知该晶胞参数为b nm,为阿伏加德罗常数,则该晶胞密度为g/cm。
六、有机推断题
-
27. 如图是中学化学中常见的有机物转化关系(部分相关物质和反应条件已略去)。

回答下列问题:
(1)、F的名称是。(2)、下列说法正确的是(填序号)。a.B中所有原子均共平面 b.C中σ键和π键数目比为6∶1
c.D中所有碳原子均采用杂化 d.H中存在手性碳原子
(3)、写出H→B+D的化学方程式: , 反应类型是。、(4)、B→C反应的化学方程式是。(5)、符合下列条件的有机物共有种。①相对分子质量比B大14;②属于B的同系物。
-
-
-
-