北京市房山区2023年中考二模化学试题
试卷更新日期:2023-08-31 类型:中考模拟
一、单选题
-
1. 下列气体中,能供给动植物呼吸的是( )A、H2 B、O2 C、N2 D、CO22. 下列不属于新能源的是( )A、
 煤
B、
煤
B、 风能
C、
风能
C、 太阳能
D、
太阳能
D、 地热能
3. 人体缺钙会引起骨质疏松,这里的“钙”指的是( )A、原子 B、分子 C、元素 D、单质4. 牙膏中的含氟化合物对牙齿有保护作用。一种氟原子的原子核内有9个质子和10个中子,该原子的核外电子数为( )A、7 B、9 C、10 D、195. 能用于治疗胃酸过多症的物质是( )A、蔗糖 B、食盐 C、小苏打 D、食醋6. 下表列出了某饼干的营养成分,其中含量最高的营养素是( )
地热能
3. 人体缺钙会引起骨质疏松,这里的“钙”指的是( )A、原子 B、分子 C、元素 D、单质4. 牙膏中的含氟化合物对牙齿有保护作用。一种氟原子的原子核内有9个质子和10个中子,该原子的核外电子数为( )A、7 B、9 C、10 D、195. 能用于治疗胃酸过多症的物质是( )A、蔗糖 B、食盐 C、小苏打 D、食醋6. 下表列出了某饼干的营养成分,其中含量最高的营养素是( )项目
每100g
蛋白质
8.0g
脂肪
10.0g
碳水化合物
65.0g
钠
150mg
A、蛋白质 B、糖类 C、油脂 D、无机盐7. 炒菜时油锅着火,用锅盖盖灭,其灭火原理是( )A、隔绝空气 B、清除可燃物 C、降低可燃物的着火点 D、使可燃物温度降到着火点以下8. 6月5日是世界环境日,2023年中国主题为“美丽中国,我是行动者”。下列做法不符合这一主题的是( )A、外出随手关灯 B、减少使用塑料袋 C、纸张双面打印 D、夏天空调温度调至最低9. 将CO2通入下列液体中,能产生白色沉淀的是( )A、水 B、稀硫酸 C、食盐水 D、澄清石灰水10. 下列物质含有氢分子的是( )A、H2 B、H2O2 C、H2SO4 D、Ca(OH)211. 下列不属于CO2用途的是( )A、灭火 B、作燃料 C、人工降雨 D、气体肥料12. 下列物质中,不需密封保存的是()A、浓硫酸 B、氢氧化钠 C、大理石 D、浓盐酸13. 下列物质中,属于氧化物的是( )A、O2 B、NaCl C、H2O D、NaOH14. 下列化学方程式书写正确的是( )A、CaO+H2O=Ca(OH)2 B、2Fe+3H2SO4=Fe2(SO4)3+3H2↑ C、2H2O=2H2↑+O2↑ D、Na2CO3+Ca(OH)2=CaCO3↓+NaOH15. 化学肥料可提高农作物的产量,下列物质能用作钾肥的是( )A、K2SO4 B、NH4Cl C、NH4NO3 D、Ca(H2PO4)216. 下图为尿素[CO(NH2)2]中各个元素质量分数的示意图,其中表示氮元素质量分数的是( ) A、① B、② C、③ D、④17. 土壤的酸碱度会影响植物的生长.下列植物在微酸性土壤中,不适宜种植的是( )
A、① B、② C、③ D、④17. 土壤的酸碱度会影响植物的生长.下列植物在微酸性土壤中,不适宜种植的是( )植物
花生
苹果
西瓜
沙枣
适宜的pH范围
5.0~6.0
5.0~6.5
6.0~7.0
8.0~8.7
A、花生 B、苹果 C、西瓜 D、沙枣18. 下列物质常用于改良酸性土壤的是( )A、石灰石 B、烧碱 C、食盐 D、熟石灰19. 下列不能用于取用固体药品的是( )A、药匙 B、镊子 C、纸槽 D、胶头滴管20. 实验室蒸发食盐水,不需要用到的仪器是( )A、蒸发皿 B、玻璃棒 C、酒精灯 D、漏斗21. 下列行为不符合实验安全要求的是( )A、熄灭酒精灯时,用灯帽盖灭 B、稀释浓硫酸时,将浓硫酸注入水中 C、加热液体时,试管口不能对着人 D、使用氢氧化钠时,用手直接接触药品22. 用如图装置测定空气中氧气的体积分数。下列说法不正确的是( ) A、加热铜丝引燃红磷,利用了铜的导热性 B、红磷的作用是消耗装置内的氧气 C、红磷燃烧时左侧水面下降 D、两侧水面高度最终保持一致
A、加热铜丝引燃红磷,利用了铜的导热性 B、红磷的作用是消耗装置内的氧气 C、红磷燃烧时左侧水面下降 D、两侧水面高度最终保持一致二、选择题组
-
23. 20℃时,按下表数据配制溶液,完成下面小题。
序号
①
②
③
④
固体种类
NaCl
NaCl
MgCl2
MgCl2
固体的质量/g
30
50
30
50
水的质量/g
100
100
100
100
 (1)、①~④所得溶液属于饱和溶液的是( )A、① B、② C、③ D、④(2)、下列关于①~④所得溶液的说法不正确的是( )A、溶质质量:①<② B、溶液质量:①=③ C、溶质质量分数:②=④ D、④中溶质与溶剂的质量比为1:2
(1)、①~④所得溶液属于饱和溶液的是( )A、① B、② C、③ D、④(2)、下列关于①~④所得溶液的说法不正确的是( )A、溶质质量:①<② B、溶液质量:①=③ C、溶质质量分数:②=④ D、④中溶质与溶剂的质量比为1:2三、单选题
-
24. 实验小组用传感器探究过氧化氢分解的反应过程。实验装置及测定结果如下图所示。

下列说法不正确的是( )
A、实验前应先检查装置的气密性再加药品 B、二氧化锰在过氧化氢分解反应中做催化剂 C、锥形瓶中产生气泡证明过氧化氢分解生成了氧气 D、相对湿度减小说明浓硫酸具有吸水性四、填空题
-
25. 垃圾分类是新时尚。补齐废弃物与垃圾桶的连线。
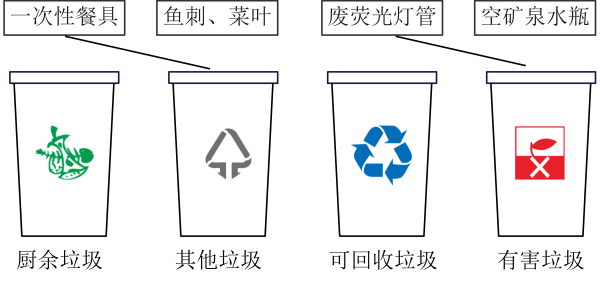 26. 二氧化碳加氢合成甲醇(CH3OH)可实现碳减排,该反应前后分子种类变化的微观示意图如下。
26. 二氧化碳加氢合成甲醇(CH3OH)可实现碳减排,该反应前后分子种类变化的微观示意图如下。 (1)、甲醇中碳、氢元素的质量比为。(2)、参加反应的甲与乙的分子个数比为。27. 氢能源汽车是未来汽车工业可持续发展的重要方向。(1)、下列汽车部件所使用的主要材料,属于有机合成材料的是____(填序号,下同)。A、钢制外壳 B、塑料灯罩 C、橡胶轮胎(2)、氢能源汽车中常用锆系储氢材料储存氢气。锆在元素周期表中的信息如图所示,下列说法正确的是____。
(1)、甲醇中碳、氢元素的质量比为。(2)、参加反应的甲与乙的分子个数比为。27. 氢能源汽车是未来汽车工业可持续发展的重要方向。(1)、下列汽车部件所使用的主要材料,属于有机合成材料的是____(填序号,下同)。A、钢制外壳 B、塑料灯罩 C、橡胶轮胎(2)、氢能源汽车中常用锆系储氢材料储存氢气。锆在元素周期表中的信息如图所示,下列说法正确的是____。 A、原子序数为40 B、元素符号为Zr C、属于金属元素 D、相对原子质量为91.22(3)、如图为氢能源汽车的电池工作原理图。电池工作时发生反应的化学方程式为。
A、原子序数为40 B、元素符号为Zr C、属于金属元素 D、相对原子质量为91.22(3)、如图为氢能源汽车的电池工作原理图。电池工作时发生反应的化学方程式为。
五、科普阅读题
-
28. 阅读下面的科普短文。
甲醛(CH2O)是一种无色有刺激性气味的气体,易挥发,易溶于水。作为室内装修最常见的污染物,其具有潜在的致敏、致畸、致癌性。
温度和湿度对甲醛的释放有较大影响,研究人员选取了部分装修后的住宅,测定了不同温度、湿度下室内甲醛浓度的变化,结果如表1和表2。
表1不同温度下室内甲醛浓度变化
温度/℃
≤23
23~25
25~27
≥27
甲醛浓度增长率/%
12.9
26.7
21.5
36.9
表2不同湿度下室内甲醛浓度变化
湿度/%rH
30~35
35~40
40~45
45~50
≥50
甲醛浓度增长率/%
16.5
18.8
7.3
43.0
33.3
降低室内甲醛含量最简单有效的方法是开窗通风。利用活性炭丰富的孔隙结构和较大的比表面积也可以吸附甲醛,该法是将甲醛从气态转化为固态存储,本质上并未改变其性质,因此当吸附接近饱和后,会有部分甲醛再次被释放,造成二次污染。采用化学降解法能彻底地去除甲醛,在甲醛催化分解材料的研究中,二氧化锰(MnO2)因其较高的低温催化活性和低毒、廉价等优势,而具有良好的应用前景。研究人员通过实验比较了不同形貌结构的MnO2对甲醛的去除效果,其结果如图。

随着科学技术的发展,更多去除甲醛的方法将会被开发和利用。
依据文章内容回答下列问题。
(1)、甲醛(CH2O)属于____(填序号)。A、纯净物 B、混合物 C、化合物(2)、甲醛的物理性质有(写出一条即可)。(3)、由表2可知,保持室内甲醛释放量维持在最低水平的湿度范围为%rH.(4)、判断下列说法是否正确(填“对”或“错”)。①由表1可知,甲醛浓度增长率随温度升高而增大。
②利用活性炭吸附甲醛时,甲醛分子不改变。
(5)、对比图中三条曲线,得到的结论是:在℃的温度范围内,当温度相同时,。六、流程题
-
29. 钛及其合金大量用于航空工业。利用钛铁矿(FeTiO3)制备钛的主要转化过程如下:

已知:焦炭的成分为C、SiO2、Al2O3.
(1)、TiCl4中钛元素的化合价为。(2)、①中X为一种反应物,从元素守恒的角度推测,X可能是____(填序号)。A、Cl2 B、O2 C、CO(3)、②中发生置换反应的化学方程式为。30. 碳酸锂(Li2CO3)是生产锂电池电极材料的主要原料。利用锂云母制取碳酸锂的主要流程如下: (1)、将锂云母与辅料送入混料机搅拌的目的是。(2)、焙烧炉中采用天然气(主要成分是甲烷)作燃料,其完全燃烧的化学方程式为。(3)、为除去水浸池中的不溶性硅砂杂质,可采用的操作为。(4)、反应釜中发生复分解反应,生成物为Li2CO3和。
(1)、将锂云母与辅料送入混料机搅拌的目的是。(2)、焙烧炉中采用天然气(主要成分是甲烷)作燃料,其完全燃烧的化学方程式为。(3)、为除去水浸池中的不溶性硅砂杂质,可采用的操作为。(4)、反应釜中发生复分解反应,生成物为Li2CO3和。七、实验题
-
31. 用下图实验研究铁的化学性质。

 (1)、实验1中,铁丝燃烧的化学方程式为。(2)、能证明铁丝与氧气发生化学反应的现象是。(3)、实验2中,证明铁生锈需要水的实验为(填序号)。(4)、依据实验2,写出一种防止铁生锈的方法:。32. 实验室配制200g溶质质量分数为5%的NaCl溶液。
(1)、实验1中,铁丝燃烧的化学方程式为。(2)、能证明铁丝与氧气发生化学反应的现象是。(3)、实验2中,证明铁生锈需要水的实验为(填序号)。(4)、依据实验2,写出一种防止铁生锈的方法:。32. 实验室配制200g溶质质量分数为5%的NaCl溶液。 (1)、需要称量NaCl的质量为g。(2)、正确的实验操作顺序为(填序号)。
(1)、需要称量NaCl的质量为g。(2)、正确的实验操作顺序为(填序号)。八、填空题
-
33. 请从A~C中任选2个作答。
装置及药品
现象
解释或结论

A、①
②铁丝
铁丝表面产生红色固体,溶液颜色变浅
Fe的金属活动性比Cu的强
B、①稀盐酸
②氧化铁
固体减少,得到黄色溶液
化学方程式:
C、①稀硫酸
②滴有酚酞的NaOH溶液
NaOH能与硫酸反应
九、实验题
-
34. 用下图装置研究物质的性质。
 (1)、石蕊纸条变红的是(填序号)。(2)、②中石蕊纸条变色的原因为。(3)、⑤中反应的化学方程式为。(4)、证明CO2能与水反应,应选取的实验方案为____。A、⑤ B、③⑤ C、③④⑤ D、①③④⑤35. 用下图实验制取CO2并研究其性质。
(1)、石蕊纸条变红的是(填序号)。(2)、②中石蕊纸条变色的原因为。(3)、⑤中反应的化学方程式为。(4)、证明CO2能与水反应,应选取的实验方案为____。A、⑤ B、③⑤ C、③④⑤ D、①③④⑤35. 用下图实验制取CO2并研究其性质。 (1)、步骤Ⅰ中用大理石和稀盐酸制取二氧化碳,反应的化学方程式为。(2)、用向上排空气法收集CO2的原因是。(3)、步骤Ⅱ中加入NaOH溶液后振荡,观察到气球变鼓,产生此现象的原因是。(4)、若证明CO2与NaOH发生了化学反应,可继续向锥形瓶中加入的药品是。
(1)、步骤Ⅰ中用大理石和稀盐酸制取二氧化碳,反应的化学方程式为。(2)、用向上排空气法收集CO2的原因是。(3)、步骤Ⅱ中加入NaOH溶液后振荡,观察到气球变鼓,产生此现象的原因是。(4)、若证明CO2与NaOH发生了化学反应,可继续向锥形瓶中加入的药品是。十、科学探究题
-
36. 酸奶是广受欢迎的乳制品。实验小组对影响酸奶发酵效果的因素进行了探究。
【进行实验】
实验1:探究影响酸奶稳定状态的因素
将仪器进行灭菌处理,添加适量乳酸菌粉和纯牛奶,密封发酵。实验记录如下:
实验序号
1-1
1-2
1-3
1-4
1-5
1-6
1-7
1-8
1-9
发酵温度/℃
36
36
36
38
x
38
40
40
40
发酵时间/h
6
7
8
6
7
8
6
7
8
乳清析出
大量
大量
较多
大量
较多
少量
较多
少量
无
组织状态
粗糙不稳定
粗糙不稳定
细腻不稳定
粗糙不稳定
细腻不稳定
细腻较稳定
细腻不稳定
细腻较稳定
细腻稳定
效果得分
54
61
70
65
72
85
75
88
96
注:效果得分越高,酸奶稳定状态越好。
实验2:探究影响酸奶口感的因素
将仪器进行灭菌处理,添加乳酸菌粉、白砂糖和纯牛奶,密封发酵。实验记录如下:
实验序号
2-1
2-2
2-3
2-4
2-5
乳酸菌接种量/%
6
6
6
10
14
白砂糖添加量/%
2
8
14
8
8
效果得分
61
99
77
72
52
注:效果得分越高,酸奶口感越好。
(1)、【解释与结论】牛奶发酵制酸奶属于(填“物理变化”或“化学变化”)。
(2)、1-5中x为。(3)、探究发酵温度对酸奶稳定状态影响的实验是(填序号)。(4)、依据1-7、1-8、1-9得出的结论是。(5)、2-1中口感较差的主要表现可能是(填“偏酸”或“偏甜”)。(6)、由上述实验,制作酸奶最好选择6%的乳酸菌接种量、8%的白砂糖添加量和。(7)、【反思与评价】依据实验数据,能否得出“乳酸菌接种量相同时,在实验研究范围内,白砂糖添加量越大,酸奶口感越好”的结论,说明理由:。
十一、计算题
-
37. 镁是航空工业的重要材料。工业上制金属镁的反应为。若制得24kg镁,计算参加反应的MgCl2的质量(写出计算过程及结果)。
-
-
-
-
-