浙江省湖州市2022-2023学年高二下学期期末检测化学试题
试卷更新日期:2023-08-16 类型:期末考试
一、单选题
-
1. 下列物质中属于共价晶体的是( )A、 B、 C、K D、2. 石膏()应用广泛,下列说法不正确的是( )A、S元素位于周期表p区 B、是强电解质 C、石膏水溶液呈酸性 D、煮沸的豆浆中加入适量石膏发生凝固3. 下列化学用语表示正确的是( )A、中子数为1的氢核素: B、硅的基态原子价电子轨道表示式:
 C、的空间结构:平面三角形
D、KCl形成过程:
C、的空间结构:平面三角形
D、KCl形成过程: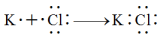 4. 物质的性质决定用途,下列两者对应关系不正确的是( )A、溶液显碱性,可用作洗涤剂 B、Fe粉具有还原性,可用作抗氧化剂 C、氨气易液化,液氨汽化时吸收大量的热,可用作制冷剂 D、明矾水解生成的胶体具有吸附性,可用作消毒剂5. 下列关于元素及其化合物的性质说法正确的是( )A、工业上通过电解制备Al和 B、FeO在空气中加热能迅速转化成 C、工业上用铜与浓硫酸反应制备 D、固体在空气中加热分解得到Na和6. 可以发生反应: , 为阿伏加德罗常数,下列说法正确的是( )A、是氧化产物 B、氧化剂和还原剂物质的量之比为1∶4 C、每转移个电子,就生成16g D、若设计成原电池,参与正极反应7. 下列反应的离子方程式正确的是( )A、碳酸钙与稀盐酸反应: B、向氯化亚铁溶液中通入少量氯气: C、向AgCl沉淀中加入KI溶液: D、将少量通入NaClO溶液:8. 下列说法不正确的是( )A、麦芽糖水解生成葡萄糖和果糖 B、酰胺在酸或碱存在并加热的条件下可以发生水解,均有盐生成 C、核酸是由许多核苷酸单体形成的聚合物 D、具有网状结构的聚丙烯酸钠是一种高吸水性树脂9. 氟他胺是一种抗肿瘤药,结构如图,下列说法正确的是( )
4. 物质的性质决定用途,下列两者对应关系不正确的是( )A、溶液显碱性,可用作洗涤剂 B、Fe粉具有还原性,可用作抗氧化剂 C、氨气易液化,液氨汽化时吸收大量的热,可用作制冷剂 D、明矾水解生成的胶体具有吸附性,可用作消毒剂5. 下列关于元素及其化合物的性质说法正确的是( )A、工业上通过电解制备Al和 B、FeO在空气中加热能迅速转化成 C、工业上用铜与浓硫酸反应制备 D、固体在空气中加热分解得到Na和6. 可以发生反应: , 为阿伏加德罗常数,下列说法正确的是( )A、是氧化产物 B、氧化剂和还原剂物质的量之比为1∶4 C、每转移个电子,就生成16g D、若设计成原电池,参与正极反应7. 下列反应的离子方程式正确的是( )A、碳酸钙与稀盐酸反应: B、向氯化亚铁溶液中通入少量氯气: C、向AgCl沉淀中加入KI溶液: D、将少量通入NaClO溶液:8. 下列说法不正确的是( )A、麦芽糖水解生成葡萄糖和果糖 B、酰胺在酸或碱存在并加热的条件下可以发生水解,均有盐生成 C、核酸是由许多核苷酸单体形成的聚合物 D、具有网状结构的聚丙烯酸钠是一种高吸水性树脂9. 氟他胺是一种抗肿瘤药,结构如图,下列说法正确的是( )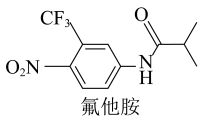 A、氟他胺分子中碳原子的杂化方式均为 B、氟他胺分子中共平面的碳原子最多有10个 C、氟他胺可发生取代、加成、消去反应 D、1mol氟他胺与足量NaOH溶液反应,最多可消耗3molNaOH10. X、Y、Z、W、R为原子序数依次增大的前20号主族元素,且位于四个周期,基态Y原子中s能级和p能级上电子数量相等,Z、W为同周期相邻元素,Y、W可形成如图所示的离子 , 下列说法正确的是( )
A、氟他胺分子中碳原子的杂化方式均为 B、氟他胺分子中共平面的碳原子最多有10个 C、氟他胺可发生取代、加成、消去反应 D、1mol氟他胺与足量NaOH溶液反应,最多可消耗3molNaOH10. X、Y、Z、W、R为原子序数依次增大的前20号主族元素,且位于四个周期,基态Y原子中s能级和p能级上电子数量相等,Z、W为同周期相邻元素,Y、W可形成如图所示的离子 , 下列说法正确的是( )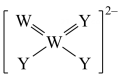 A、原子半径:Z<W<R B、Y和W的最简单氢化物沸点:Y<W C、X与R组成的化合物为分子晶体 D、W、R组成的化合物中可能含有非极性共价键11. 一种高效的除去废水中的的电化学装置如图所示。已知难溶于水,废水中发生的反应为 , 下列说法不正确的是( )
A、原子半径:Z<W<R B、Y和W的最简单氢化物沸点:Y<W C、X与R组成的化合物为分子晶体 D、W、R组成的化合物中可能含有非极性共价键11. 一种高效的除去废水中的的电化学装置如图所示。已知难溶于水,废水中发生的反应为 , 下列说法不正确的是( ) A、铁为阳极,电极反应为: B、通电后两电极附近的pH均增大 C、通电后,向铁电极移动 D、溶液中除去1mol , 电路中须通过电子12. 与水在空气中反应时会剧烈燃烧,甚至有爆炸的危险。工业上可由硅粉与氯化氢反应制得,主要副产物是、和 , (已知电负性数值Si~1.8:H~2.1)。下列说法不正确的是( )A、是非极性分子 B、存在同分异构体 C、遇水生成氢气 D、与乙醇反应生成和HCl13. 萤石()是自然界中常见的含氟矿物,其晶胞结构如图所示,该立方晶胞边长为apm。下列说法不正确的是( )
A、铁为阳极,电极反应为: B、通电后两电极附近的pH均增大 C、通电后,向铁电极移动 D、溶液中除去1mol , 电路中须通过电子12. 与水在空气中反应时会剧烈燃烧,甚至有爆炸的危险。工业上可由硅粉与氯化氢反应制得,主要副产物是、和 , (已知电负性数值Si~1.8:H~2.1)。下列说法不正确的是( )A、是非极性分子 B、存在同分异构体 C、遇水生成氢气 D、与乙醇反应生成和HCl13. 萤石()是自然界中常见的含氟矿物,其晶胞结构如图所示,该立方晶胞边长为apm。下列说法不正确的是( )
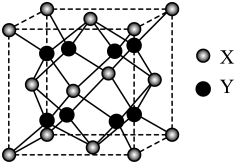 A、Y代表的离子是 B、与距离最近的数目为6 C、与距离最近的数目为12 D、阴阳离子的核间距最小为14. 关于如图有机物,下列说法不正确的是( )
A、Y代表的离子是 B、与距离最近的数目为6 C、与距离最近的数目为12 D、阴阳离子的核间距最小为14. 关于如图有机物,下列说法不正确的是( ) A、分子中存在1种含氧官能团 B、分子含有1个手性碳原子 C、与酸性高锰酸钾溶液反应,产物之一为对苯二甲酸 D、与酸或碱溶液反应都可生成盐15. 常温下,将一定量稀硫酸逐滴滴入高铁酸钠()溶液中,溶液中含铁微粒存在如下平衡: , 各微粒的物质的量分数随pOH变化如图。下列说法正确的是( )
A、分子中存在1种含氧官能团 B、分子含有1个手性碳原子 C、与酸性高锰酸钾溶液反应,产物之一为对苯二甲酸 D、与酸或碱溶液反应都可生成盐15. 常温下,将一定量稀硫酸逐滴滴入高铁酸钠()溶液中,溶液中含铁微粒存在如下平衡: , 各微粒的物质的量分数随pOH变化如图。下列说法正确的是( )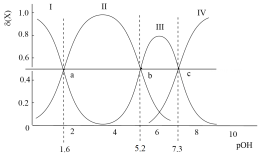 A、曲线IV代表变化 B、当时,溶液 C、 D、时,溶液中16. 下列方案设计、现象和结论都正确的是( )
A、曲线IV代表变化 B、当时,溶液 C、 D、时,溶液中16. 下列方案设计、现象和结论都正确的是( )A
探究固体样品是否变质
取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量溶液
若有白色沉淀产生,则样品已经变质
B
探究KI与反应的限度
取1mLKI溶液于试管中,加入3mL溶液,充分反应后滴入5滴15%KSCN溶液
若溶液变血红色,则KI与的反应有一定限度
C
验证分子中的碳碳双键
取样与适量溴水混合,充分反应,观察现象
溴水褪色,说明样品分子中含有碳碳双键
D
检验淀粉水解是否完全
将适量样品与稀硫酸反应,加入足量NaOH溶液后加入碘水,观察现象
无明显现象,说明淀粉水解完全
A、A B、B C、C D、D二、结构与性质
-
17. C、N、P、S及其化合物在医药化工领域应用十分广泛。请回答:(1)、①基态磷原子核外电子共有种运动状态。磷原子在成键时,能将一个3s电子激发进入3d能级而参与成键,写出该激发态磷原子的核外电子排布式。
②沸点:(填“>、<、=”),分析其原因。
(2)、氨硼烷(分子中N和B最外层均满足8电子),与水反应的离子方程式为: , 的结构为 。下列说法正确的是____。 A、中存在配位键,N原子提供孤电子对 B、该反应中,氧化剂是 C、第一电离能大小: D、该反应中,B原子的杂化轨道类型由变为(3)、单质硫和氢气一定条件下可形成一种新材料,其晶胞如图,晶胞边长为anm,表示阿伏加德罗常数的值,晶体密度为。
。下列说法正确的是____。 A、中存在配位键,N原子提供孤电子对 B、该反应中,氧化剂是 C、第一电离能大小: D、该反应中,B原子的杂化轨道类型由变为(3)、单质硫和氢气一定条件下可形成一种新材料,其晶胞如图,晶胞边长为anm,表示阿伏加德罗常数的值,晶体密度为。
三、元素或物质推断题
-
18. 黄褐色物质X(不含结晶水)由四种常见元素组成,不溶于水。某学习小组按如下流程进行实验:

已知:固体B为混合物,完全溶于硫酸溶液,过程中无气体放出。请回答:
(1)、X的组成元素是H、O、;固体X的化学式是。(2)、若X在500℃受热分解,得到一种红棕色固体和三种气体(500℃),则气体产物中除之外还有(填化学式)。(3)、溶液C中加铁粉至过量后得溶液M,利用热溶液M和稀硝酸可以制得X,请写出热溶液M和稀硝酸反应的离子方程式。(4)、设计实验检验溶液C中的阳离子。四、原理综合题
-
19. 是大气主要污染物之一,还原烟气中的回收S的相关反应如下:
I: , 活化能
II: , 活化能
请回答:
(1)、已知 , 则(填“>”、“<”或“=”)。(2)、反应I的平衡常数表达式为:。(3)、恒温恒容条件下进行上述反应,下列说法正确的是____。A、反应I在一定条件下自发进行, B、气体密度不变说明体系达到平衡 C、若 , 则体系中一定以反应I为主 D、通过监测反应体系中与S的浓度变化可判断反应I和反应II是否同时发生(4)、现以(一种多孔性物质,具有良好的吸附性能)作为催化剂,用CO去除烟气中的 , 反应相同的时间,的去除率随反应温度的变化如图所示。
反应温度低于240℃时,随着温度的升高,去除率降低的原因是。
(5)、恒温恒容条件下,保持、CO和C的投料比不变,请在下图中画出平衡时随压强变化示意图。
五、工业流程题
-
20. 某研究小组利用电解锰渣(主要成分是MnS,含少量、、CaO)制备高纯晶体,流程如下:
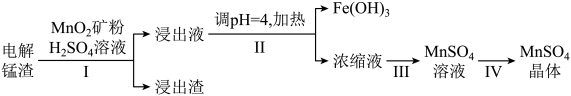 (1)、下列有关说法不正确的是____。A、过程I、II均涉及过滤操作 B、过程I,适当提高溶液浓度可提高锰的浸出率 C、过程I,加可减少有毒气体的生成 D、过程II,调pH最好选用NaOH溶液(2)、过程II需持续加热一段时间,目的是。(3)、过程III除去并富集的原理为:(油相)(油相)[表示或]。
(1)、下列有关说法不正确的是____。A、过程I、II均涉及过滤操作 B、过程I,适当提高溶液浓度可提高锰的浸出率 C、过程I,加可减少有毒气体的生成 D、过程II,调pH最好选用NaOH溶液(2)、过程II需持续加热一段时间,目的是。(3)、过程III除去并富集的原理为:(油相)(油相)[表示或]。实验步骤如下:
①调节浓缩液pH,加入溶有HA的磺化煤油,系列操作,分离得水层;
②继续调节水层pH,加入溶有HA的磺化煤油,系列操作,分离得油层;
③向②所得油层中加入试剂X,系列操作,得溶液。
上述步骤中的进行“系列操作”的主要仪器名称是 , 试剂X为。
(4)、不同温度下的溶解度如下表。温度/℃
0
20
40
60
80
100
溶解度/g
52.9
62.9
60.0
53.6
45.6
35.3
从下列选项中选择“过程IV”的正确操作并排序:
将溶液加热至100℃→→→洗涤→干燥
a.蒸发至出现大量晶体 b.蒸发至溶液表面出现晶膜
c.冷却结晶,过滤 d.趁热过滤
(5)、纯度的测定:准确称取mg产品,加入足量稀硫酸充分溶解后,加入足量固体(不溶于水)将完全转化为过滤,用的标准溶液滴定至终点,消耗20.00mL标准溶液,则的纯度为(用含m的代数式表示)。六、有机推断题
-
21. 某研究小组按下列路线合成某黄酮类物质H。
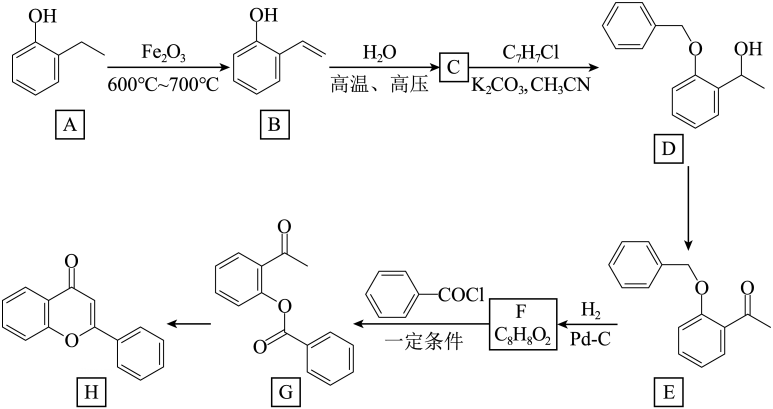
已知:

请回答:
(1)、化合物G的官能团名称是。(2)、化合物C的结构简式是。(3)、下列说法不正确的是____。A、A→B的反应类型为氧化反应 B、设计C→D反应的目的是保护酚羟基,防止其被还原 C、F→G的反应不用苯甲酸的原因可能是酚羟基和羧基不易发生反应 D、化合物H的分子式为(4)、写出F→G的化学方程式。(5)、设计以为原料合成 (用流程图表示,无机试剂任选)。 (6)、写出3种同时符合下列条件的化合物F的同分异构体的结构简式。
(用流程图表示,无机试剂任选)。 (6)、写出3种同时符合下列条件的化合物F的同分异构体的结构简式。①分子中含有苯环,不含“—O—O—”; ②分子中有3种不同化学环境的氢原子
-
-
-
-