浙江省温州新力量联盟2022-2023学年高二下学期期末检测化学试题
试卷更新日期:2023-08-16 类型:期末考试
一、单选题
-
1. 下列物质熔融状态下能导电且含有非极性键的氧化物的是( )A、 B、 C、MgO D、2. Ca(ClO)Cl具有强氧化剂的盐,下列说法不正确的是( )A、Ca元素位于周期表s区 B、Ca(ClO)Cl属于强电解质 C、其水溶液呈中性 D、Ca(ClO)Cl可作漂白剂3. 下列化学用语表示正确的是( )A、中子数为81的钡原子: B、铁的基态原子的价电子轨道表示式:
 C、的空间结构:正四面体形
D、的中心原子的杂化轨道类型:sp3
4. 物质的性质决定用途,下列两者对应关系正确的是( )A、能遇有色物质褪色,可用作葡萄酒抗氧化剂 B、二氧化硅硬度高,可用于制造光导纤维 C、溶液呈酸性,可用作消毒剂 D、钛合金与人体“相容性”好,可用于制造人造骨骼5. 下列关于元素及其化合物的性质说法正确的是( )A、实验室用和98%浓硫酸反应生成 B、将通入溶液中,制得以为有效成分的漂白粉 C、工业上用氨的催化氧化制备NO D、常温下铁与浓硝酸反应可制备6. 关于反应 , 下列说法正确的是( )A、KCl是还原产物 B、氧化剂与还原剂的物质的量之比为1∶6 C、HCl既有还原性又有酸性 D、生成67.2L , 转移5mol电子7. 下列反应的离子方程式正确的是( )A、通入氢氧化钠溶液: B、少量的通入亚硫酸钠溶液: C、向苯酚钠溶液中通入少量溶液变浑浊:
C、的空间结构:正四面体形
D、的中心原子的杂化轨道类型:sp3
4. 物质的性质决定用途,下列两者对应关系正确的是( )A、能遇有色物质褪色,可用作葡萄酒抗氧化剂 B、二氧化硅硬度高,可用于制造光导纤维 C、溶液呈酸性,可用作消毒剂 D、钛合金与人体“相容性”好,可用于制造人造骨骼5. 下列关于元素及其化合物的性质说法正确的是( )A、实验室用和98%浓硫酸反应生成 B、将通入溶液中,制得以为有效成分的漂白粉 C、工业上用氨的催化氧化制备NO D、常温下铁与浓硝酸反应可制备6. 关于反应 , 下列说法正确的是( )A、KCl是还原产物 B、氧化剂与还原剂的物质的量之比为1∶6 C、HCl既有还原性又有酸性 D、生成67.2L , 转移5mol电子7. 下列反应的离子方程式正确的是( )A、通入氢氧化钠溶液: B、少量的通入亚硫酸钠溶液: C、向苯酚钠溶液中通入少量溶液变浑浊: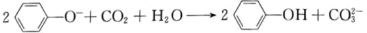 D、溶液中滴入氯化钙溶液:
8. 下列说法不正确的是( )A、纤维素可用于生产纸张、棉纱、合成纤维等 B、蛋白质溶液与浓硝酸作用产生白色沉淀,加热后沉淀变黄色 C、只用新制氢氧化铜悬浊液(可加热)就能区分乙醛、乙酸、葡萄糖、四氯化碳 D、DNA分子由两条多聚核苷酸链组成,两条链上的碱基通过氢键作用,互补配对9. 化合物“E7974”具有抗肿痛活性,结构简式如下,下列有关该化合物说法正确的是( )
D、溶液中滴入氯化钙溶液:
8. 下列说法不正确的是( )A、纤维素可用于生产纸张、棉纱、合成纤维等 B、蛋白质溶液与浓硝酸作用产生白色沉淀,加热后沉淀变黄色 C、只用新制氢氧化铜悬浊液(可加热)就能区分乙醛、乙酸、葡萄糖、四氯化碳 D、DNA分子由两条多聚核苷酸链组成,两条链上的碱基通过氢键作用,互补配对9. 化合物“E7974”具有抗肿痛活性,结构简式如下,下列有关该化合物说法正确的是( )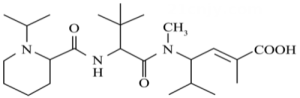 A、分子中含有4个手性碳原子 B、分子中含有3种官能团 C、能使酸性高锰酸钾溶液褪色 D、1mol该化合物最多与2molNaOH反应10. 前四周期元素W、X、Y、Z的原子序数依次增大。基态W原子中有7个运动状态不同的电子,X元素形成的某种单质是极性分子,基态Y原子的价层电子排布式为 , 基态Z原子次外层全充满,最外层电子数为1,下列说法正确的是( )A、空间构型是直线形 B、基态X原子的第一电离能比同周期相邻原子都要低 C、W和X的电负性:W>X D、单质Z与单质Y反应生成ZY11. 一种钠离子电池的工作原理如图所示,放电时电池反应可表示为。下列说法正确的是( )
A、分子中含有4个手性碳原子 B、分子中含有3种官能团 C、能使酸性高锰酸钾溶液褪色 D、1mol该化合物最多与2molNaOH反应10. 前四周期元素W、X、Y、Z的原子序数依次增大。基态W原子中有7个运动状态不同的电子,X元素形成的某种单质是极性分子,基态Y原子的价层电子排布式为 , 基态Z原子次外层全充满,最外层电子数为1,下列说法正确的是( )A、空间构型是直线形 B、基态X原子的第一电离能比同周期相邻原子都要低 C、W和X的电负性:W>X D、单质Z与单质Y反应生成ZY11. 一种钠离子电池的工作原理如图所示,放电时电池反应可表示为。下列说法正确的是( )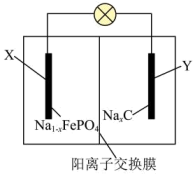 A、放电时,电能转化为化学能 B、放电时,Y极为正极,发生还原反应 C、充电时,X极电极反应式为 D、充电时,每转移1mol , Y极质量减少23g12. 近日科学家合成了一种新型芳香化合物 , 其结构中含有(平面正六边形,与苯的结构类似)、(平面正五边形)以及。下列说法不正确的是( )A、氮的原子结构示意图:
A、放电时,电能转化为化学能 B、放电时,Y极为正极,发生还原反应 C、充电时,X极电极反应式为 D、充电时,每转移1mol , Y极质量减少23g12. 近日科学家合成了一种新型芳香化合物 , 其结构中含有(平面正六边形,与苯的结构类似)、(平面正五边形)以及。下列说法不正确的是( )A、氮的原子结构示意图: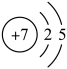 B、的电子式:
B、的电子式: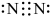 C、和中N原子杂化方式为
D、和中含有大键
13. 常温常压下,某同学向氨水中逐滴加入的盐酸,实验测得溶液的随加入盐酸体积的变化如图所示,其中N点为反应终点(此时盐酸与氨水恰好完全反应),此时消耗盐酸的体积为。下列说法中正确的是( )
C、和中N原子杂化方式为
D、和中含有大键
13. 常温常压下,某同学向氨水中逐滴加入的盐酸,实验测得溶液的随加入盐酸体积的变化如图所示,其中N点为反应终点(此时盐酸与氨水恰好完全反应),此时消耗盐酸的体积为。下列说法中正确的是( )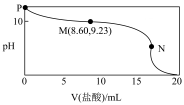
指示剂
pH范围及对应颜色
甲基橙
<3.1(红色)
3.1~4.4(橙色)
>4.4(黄色)
酚酞
<8.2(无色)
8.2~10.0(粉红色)
>10.0(红色)
A、选择甲基橙作指示剂,误差比酚酞的大 B、M点的溶液中存在 C、N点溶液中 D、P、M、N三点对应溶液中水的电离程度最大的为M点14. 一定条件下,反应物和生成物的相对能量与反应历程示意图如下,下列说法不正确的是( )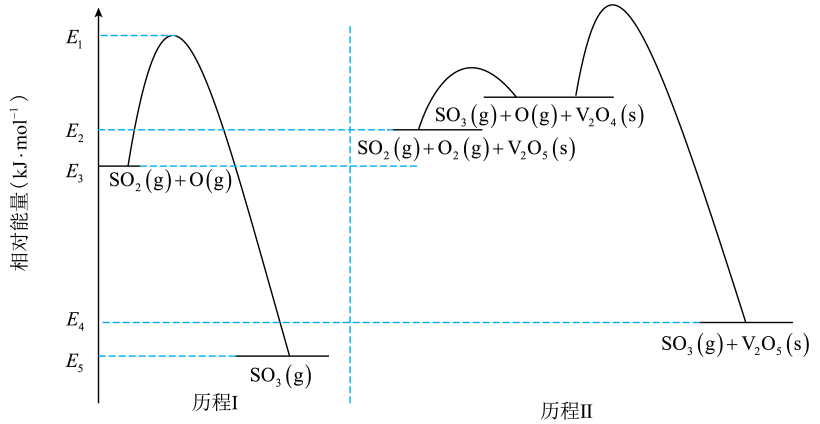 A、由历程I可计算,的总键能 B、由历程Ⅱ可知,相同条件下的浓度比的浓度对反应速度影响更大 C、相同条件下,的平衡转化率,历程I=历程Ⅱ D、由历程I和历程Ⅱ可得,15. 可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。已知:;。下列推断正确的是( )A、饱和溶液中存在: B、向、的饱和混合溶液中加入少量 , 溶液中减小 C、不用碳酸钡作为内服造影剂,是因为 D、若每次加入的溶液,至少需要6次可将转化为16. 下列实验方案能达到实验目的的是( )
A、由历程I可计算,的总键能 B、由历程Ⅱ可知,相同条件下的浓度比的浓度对反应速度影响更大 C、相同条件下,的平衡转化率,历程I=历程Ⅱ D、由历程I和历程Ⅱ可得,15. 可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。已知:;。下列推断正确的是( )A、饱和溶液中存在: B、向、的饱和混合溶液中加入少量 , 溶液中减小 C、不用碳酸钡作为内服造影剂,是因为 D、若每次加入的溶液,至少需要6次可将转化为16. 下列实验方案能达到实验目的的是( )选项
实验目的
实验方案
A
向两支分别盛有2mL苯和2mL甲苯的试管中各加入几滴酸性高锰酸钾溶液,用力振荡,观察现象
探究有机物中基团间的相互作用
B
检验中的溴元素
将与NaOH溶液混合加热,静置,向上层清液加入溶液,观察是否生成浅黄色沉淀
C
证明蔗糖与浓硫酸反应产生的气体中含
将气体通入澄清石灰水中,观察是否生成白色沉淀
D
用NaCl固体配制100mL1.00NaCl溶液
将5.85gNaCl固体放在烧杯中,加入100mL蒸馏水,搅拌
A、A B、B C、C D、D二、结构与性质
-
17. 我国科学家研究发现(家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题(1)、基态铬原子的价电子排布式为;基态硫原子核外电子的运动状态有种。(2)、同周期元素Si、P、S的第一电离能由大到小的顺序为(用元素符号表示)。(3)、硫元素能形成多种微粒如、、、、等。的中心原子的杂化类型是。(4)、中Cr元素化合价为+6价,常温下呈蓝色,则其结构式可能为(填标号)。



A
B
C
(5)、某含铬化合物立方晶胞如图所示。该晶体的化学式为。 (6)、已知晶体的密度为 , 为阿伏加德罗常数的值,则相邻与之间的最短距离为=pm(列出计算式即可)。
(6)、已知晶体的密度为 , 为阿伏加德罗常数的值,则相邻与之间的最短距离为=pm(列出计算式即可)。三、元素或物质推断题
-
18. 化合物X由三种前四周期常见元素组成,某学习小组按如下流程进行实验:
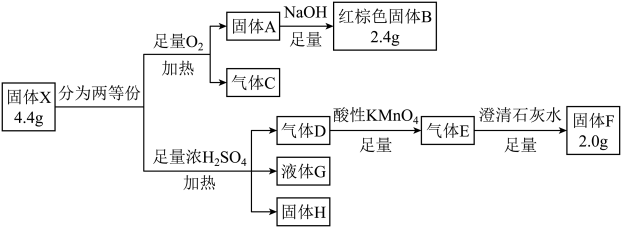
请回答:
(1)、E的电子式是 , X的化学式是。(2)、写出X与足量浓反应的化学方程式。(3)、写出气体D与酸性溶液反应的离子反应方程式。(4)、设计实验检验溶液G中的阳离子。四、原理综合题
-
19. 某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应: , 回答问题:(1)、已知:电解液态水制备1mol , 电解反应的。由此计算的燃烧热(焓)。(2)、已知:的平衡常数(K)与反应温度(t)之间的关系如图1所示。

①若反应为基元反应,且反应的与活化能()的关系为。补充完成该反应过程的能量变化示意图(图2)。
②某研究小组模拟该反应,温度t下,向容积为10L的抽空的密闭容器中通入0.1mol和0.4mol , 反应平衡后测得容器中。则的转化率为 , 反应温度t约为℃。
(3)、在相同条件下,与还会发生不利于氧循环的副反应: , 在反应器中按通入反应物,在不同温度、不同催化剂条件下,反应进行到2min时,测得反应器中、浓度()如下表所示。催化剂
t=350℃
t=400℃
催化剂I
10.8
12722
345.2
42780
催化剂II
9.2
10775
34
38932
若某空间站的生命保障系统实际选择使用催化剂II和400℃的反应条件,原因是。
(4)、某温度下,反应在密闭容器中达到平衡,下列说法正确的是____。A、增大压强, , 平衡常数不变 B、加入催化剂,平衡时的浓度增大 C、恒容下,充入一定量的稀有气体,平衡向正反应方向移动 D、催化剂II选择性地提高该反应的速率五、实验题
-
20. 小组同学探究和不同铜盐溶液的反应,实验如下。
实验:向2mL0.5000溶液中加入1mL0.2500溶液,立即产生橙黄色沉淀(沉淀A),放置5min左右,转化为白色沉淀(沉淀B)。
已知:i.
ii.
(1)、研究沉淀B的成分。向洗涤后的沉淀B中加入足量浓氨水,得到无色溶液,在空气中放置一段时间,溶液变为深蓝色。取少量深蓝色溶液,滴加试剂X,产生白色沉淀。
①配制0.2500溶液时用的玻璃定量仪器是 , X试剂是。
②无色溶液在空气中放置变为深蓝色,反应的离子方程式为。
(2)、经检验,沉淀A不含。推测沉淀A能转化为沉淀B与有关,为研究沉淀A的成分及沉淀A转化为B的原因,实验如下。
①仅通过上述实验不能证明沉淀A中含有 , 补充实验:向少量洗净的沉淀A加入稀硫酸,证实沉淀A中含有的证据是。
②无色溶液中含有 , 推测的产生有两个途径:
途径1:实验过程中氧化;
途径2:(将途径补充完整)。
经研究,途径1不合理,途径2合理。
③下列有关说法不正确的是。
A.和溶液生成棕黄色沉淀A的反应速率快
B.生成白色沉淀B的限度大
C.配合物中,给出孤对电子,提供空轨道
D.洗涤时,向沉淀物中加入洗涤剂至没过沉淀,搅拌,让洗涤剂顺利留下,多次操作
(3)、用和溶液重复上述实验,仅产生橙黄色沉淀,放置72h后变为暗红色沉淀(可溶于氨水,得到无色溶液,放置变为深蓝色)。根据上述实验所得结论:①和能发生复分解反应和氧化还原反应,且复分解反应速率更快;②。
六、有机推断题
-
21. 黄酮哌酯是一种解痉药,可通过如下路线合成:

回答问题:
(1)、化合物D的官能团名称是。(2)、黄酮哌酯的分子式是。(3)、下列说法正确的是____。A、A→B的反应类型为氧化反应 B、化合物B为一元强酸,可以制备合成洗涤剂 C、可以用溶液鉴别E和F D、化合物E与氢氧化钠溶液反应,耗2molNaOH(4)、写出D→E的反应方程式。(5)、X是F的分异构体,符合下列条件的X可能的结构简式为。①含有酯基②含有苯环③核磁共振氢谱有两组峰
(6)、设计以 为原料合成
为原料合成 的路线(其他试剂任选)。
的路线(其他试剂任选)。
-
-
-
-