新疆生产建设兵团第三师图木舒克市第一中学2022-2023学年高二下学期期末考试化学试题
试卷更新日期:2023-08-16 类型:期末考试
一、单选题
-
1. 通过践行“教育兴国,科技兴国”的发展战略,近年来诸多的“中国制造”享誉国内外。下列有关说法中正确的是( )A、磁悬浮列车中使用的聚氯乙烯塑料可由乙烯和通过加成反应制得 B、中国天眼“FAST”,用到的碳化硅是一种新型的有机非金属材料 C、北京冬奥会速滑竞赛服采用的聚氨酯材料可以通过缩聚反应制成 D、我国科学家实现了淀粉的人工合成,淀粉分子式为 , 属于纯净物2. 下列化学用语正确的是( )A、硝基苯的结构简式
 B、球棍模型
B、球棍模型 一定表示的是甲烷
C、顺-2-丁烯的键线式
一定表示的是甲烷
C、顺-2-丁烯的键线式 D、羟基的电子式:
D、羟基的电子式: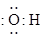 3. 有机化合物分子中原子或原子团之间相互影响会导致物质化学性质的不同。下列各项事实中,不能说明上述观点的是( )A、苯酚能跟浓溴水反应而苯不能 B、丙酮的氢原子比乙烷的氢原子活泼 C、苯酚显弱酸性而乙醇不显弱酸性 D、甲醛和甲酸都能发生银镜反应4. 下列各组有机物只用一种试剂无法鉴别的是( )A、乙醇、甲苯、硝基苯 B、苯、甲苯、环己烷 C、苯、苯酚、己烯 D、甲酸、乙醛、乙酸5. 有机物结构复杂,种类繁多主要是因为有机物中碳原子的连接方式多种多样,且存在同分异构现象,下列有关有机物结构说法正确的是( )A、
3. 有机化合物分子中原子或原子团之间相互影响会导致物质化学性质的不同。下列各项事实中,不能说明上述观点的是( )A、苯酚能跟浓溴水反应而苯不能 B、丙酮的氢原子比乙烷的氢原子活泼 C、苯酚显弱酸性而乙醇不显弱酸性 D、甲醛和甲酸都能发生银镜反应4. 下列各组有机物只用一种试剂无法鉴别的是( )A、乙醇、甲苯、硝基苯 B、苯、甲苯、环己烷 C、苯、苯酚、己烯 D、甲酸、乙醛、乙酸5. 有机物结构复杂,种类繁多主要是因为有机物中碳原子的连接方式多种多样,且存在同分异构现象,下列有关有机物结构说法正确的是( )A、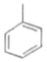 和
和 的一氯代物数相同(不考虑立体异构)
B、
的一氯代物数相同(不考虑立体异构)
B、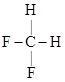 和
和 是同一种物质
C、
是同一种物质
C、 与
与 互为同分异构体
D、
互为同分异构体
D、 与
与 互为同系物
6. 立体异构包括顺反异构、对映异构等。有机物M(2-溴丁烷)存在如图转化关系,下列说法正确的是( )
互为同系物
6. 立体异构包括顺反异构、对映异构等。有机物M(2-溴丁烷)存在如图转化关系,下列说法正确的是( )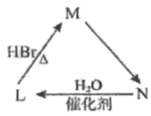 A、M转化为N所需的条件为水溶液加热 B、N分子能使溴水褪色,且不存在顺反异构 C、L的同分异构体中,能被氧化为醛的醇有4种 D、L的任一同分异构体中最多有1个手性碳原子7. 环丙叉环丙烷(b)由于其特殊的结构,一直受到结构和理论化学家的注意,根据其转化关系,下列说法正确的是( )
A、M转化为N所需的条件为水溶液加热 B、N分子能使溴水褪色,且不存在顺反异构 C、L的同分异构体中,能被氧化为醛的醇有4种 D、L的任一同分异构体中最多有1个手性碳原子7. 环丙叉环丙烷(b)由于其特殊的结构,一直受到结构和理论化学家的注意,根据其转化关系,下列说法正确的是( )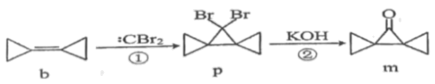 A、b二氯代物有4种同分异构体 B、①是加成反应,②是消去反应 C、m的芳香族同分异构体共有4种 D、b、m均能使酸性溶液褪色8. 下列物质的性质和应用叙述均正确,且有因果关系的是( )
A、b二氯代物有4种同分异构体 B、①是加成反应,②是消去反应 C、m的芳香族同分异构体共有4种 D、b、m均能使酸性溶液褪色8. 下列物质的性质和应用叙述均正确,且有因果关系的是( )选项
性质
应用
A
糖类在一定条件下能够发生水解
可用淀粉水解生成葡萄糖,葡萄糖水解成乙醇来酿酒
B
蛋白质的盐析是一个可逆的过程
向蛋白质溶液中加入 , 进行多次盐析可实现蛋白质的提纯
C
油脂在碱性条件下能够水解
可用碱溶液鉴别地沟油和矿物油
D
苯酚又名石炭酸,显酸性且有毒对皮肤有一定的腐蚀性
可用浓溶液洗涤沾到皮肤上的苯酚
A、A B、B C、C D、D9. 硼酸主要用于玻璃生产,能改善玻璃的耐热、透明性能,提高机械强度。硼酸是一元弱酸,其电离方程式如下,常温下,其电离常数。下列说法正确的是( )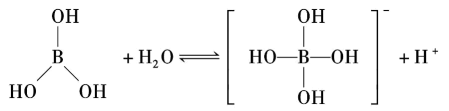 A、电离常数的表达式为 B、分子的空间构型为三角锥形 C、的中心原子的模型为四面体形 D、中普通共价键与配位键的个数之比为10. 光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
A、电离常数的表达式为 B、分子的空间构型为三角锥形 C、的中心原子的模型为四面体形 D、中普通共价键与配位键的个数之比为10. 光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。
下列说法错误的是
A、该高分子材料可降解 B、异山梨醇分子中有3个手性碳 C、反应式中化合物X为甲醇 D、该聚合反应为缩聚反应11. 下列关于化学键的说法正确的是:①s-sσ键与s-pσ键的电子云对称性相同
②物质只有发生化学变化时才会有化学键的断裂
③成键的原子间原子轨道重叠越多,共价键越牢固
④非金属元素之间形成的化合物中只含有共价键
⑤1个N原子最多只能与3个H原子结合形成分子,这是由共价键的饱和性决定的
A、①②③ B、①③⑤ C、②④⑤ D、③④⑤12. 下列表达方式或说法正确的是( )A、基态到激发态产生的光谱是发射光谱 B、氯化铵的电子式: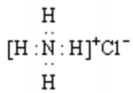 C、NH3、H2O、CO2、HCl 四分子中孤电子对最多的是 CO2
D、硫离子的核外电子排布式 1s22s22p63s23p4
13. 一种可吸附甲醇的材料,其化学式为 , 部分晶体结构如下图所示,其中为平面结构。
C、NH3、H2O、CO2、HCl 四分子中孤电子对最多的是 CO2
D、硫离子的核外电子排布式 1s22s22p63s23p4
13. 一种可吸附甲醇的材料,其化学式为 , 部分晶体结构如下图所示,其中为平面结构。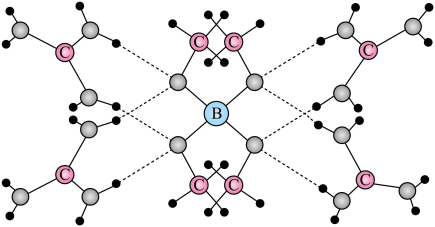
下列说法正确的是
A、该晶体中存在N-H…O氢键 B、基态原子的第一电离能: C、基态原子未成对电子数: D、晶体中B、N和O原子轨道的杂化类型相同14. 下列叙述中正确的是( )A、为角形的极性分子,形成分子晶体 B、的空间结构为平面三角形 C、氯化硼的熔点为 , 氯化硼液态时能导电而固态时不导电 D、和的中心原子均为杂化, 分子呈正四面体形,呈三角锥形15. 达芦那韦对新型冠状病毒有较好的抑制,灭活能力,其结构简式如图所示。下列有关达芦那韦的说法错误的是( ) A、分子中至少有7个碳原子共平面 B、能与金属钠反应放出氢气 C、分子中存在多种官能团,如羟基等 D、是高分子化合物
A、分子中至少有7个碳原子共平面 B、能与金属钠反应放出氢气 C、分子中存在多种官能团,如羟基等 D、是高分子化合物二、填空题
-
16. 某烃A的相对分子质量为84。回答下列问题:(1)、烃A的分子式为。(2)、下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是;若总质量一定,充分燃烧消耗氧气的量不变的是。
A.C7H8 B.C6H14 C.C7H14 D.C8H8
(3)、若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。 A的结构简式为 , 其名称为。(4)、若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为。其二氯代物有种。三、工业流程题
-
17. 己二酸是一种二元弱酸,通常为白色结晶体,微溶于冷水,易溶于热水和乙醇。实验室以环己醇(
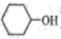 )为原料制取己二酸的实验流程如图:
)为原料制取己二酸的实验流程如图:
已知:①“氧化”过程在三项烧瓶(如下图1所示)中进行,发生的主要反应为:

②不同温度下,相关物质在水中的溶解度如下表:
物质
己二酸
氯化钠
氯化钾
25℃时溶解度/g
2.1
36.1
34.3
70℃时溶解度/g
68
37.8
48
100℃时溶解度/g
160
39.5
56.3
回答下列问题:
(1)、环己醇的分子式为 , 其中所有碳原子一定(填“能”或“不能”)共面。(2)、操作1的名称为。(3)、图1中恒压滴液漏斗侧管的作用为:。 (4)、“氧化”过程在环己醇不同滴速下,溶液温度随时间变化曲线如图2所示,实验过程中应选择的环己醇滴速为滴/min。
(4)、“氧化”过程在环己醇不同滴速下,溶液温度随时间变化曲线如图2所示,实验过程中应选择的环己醇滴速为滴/min。 (5)、己二酸晶体“洗涤”的方法为____(填字母)。A、用冷水洗涤 B、用热水洗涤 C、用乙醇洗涤(6)、除去己二酸晶体中含有的氯化钠杂质通常采取的实验方法名称为。(7)、实验时称取的环己醇质量为 , 最终得到纯净的己二酸晶体 , 则该实验中己二酸的产率为%(保留两位有效数字)。
(5)、己二酸晶体“洗涤”的方法为____(填字母)。A、用冷水洗涤 B、用热水洗涤 C、用乙醇洗涤(6)、除去己二酸晶体中含有的氯化钠杂质通常采取的实验方法名称为。(7)、实验时称取的环己醇质量为 , 最终得到纯净的己二酸晶体 , 则该实验中己二酸的产率为%(保留两位有效数字)。四、结构与性质
-
18. 2023年1月30日,中国科学院朱庆山团队研究六方相砷化镍(NiAs)型到正交相磷化锰(MnP)型结构转变,实现了对锂硫催化剂的精确设计。回答下列问题:(1)、第三周期元素中第一电离能比P大的元素有种。(2)、基态As原子的电子排布式为。(3)、与的空间构型均为 , 其中沸点较高的是 , 键角较大的是。(4)、Mn的一种配合物化学式为[],该配合物中锰原子的配位数为。(5)、中C原子的杂化类型为。(6)、等物质的量的和CO中,π键数目之比。(7)、NiAs的一种晶胞结构如图所示。若阿伏加德罗常数的值为 , 晶体的密度为ρ , 则该晶胞中最近的砷原子之间的距离为pm(列出计算式)。

五、有机推断题
-
19. 3,4-二羟基肉桂酸乙酯(
 )具有抗炎作用和治疗自身免疫性疾病的潜力。由气体A制备该物质的合成路线如下:
)具有抗炎作用和治疗自身免疫性疾病的潜力。由气体A制备该物质的合成路线如下: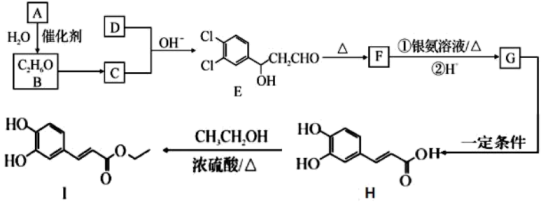
已知:

回答下列问题:
(1)、D的结构简式为。(2)、E中含有的含氧官能团的名称为。(3)、E→F、G→H的反应类型分别是、。(4)、反应E→F的化学方程式为。(5)、芳香族化合物X是H的同分异构体,其苯环上有三个取代基,1molX与足量溶液反应可生成2mol , 符合条件的X有种,其中核磁共振氢谱的峰面积比为3:2:2:1的结构简式为(写出一种)。(6)、根据上述路线中的相关知识,设计以乙醛为主要原料制备 的合成路线。
的合成路线。
-
-
-