江苏省宿迁市2023年中考化学真题
试卷更新日期:2023-08-16 类型:中考真卷
一、单选题
-
1. 我国传统文化源远流长,下列相关制作过程中一定发生了化学变化的是( )A、丝绸刺绣 B、手工剪纸 C、玉柄雕琢 D、烧制陶器2. 下列实验操作正确的是( )A、
 检查装置气密性
B、
检查装置气密性
B、 测溶液
C、
测溶液
C、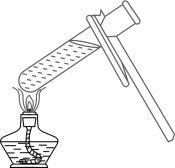 加热液体
D、
加热液体
D、 读液体体积
3. 下列说法正确的是( )A、人类利用的能量都是通过燃烧获得的 B、原子得失电子变成离子后,元素种类发生了改变 C、回收废旧金属有利于金属资源的充分利用 D、原子核都是由质子和中子构成的4. 金银花作为常见的中药材,具有清热解毒、消炎退肿等功效,其有效成分之一是绿原酸。下列有关绿原酸的说法正确的是( )A、绿原酸分子由碳、氢、氧三个元素组成 B、绿原酸中碳元素的质量分数最大 C、绿原酸的相对分子质量是 D、绿原酸中碳、氢、氧元素的质量比为5. 热爱劳动从我做起。下列家务劳动中所涉及的化学知识错误的是( )
读液体体积
3. 下列说法正确的是( )A、人类利用的能量都是通过燃烧获得的 B、原子得失电子变成离子后,元素种类发生了改变 C、回收废旧金属有利于金属资源的充分利用 D、原子核都是由质子和中子构成的4. 金银花作为常见的中药材,具有清热解毒、消炎退肿等功效,其有效成分之一是绿原酸。下列有关绿原酸的说法正确的是( )A、绿原酸分子由碳、氢、氧三个元素组成 B、绿原酸中碳元素的质量分数最大 C、绿原酸的相对分子质量是 D、绿原酸中碳、氢、氧元素的质量比为5. 热爱劳动从我做起。下列家务劳动中所涉及的化学知识错误的是( )选项
家务劳动
化学知识
A
将洗净的铁锅擦干水放置
潮湿的铁锅在空气中易生锈
B
用洗涤剂清洗餐具上的油污
洗涤剂能乳化油污
C
用食醋除去水壶内的水垢
食醋的
D
在阳光较好的地方晾晒湿衣服
水分子获得能量,运动速率加快
A、A B、B C、C D、D6. 乙醇作为一种清洁能源,已成为各国可再生能源的发展重点之一。下图为乙醇充分燃烧的微观示意图,下列有关该区应的说法正确的是( ) A、反应生成丙和丁的分子个数比是2:3 B、反应前后原子种类发生改变 C、反应前后各元素的化合价均没有变化 D、该反应中共涉及到三种氧化物7. 下列各组离子在溶液中能大量共存,并形成无色溶液的是( )A、、、、 B、、、、 C、、、、 D、、、、8. 如图是硝酸钾和氯化钾的溶解度曲线,下列说法正确的是( )
A、反应生成丙和丁的分子个数比是2:3 B、反应前后原子种类发生改变 C、反应前后各元素的化合价均没有变化 D、该反应中共涉及到三种氧化物7. 下列各组离子在溶液中能大量共存,并形成无色溶液的是( )A、、、、 B、、、、 C、、、、 D、、、、8. 如图是硝酸钾和氯化钾的溶解度曲线,下列说法正确的是( ) A、氯化钾的溶解度比硝酸钾小 B、时,硝酸钾和氯化钾溶液的溶质质量分数一定相等 C、将时硝酸钾饱和溶液降温至 , 溶液质量不变 D、时,硝酸钾饱和溶液中溶质与溶剂的质量比为11:109. 分类法是学习化学常用的一种方法。下列选项不符合图示关系(a、b为并列关系,分别包含c、d)的是( )
A、氯化钾的溶解度比硝酸钾小 B、时,硝酸钾和氯化钾溶液的溶质质量分数一定相等 C、将时硝酸钾饱和溶液降温至 , 溶液质量不变 D、时,硝酸钾饱和溶液中溶质与溶剂的质量比为11:109. 分类法是学习化学常用的一种方法。下列选项不符合图示关系(a、b为并列关系,分别包含c、d)的是( )
选项
a
b
c
d
A
物理性质
化学性质
溶解性
还原性
B
单质
化合物
液氮
二氧化锰
C
化合物
有机物
氯化钠
碳酸
D
纯净物
混合物
冰水混合物
蔗糖溶液
A、A B、B C、C D、D10. 将一定质量的粉加和的混合溶液中,充分反应后过滤,得滤渣和滤液。下列说法正确的是( )A、滤渣质量与加入的粉质量可能相等 B、滤液中一定有、 , 可能有 C、若加入的Fe粉过量,则得到的滤液呈无色 D、若向滤渣中加入稀盐酸,有气泡生成,则滤渣中一定有二、填空题
-
11. 2023年5月30日,神舟十六号载人飞船成功对接于空间站天和核心舱径向端口,三名航天员顺利进驻空间站。(1)、空间站实验舱使用的柔性三结砷化镓太阳能电池中含有镓(Ca)元素。金属镓由(填“分子”、“原子”或“离子”)构成。(2)、航天员通过航天食品摄入优质蛋白质、补充钙元素。
①下列航天食品中,富含蛋白质的是(填字母)
A.脱水米饭 B.酱牛肉 C.冻干草莓
②在人体中,钙元素属于元素(填“常量”或“微量”)。
(3)、制造飞船的某些机器零件使用了铝合金,铝合金属于材料。铝具有很好的抗腐蚀性能,是因为铝在常温下就能与氧气发生反应,生成一层致密而坚固的保护膜,写出该反应的化学方程式:。12. 习近平总书记在三亚考察时指出,一定要向海洋进军,加快建设海洋强国。海洋是一个巨大的资源宝库,我们应予以合理开发及综合利用。(1)、海水淡化。蒸馏法是常用的海水淡化方法,该方法是利用海水中各物质的不同,将水分离出来。(2)、海水“晒盐”。通常采用(填“降温”或“蒸发”)结晶的方法使海水中的氯化钠析出。(3)、海水“制碱”。下图是氨碱法生产纯碱的流程图。
①过滤操作中玻璃棒的作用是。
②碳酸氢钠受热分解的化学方程式为。
③我国化学家侯德榜在氨碱法的基础区,创立了更为先进的联合制碱法,使其中的单独结晶析出,用作氮肥。常见化肥除了氮肥,还有磷肥、钾肥和复合肥,下列属于复合肥的是。(填字母)。
A. B. C. D.
三、实验题
-
13. 下图为实验室常用仪器和装置的示意图,根据题意回答问题。
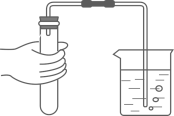
 (1)、写出标号①的仪器名称:。(2)、实验室制取时,可用装置收集,说明具有的物理性质是;若要测量产生的体积,应将装置的(填“a”或“b”)端与量筒连接。(3)、实验室制取的化学方程式为。若要控制反应的发生与停止,应选择的发生装置是(填字母);若要获得干燥的 , 可将发生装置与装置连接,中应盛放的试剂是(填名称)。14. 学习小组在老师的指导下对氢氧化钠、氧氧化钙的性质进行探究。
(1)、写出标号①的仪器名称:。(2)、实验室制取时,可用装置收集,说明具有的物理性质是;若要测量产生的体积,应将装置的(填“a”或“b”)端与量筒连接。(3)、实验室制取的化学方程式为。若要控制反应的发生与停止,应选择的发生装置是(填字母);若要获得干燥的 , 可将发生装置与装置连接,中应盛放的试剂是(填名称)。14. 学习小组在老师的指导下对氢氧化钠、氧氧化钙的性质进行探究。I.探究的性质:同学们设计如图所示实验。
 (1)、实验一中酚酞试液变红,说明溶液显性。(2)、实验二、实验三验证了能与某些发生反应(填物质类别)。写出实验三中发生反应的化学方程式:。(3)、实验四中滴入浓溶液后观察到的现象是。(4)、II.探究的性质:甲、乙两位同学分别取 , 固体于试管中,各加入水,充分振荡,均得到悬浊液。
(1)、实验一中酚酞试液变红,说明溶液显性。(2)、实验二、实验三验证了能与某些发生反应(填物质类别)。写出实验三中发生反应的化学方程式:。(3)、实验四中滴入浓溶液后观察到的现象是。(4)、II.探究的性质:甲、乙两位同学分别取 , 固体于试管中,各加入水,充分振荡,均得到悬浊液。甲同学将盛悬浊液的试管静置后,吸取上层清液滴入盛有少量碳酸钠溶液的试管中,观察到有白色沉淀产生,该反应的化学方程式为。
(5)、如下图所示,乙同学向盛悬浊液的试管中滴入2滴酚酞试液,振荡、静置后,观察到试管底部有固体,上层清液呈红色,然后向试管中逐滴加入稀盐酸至上层清液变为无色,该过程中发生反应的实质是;再将试管振荡、静置,上层清液又变成红色,其原因。
四、推断题
-
15. 是初中化学常见的物质,其中是赤铁矿的主要成分,、是组成元素相同的两种气体,E的浓溶液稀释时会放出大量的热,是最常用的溶剂,它们之间的关系如图所示(其中“-”代表物质间能发生反应,“→”代表物质间能够转化,部分反应物、生成物和反应条件已略去)。
 (1)、与反应的实验现象为。(2)、列举物质的一条用途:。(3)、物质I由构成(填化学用语)。(4)、写出与的稀溶液反应的化学方程式: , 其基应类型为。
(1)、与反应的实验现象为。(2)、列举物质的一条用途:。(3)、物质I由构成(填化学用语)。(4)、写出与的稀溶液反应的化学方程式: , 其基应类型为。五、计算题
-
16. 我们的祖先很早就掌握了炼铜的工艺,他们将孔雀石[主要成分是和木炭一起加热就可得到红色的铜。兴趣小组为测定某孔雀石中的质量分数,进行如下实验:称取孔雀石样品,粉碎后放入烧杯,向其中加入稀硫酸(稀硫酸过量),充分反应后称量,烧杯内物质的总质量为220.6g(假设杂质都不与稀硫酸发生反应)。(1)、。(2)、生成气体的质量是g。(3)、求该孔雀石中的质量分数(写出计算过程)。
-